й«ҳдёӯеҢ–еӯҰдәәж•ҷзүҲпјҲ2019пјүеҝ…дҝ®з¬¬дёҖеҶҢ第дёүз« е®һйӘҢжҙ»еҠЁ2 й“ҒеҸҠе…¶еҢ–еҗҲзү©зҡ„жҖ§иҙЁ
ж•ҷжқҗзүҲжң¬пјҡеҢ–еӯҰ
иҜ•еҚ·еҲҶзұ»пјҡеҢ–еӯҰй«ҳдёҖдёҠеӯҰжңҹ
иҜ•еҚ·еӨ§е°Ҹпјҡ1.0 MB
ж–Ү件зұ»еһӢпјҡ.doc жҲ– .pdf жҲ– .zip
еҸ‘еёғж—¶й—ҙпјҡ2024-05-01
жҺҲжқғж–№ејҸпјҡе…Қиҙ№дёӢиҪҪ
дёӢиҪҪең°еқҖпјҡзӮ№жӯӨдёӢиҪҪ
д»ҘдёӢдёәиҜ•еҚ·йғЁеҲҶиҜ•йўҳйў„и§Ҳ
| 1. еЎ«з©әйўҳ | |
|
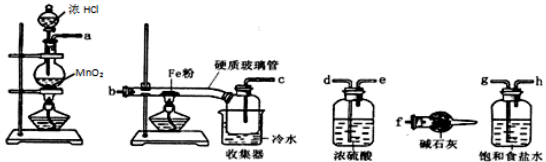
еңЁеҰӮеӣҫиЈ…зҪ®дёӯпјҢз”ЁNaOHжә¶ж¶ІгҖҒй“Ғеұ‘гҖҒзЁҖзЎ«й…ёзӯүиҜ•еүӮеҲ¶еӨҮFeпјҲOHпјү2 пјҺ
пјҲ1пјүеңЁиҜ•з®ЎIдёӯеҠ е…Ҙзҡ„иҜ•еүӮжҳҜ пјҺ пјҲ2пјүдёәдәҶеҲ¶еҫ—FeпјҲOHпјү2зҷҪиүІжІүж·ҖпјҢеңЁиҜ•з®ЎIе’Ңв…ЎдёӯеҠ е…ҘиҜ•еүӮпјҢжү“ејҖжӯўж°ҙеӨ№пјҢеЎһзҙ§еЎһеӯҗеҗҺи§ӮеҜҹеҲ°иҜ•з®ЎIдә§з”ҹеӨ§йҮҸж°”дҪ“пјҺдёҖж®өж—¶й—ҙеҗҺпјҢжЈҖйӘҢеҲ°иҜ•з®Ўв…Ўж”Ҝз®ЎеҮәеҸЈзҡ„ж°”дҪ“еҸӘжңүдёҖз§Қж—¶пјҢеҶҚиҝӣиЎҢзҡ„ж“ҚдҪңжҳҜ пјҢдҪҝиҜ•з®ЎIдёӯзҡ„жә¶ж¶Іиҝӣе…ҘеҲ°иҜ•з®Ўв…Ўдёӯжә¶ж¶Іеә•йғЁпјҢдә§з”ҹFeпјҲOHпјү2 пјҺ пјҲ3пјүиҝҷж ·з”ҹжҲҗзҡ„FeпјҲOHпјү2жІүж·ҖиғҪиҫғй•ҝж—¶й—ҙдҝқжҢҒзҷҪиүІпјҢе…¶зҗҶз”ұжҳҜ пјҺ пјҲ4пјүеҸҚеә”з»“жқҹеҗҺпјҢе°ҶFeпјҲOHпјү2жІүж·ҖеҖ’еҮәпјҢеңЁз©әж°”дёӯиҝ…йҖҹеҸҳдёәзҒ°з»ҝиүІпјҢжңҖеҗҺеҸҳдёәзәўиӨҗиүІпјҢе…¶еҺҹеӣ жҳҜгҖҖ пјҲз”ЁеҢ–еӯҰж–№зЁӢејҸиЎЁзӨәпјүпјҺ
|
|
| 2. еЎ«з©әйўҳ | |
|
з”ЁдёӢйқўдёӨз§Қж–№жі•еқҮеҸҜеҲ¶еҫ—FeпјҲOHпјү2зҷҪиүІжІүж·ҖпјҺ
ж–№жі•дёҖпјҡз”ЁдёҚеҗ«Fe3+зҡ„FeSO4жә¶ж¶ІдёҺдёҚеҗ«O2зҡ„и’ёйҰҸж°ҙй…ҚеҲ¶зҡ„NaOHжә¶ж¶ІеҸҚеә”еҲ¶еӨҮпјҺ пјҲ1пјүз”ЁзЎ«й…ёдәҡй“Ғжҷ¶дҪ“й…ҚеҲ¶дёҠиҝ°FeSO4жә¶ж¶Іж—¶иҝҳйңҖиҰҒеҠ е…Ҙ пјҺ пјҲ2пјүйҷӨеҺ»и’ёйҰҸж°ҙдёӯжә¶и§Јзҡ„O2еёёйҮҮз”Ё зҡ„ж–№жі•пјҺ пјҲ3пјүеҲ¶еҸ–FeпјҲOHпјү2зҷҪиүІжІүж·Җзҡ„ж“ҚдҪңжҳҜз”Ёй•ҝж»ҙз®ЎеҗёеҸ–дёҚеҗ«O2зҡ„NaOHжә¶ж¶ІпјҢжҸ’е…ҘFeSO4жә¶ж¶Іж¶ІйқўдёӢпјҢеҶҚжҢӨеҮәNaOHжә¶ж¶ІпјҺиҝҷж ·ж“ҚдҪңзҡ„зҗҶз”ұжҳҜпјҡйҳІжӯўеҸ‘з”ҹеҸҚеә” пјҺпјҲеЎ«еҢ–еӯҰж–№зЁӢејҸпјү ж–№жі•дәҢгҖҖеңЁеҰӮеӣҫжүҖзӨәзҡ„иЈ…зҪ®дёӯпјҢз”ЁNaOHжә¶ж¶ІгҖҒй“Ғеұ‘гҖҒзЁҖH2SO4зӯүиҜ•еүӮеҲ¶еӨҮпјҺ пјҲ4пјүеңЁиҜ•з®Ўв… йҮҢеҠ е…Ҙзҡ„иҜ•еүӮжҳҜ пјҺ пјҲ5пјүдёәдәҶеҲ¶еҫ—FeпјҲOHпјү2зҷҪиүІжІүж·ҖпјҢеңЁиҜ•з®Ўв… е’Ңв…ЎдёӯеҠ е…ҘиҜ•еүӮпјҢжү“ејҖжӯўж°ҙеӨ№пјҢеЎһзҙ§еЎһеӯҗеҗҺзҡ„е®һйӘҢжӯҘйӘӨжҳҜ пјҺ
|
|
| 3. еӨҡйҖүйўҳ | |
|
дёӢеҲ—е…ідәҺFe(OH)2зҡ„еҲ¶еӨҮиғҪеӨҹжҲҗеҠҹзҡ„жҳҜпјҲ пјү
A . еҗ‘FeCl2жә¶ж¶ІдёӯйҖҗж»ҙеҠ е…ҘNaOHжә¶ж¶І
B . еҗ‘FeSO4жә¶ж¶ІдёӯйҖҗж»ҙеҠ е…Ҙж°Ёж°ҙ
C . е…Ҳе°ҶиЈ…жңүNaOHжә¶ж¶Ізҡ„й•ҝж»ҙз®ЎжҸ’е…ҘFeSO4жә¶ж¶Іж¶ІйқўдёӢпјҢеҶҚжҢӨеҮәNaOHжә¶ж¶ІеҸҜеҲ¶еҫ—Fe(OH)2зҷҪиүІжІүж·Җ
D . еҸ–йҖӮйҮҸж–°й…ҚеҲ¶зҡ„FeSO4жә¶ж¶ІдәҺиҜ•з®ЎдёӯпјҢеҶҚеҠ е…ҘдёҖеұӮжӨҚзү©жІ№(еҜҶеәҰе°ҸдәҺж°ҙпјҢдё”дёҚжә¶дәҺж°ҙ)пјҢ然еҗҺеҗ‘иҜ•з®ЎеҶ…йҖҗж»ҙеҠ е…ҘNaOHжә¶ж¶І
|
|
| 4. еҚ•йҖүйўҳ | |
|
ж¬ІиҝӣиЎҢдёӢеҲ—е®һйӘҢпјҢе…¶ж–№жЎҲи®ҫи®ЎеҗҲзҗҶзҡ„жҳҜпјҲ пјү
A . еӣҫ1дёәеҲ¶еӨҮFe(OH)2
B . еӣҫ2дёәжҜ”иҫғNa2CO3е’ҢNaHCO3зҡ„зЁіе®ҡжҖ§
C . еӣҫ3дёәйӘҢиҜҒSO2зҡ„иҝҳеҺҹжҖ§
D . еӣҫ4дёәйӘҢиҜҒCl2е…·жңүжјӮзҷҪжҖ§
|
|
| 5. еҚ•йҖүйўҳ | |
|
дёӢеҲ—зҰ»еӯҗжЈҖйӘҢж“ҚдҪңгҖҒз»“и®әеқҮеҗҲзҗҶзҡ„жҳҜпјҲ пјү
A . з”ЁAgNO3жә¶ж¶ІжЈҖйӘҢClпјҚж—¶пјҢе…ҲеҠ е…ҘйҖӮйҮҸзЁҖзӣҗй…ёд»ҘжҺ’йҷӨCO32пјҚе№Іжү°
B . жҹҗжә¶ж¶Ідёӯж»ҙеҠ KSCNжә¶ж¶Іе‘ҲзәўиүІпјҢиҜҙжҳҺдёҚеҗ«Fe2пјӢ
C . жҹҗжә¶ж¶Ідёӯж»ҙеҠ ж°Ҝж°ҙеҗҺеҶҚж»ҙеҠ KSCNжә¶ж¶Іе‘ҲзәўиүІпјҢиҜҙжҳҺеҺҹжә¶ж¶Іеҗ«жңүFe3пјӢ
D . жҹҗж— иүІжә¶ж¶Ідёӯж»ҙеҠ ж°Ҝж°ҙеҗҺжә¶ж¶Іе‘ҲжЈ•иүІпјҢеҶҚж»ҙеҠ ж·ҖзІүжә¶ж¶Іжҳҫи“қиүІпјҢиҜҙжҳҺеҺҹжә¶ж¶Ідёӯеҗ«жңүIпјҚ
|
|
| 6. еҚ•йҖүйўҳ | |
|
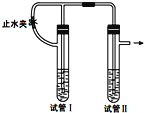
дёӢеҲ—еҗ„еӣҫзӨәдёӯиғҪиҫғй•ҝж—¶й—ҙзңӢеҲ° Fe(OH)2зҷҪиүІжІүж·Җзҡ„жҳҜпјҲ пјү
(е·ІзҹҘпјҡиӢҜдёәйҡҫжә¶дәҺж°ҙдё”еҜҶеәҰжҜ”ж°ҙе°Ҹзҡ„ж¶ІдҪ“)
A . в‘ в‘Ўв‘ў
B . в‘ в‘Ўв‘Ј
C . в‘ в‘ўв‘Ј
D . в‘Ўв‘ўв‘Ј
|
|
| 7. еҚ•йҖүйўҳ | ||||||||||||||||
|
дёӢеҲ—е®һйӘҢж“ҚдҪңе’ҢзҺ°иұЎгҖҒз»“и®әжҲ–зӣ®зҡ„еқҮжӯЈзЎ®зҡ„жҳҜ( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 8. еҚ•йҖүйўҳ | |
|
дёӢеҲ—зү©иҙЁеҸҚеә”еҗҺдёҖе®ҡжңү+3д»·й“Ғз”ҹжҲҗзҡ„жҳҜпјҲ пјү
в‘ иҝҮйҮҸзҡ„FeеңЁCl2дёӯзҮғзғ§пјӣв‘ЎFeе’ҢиҝҮйҮҸзӣҗй…ёеҸҚеә”пјӣв‘ўеҗ‘FeCl2жә¶ж¶ІдёӯйҖҡе…Ҙе°‘йҮҸCl2пјӣв‘Је°ҶFeе’ҢFe2O3зҡ„ж··еҗҲзү©жә¶дәҺзӣҗй…ёдёӯ
A . в‘
B . в‘ в‘ў
C . в‘ в‘Ўв‘ў
D . в‘ в‘Ўв‘ўв‘Ј
|
|
| 9. еҚ•йҖүйўҳ | |
|
жҹҗе…ҙи¶Је°Ҹз»„жҺўз©¶ SO2 ж°”дҪ“иҝҳеҺҹ Fe3пјӢ пјҢ 他们дҪҝз”Ёзҡ„иҚҜе“Ғе’ҢиЈ…зҪ®еҰӮдёӢеӣҫжүҖзӨәпјҢдёӢеҲ—иҜҙжі•дёҚеҗҲзҗҶзҡ„жҳҜ( )
A . B дёӯзҺ°иұЎдёәжә¶ж¶Іи“қиүІиӨӘеҺ»
B . иЈ…зҪ® C зҡ„дҪңз”ЁжҳҜеҗёж”¶ SO2 е°ҫж°”пјҢйҳІжӯўжұЎжҹ“з©әж°”
C . дёәдәҶйӘҢиҜҒ A дёӯеҸ‘з”ҹдәҶж°§еҢ–иҝҳеҺҹеҸҚеә”пјҢеҠ е…Ҙ KMnO4 жә¶ж¶ІпјҢзҙ«зәўиүІиӨӘеҺ»
D . еҸҚеә”еҗҺпјҢA дёӯжә¶ж¶Ізҡ„й…ёжҖ§еўһејә
|
|
| 10. е®һйӘҢжҺўз©¶йўҳ | |
|
е·ІзҹҘдёүж°ҜеҢ–й“Ғзҡ„зҶ”зӮ№дёә306в„ғпјҢжІёзӮ№дёә315в„ғпјҢжҳ“жә¶дәҺж°ҙ并且жңүејәзғҲзҡ„еҗёж°ҙжҖ§пјҢиғҪеҗёж”¶з©әж°”йҮҢзҡ„ж°ҙеҲҶиҖҢжҪ®и§ЈгҖӮжҹҗеӯҰд№ е°Ҹз»„зҡ„еҗҢеӯҰеҜ№ж°Ҝж°”дёҺй“Ғзҡ„еҸҚеә”еҸҠдә§зү©еҒҡдәҶеҰӮдёӢжҺўз©¶е®һйӘҢпјҡ
|
|
- 2022е№ҙй«ҳиҖғеҢ–еӯҰиҖғеүҚзҹҘиҜҶдё“йўҳеӨҚд№ 11 еёёи§ҒйҮ‘еұһе…ғзҙ еҸҠе…¶еҢ–еҗҲзү©
- еҶ…й»„дёҖдёӯй«ҳдёҖ12жңҲжңҲиҖғеҢ–еӯҰиҜ•йўҳеҸҠзӯ”жЎҲ
- жҳҢе№іеҢәй«ҳдёҖеҢ–еӯҰжңҹжң«иҜ•еҚ·еҸҠзӯ”жЎҲ
- йҖүдҝ®еӣӣ第дёүз« ж°ҙжә¶ж¶Ідёӯзҡ„зҰ»еӯҗе№іиЎЎиғҪеҠӣжЈҖжөӢйўҳеҸҠзӯ”жЎҲи§Јжһҗ
- йҖүдҝ®1-1 4.3еһғеңҫиө„жәҗеҢ–иҜҫ件еҸҠз»ғд№ йўҳеҗ«зӯ”жЎҲиҜҰи§Ј
- й«ҳдёүеҢ–еӯҰдёҖиҪ®еӨҚд№ зү©иҙЁзҡ„з»„жҲҗгҖҒеҲҶзұ»гҖҒжҖ§иҙЁдёҺз”ЁйҖ”еӨҚд№ йўҳеҸҠзӯ”
- еҚ—жҳҢеёӮдёүж ЎиҒ”иҖғй«ҳдәҢ1жңҲеҢ–еӯҰиҜ•еҚ·еҸҠзӯ”жЎҲ
- й«ҳдёӯеҢ–еӯҰеӯҰдёҡж°ҙе№іеӨҚд№ йўҳпјҡеҚҒе…« еҢ–еӯҰе®һйӘҢеҹәзЎҖзҹҘиҜҶ
- ж·®е®үеёӮдёңж–№еҸҢиҜӯеӯҰж Ўй«ҳдәҢе…ғжңҲжңҲиҖғеҢ–еӯҰиҜ•йўҳеҸҠзӯ”жЎҲ
- е…°е·һдёҖдёӯ第2еӯҰжңҹй«ҳдәҢеҢ–еӯҰжңҹжң«иҜ•еҚ·еҸҠзӯ”жЎҲ
- 2022е№ҙй«ҳиҖғеҢ–еӯҰиҖғеүҚзҹҘиҜҶдё“йўҳеӨҚд№ 16 жңүжңәеҢ–еӯҰеҹәзЎҖпјҲйҖүиҖғпјү
- жҳҢе№іеҢәй«ҳдёүеҢ–еӯҰжңҹжң«иҜ•еҚ·еҸҠзӯ”жЎҲ





 жә¶ж¶Іж»ҙеҠ еҲ°жө“
жә¶ж¶Іж»ҙеҠ еҲ°жө“  жә¶ж¶Ідёӯ
жә¶ж¶Ідёӯ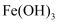 иғ¶дҪ“
иғ¶дҪ“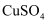 жә¶ж¶ІдёӯеҠ е…ҘдёҖе°Ҹеқ—й’ пјҢз”ҹжҲҗж°”дҪ“е’ҢжІүж·Җ
жә¶ж¶ІдёӯеҠ е…ҘдёҖе°Ҹеқ—й’ пјҢз”ҹжҲҗж°”дҪ“е’ҢжІүж·Җ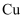
 пјҢеҶҚеҠ е…Ҙ
пјҢеҶҚеҠ е…Ҙ 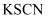 жә¶ж¶ІпјҢжә¶ж¶ІеҸҳзәўиүІ
жә¶ж¶ІпјҢжә¶ж¶ІеҸҳзәўиүІ