2016年江西省宜春市樟树市高考化学一模试卷
2016年江西省宜春市樟树市高考化学一模试卷
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
在某温度下,将H2和I2各1mol的气态混合物充入1L的密闭容器中,发生反应:H2(g)+I2(g)⇌2HI(g)△H<0;5min后达到平衡状态,测得c(H2)=0.9mol•L﹣1 , 则下列结论中,不能成立的是( )
A . 平衡时H2、I2的转化率相等
B . 从反应开始至平衡的过程中,v(HI)=0.04mol•L﹣1•min﹣1
C . 其他条件不变再向容器中充入少量H2 , I2的转化率提高
D . 若将容器温度提高,其平衡常数K一定增大
|
|
| 2. 单选题 | |
|
下列关于蛋白质的叙述不正确的是( )
A . 蛋白质溶液中加入饱和的硫酸铵溶液,蛋白质析出,如再加水能溶解
B . 蛋白质中的蛋白质分子能透过滤纸,但不能透过半透膜
C . 重金属盐能使蛋白质变性,所以吞服“钡餐”会引起中毒
D . 浓硝酸溅在皮肤上,能使皮肤呈黄色是由于蛋白质与浓硝酸发生了颜色反应
|
|
| 3. 单选题 | |
|
门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确.根据元素周期律,下列有关X的性质的描述中正确的是( )
A . X单质易与水反应
B . X形成的氧化物易与水反应生成酸
C . X易形成氧化物XO
D . XH4的稳定性比SiH4的低
|
|
| 4. 单选题 | |
|
对于反应:M+N﹣→P,如果温度每升高10℃,化学反应速率提高到原来的3倍,在10℃时完成反应的10%需要81min,将温度提高到30℃时,完成反应的10%需要的时间为( )
A . 9 min
B . 27 min
C . 13.5 min
D . 3 min
|
|
| 5. 单选题 | |
|
设NA为阿伏加德罗常数的值,下列关于0.2 mol•L﹣1Ba(NO3)2溶液的说法不正确的是( )
A . 1 L溶液中含Ba2+、N
 的总数是0.6NA
B . 500 mL溶液中Ba2+的浓度是0.2 mol•L﹣1
C . 500 mL溶液中N 的总数是0.6NA
B . 500 mL溶液中Ba2+的浓度是0.2 mol•L﹣1
C . 500 mL溶液中N  的浓度是0.2 mol•L﹣1
D . 1 L溶液中含有0.4NA个N 的浓度是0.2 mol•L﹣1
D . 1 L溶液中含有0.4NA个N 
|
|
| 6. 单选题 | |
|
常温下,下列各组离子在指定溶液中一定能大量共存的( )
A . 加入Al能放出H2的溶液中:ClO﹣、HCO
 、SO 、SO  、NH 、NH  B . pH=2的溶液中:Fe2+、Na+、Mg2+、NO
B . pH=2的溶液中:Fe2+、Na+、Mg2+、NO  C . 能使KSCN溶液变红的溶液中:Na+、I﹣、NO
C . 能使KSCN溶液变红的溶液中:Na+、I﹣、NO  、HCO 、HCO  D . 由水电离出的c(OH﹣)=1.0×10﹣13mol•L﹣1的溶液中:Na+、Ba2+、Cl﹣、Br﹣
D . 由水电离出的c(OH﹣)=1.0×10﹣13mol•L﹣1的溶液中:Na+、Ba2+、Cl﹣、Br﹣
|
|
| 7. 单选题 | |
|
某课外活动小组,收集了一种合金进行研究:
①外观暗灰色,表皮光滑. ②在酒精灯上灼烧,火焰绿色;合金片熔化,但不滴落. ③取刮去表皮的金属,放入足量稀硫酸中,收集到标准状况下氢气9.96 L. ④另取刮去表皮的金属,放入足量氢氧化钠溶液中,也收集到标准状况下氢气9.96 L. 试据此判断,合金中含有的成分是( )
A . Cu、Fe
B . K,Na
C . Cu、Al
D . Zn、Mg
|
|
| 8. 单选题 | |
|
由下列实验事实得出的结论正确的是( )
A . 由SiO2不能与水反应生成H2SiO3 , 可知SiO2不是H2SiO3的酸酐
B . 由SiO2+2C
 Si+2CO↑,可知碳的非金属性大于硅
C . CO2通入Na2SiO3溶液产生白色沉淀,可知酸性H2CO3>H2SiO3
D . SiO2可与NaOH溶液反应,也可与氢氟酸反应,可知SiO2为两性氧化物 Si+2CO↑,可知碳的非金属性大于硅
C . CO2通入Na2SiO3溶液产生白色沉淀,可知酸性H2CO3>H2SiO3
D . SiO2可与NaOH溶液反应,也可与氢氟酸反应,可知SiO2为两性氧化物
|
|
| 9. 综合题 | |||||||||
|
现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题:
|
|||||||||
| 10. 实验探究题 | |
|
食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水份、空气中的氧气以及光照、受热而引起的.已知:
氧化性:IO 3I2+6OH﹣═5I﹣+IO
|
|
高中化学 试卷推荐
- 内蒙古自治区呼伦贝尔市阿荣旗第一中学2019-2020学年高二下学期化学期末考试试卷
- 2016-2017学年北京市昌平区临川育人学校高二上学期期末化学试卷
- 人教版化学高二选修5第三章第四节有机合成同步练习
- 广东省华附、省实、广雅、深中2018-2019学年高三上学期理综-化学期末考试试卷
- 专题19:原子结构与性质
- 2016-2017学年广东省清远市清城区高三上学期期末化学试卷(A卷)
- 2016-2017学年江苏省宿迁市沭阳县高一上学期期中化学试卷
- 湖南省益阳市桃江县2019-2020学年高二下学期化学期末考试试卷
- 山东省德州市2020年高考化学一模试卷
- 2020高考化学常考知识点专练 09:物质结构与性质
- 河北省2020年高考理综-化学一模试卷(全国Ⅰ卷)
- 浙江省金华十校2019-2020学年高一下学期化学期末考试试卷
最近更新

 >Fe3+>I2;还原性:S2O
>Fe3+>I2;还原性:S2O 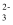 >I﹣
>I﹣


