2016-2017学年黑龙江省双鸭山市友谊县红兴隆管理局一中高三上学期期中化学试卷
2016-2017学年黑龙江省双鸭山市友谊县红兴隆管理局一中高三上学期期中化学试卷
教材版本:化学
试卷分类:化学高三上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高三上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
已知:2Zn(s)+O2(g)=2ZnO(s);△H=﹣701.0kJ•mol﹣1
2Hg(l)+O2(g)=2HgO(s);△H=﹣181.6kJ•mol﹣1 则反应Zn(s)+HgO(s)=ZnO(s)+Hg(l)的△H为( )
A . +519.4kJ•mol﹣1
B . +259.7 kJ•mol﹣1
C . ﹣259.7kJ•mol﹣1
D . ﹣519.4kJ•mol﹣1
|
|
| 2. 单选题 | |
|
提出元素周期律并根据元素周期律编制第一个元素周期表的科学家是( )
A . 道尔顿
B . 普利斯特里
C . 门捷列夫
D . 阿伏加德罗
|
|
| 3. 单选题 | |
|
化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
A . 电解NaCl饱和溶液,可制得金属钠
B . 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
C . 寻找高效催化剂,利用太阳能分解水是制取氢气的较理想方法
D . MgO的熔点很高,可用于制作耐高温材料
|
|
| 4. 单选题 | |
|
一定条件下,X(g)+3Y(g)⇌2Z(g)达到化学平衡的标志是( )
A . Z的分解速率和Y的生成速率相等
B . 单位时间内生成nmolZ,同时生成nmolX
C . 反应体系的总质量保持不变
D . X,Y,Z的浓度不再变化
|
|
| 5. 单选题 | |
|
铜锌原电池(如图)工作时,下列叙述不正确的是( )
A . 负极反应为:Zn﹣2e﹣═Zn2+
B . 电池反应为:Zn+Cu2+═Zn2++Cu
C . 在外电路中,电子从负极流向正极
D . 盐桥中的K+移向ZnSO4溶液
|
|
| 6. 单选题 | |
|
NA表示阿伏加德罗常数的值,下列说法正确的是( )
A . 标准状况下,22.4L二氯甲烷的分子数约为NA个
B . 盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5mol
C . 17.6g丙烷中所含的极性共价键为NA
D . 电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少 64g
|
|
| 7. 单选题 | |
|
已知4NH3+5O2═4NO+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
A .
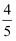 v(NH3)=v(O2)
B . v(NH3)=v(O2)
B . 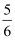 v(O2)=v(H2O)
C . v(O2)=v(H2O)
C . 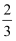 v(NH3)=v(H2O)
D . v(NH3)=v(H2O)
D . 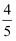 v(O2)=v(NO) v(O2)=v(NO)
|
|
| 8. 单选题 | |
|
下列各组离子可能大量共存的是( )
A . 在含大量Fe3+的溶液中:NH4+、Na+、Cl﹣、SCN﹣
B . 在含有Al3+、Cl﹣的溶液中:HCO3﹣、I﹣、NH4+、Mg2+
C . 在c(H+)=1×10﹣13 mol•L﹣1的溶液中:Na+、S2﹣、SO32﹣、NO3﹣
D . 在溶质为KNO3和NaHSO4的溶液中:Fe2+、Ca2+、Al3+、Cl﹣
|
|
| 9. 单选题 | |
|
向一体积为2L的恒容密闭容 器里充入1mol N2和3mol H2 , 在一定温度下发生反应:N2(g)+3H2(g)⇌2NH3(g);△H<0.10秒时达到平衡,c(NH3)为0.4mol/L.下列说法正确的是( )
A . 向该容器中充入N2 , 平衡正向移动
B . 降低温度能使混合气体的密度增大
C . 该反应达平衡时H2的转化率为20%
D . 研发高效催化剂可大大提高N2的转化率
|
|
| 10. 单选题 | |
|
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)⇌2SO3(g)△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的( )
A . 图Ⅰ研究的是t0时刻增大O2的物质的量浓度对反应速率的影响
B . 图Ⅱ研究的是t0时刻通入氦气增大体系压强对反应速率的影响
C . 图Ⅲ研究的是催化剂对化学平衡的影响,且甲的催化效率比乙高
D . 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高
|
|
高中化学 试卷推荐
- 新疆伊宁生产建设兵团五校联考2017-2018学年高二下学期化学期末考试试卷
- 广东省茂名市五校联盟2019-2020学年高二下学期化学期末考试试卷
- 上海大学附属中学2018-2019学年高二下学期化学期中考试试卷
- 安徽省合肥市巢湖市无为中学2017-2018学年高二上学期化学开学考试试卷
- 江西省四校协作体2017-2018学年高二上学期化学期中考试试卷
- 安徽省淮北市濉溪中学等三校联考2017-2018学年高二上学期化学期中考试试卷
- 陕西省安康市2019-2020学年高一下学期化学期末考试试卷
- 浙江省书生中学2019-2020学年高二上学期化学第一次月考试卷
- 2016-2017学年辽宁省大连渤海高中高三上学期期中化学试卷
- 湖北省武汉市华中师大一附中2016-2017学年高一上学期化学期中考试试卷
- 江西省鹰潭市2019-2020学年高一下学期化学期末考试试卷
- 上海市浦东新区2016-2017学年高一上学期化学期末考试试卷
最近更新





