黑龙江省齐齐哈尔市2017-2018学年高考理综-化学一模考试试卷
黑龙江省齐齐哈尔市2017-2018学年高考理综-化学一模考试试卷
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-04-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
化学知识在生产和生活中有着重要的应用。下列说法正确的是( )
A . 危化品仓库中的金属钠、钾着火时,可用水扑灭
B . 自来水厂常用明矾作为天然水的消毒剂
C . 纯碱在医疗上是治疗胃酸过多的一种药剂
D . 氧化铝可用来制造耐高温的实验仪器
|
|
| 2. 单选题 | |
|
NA为阿伏加德罗常数的值。下列说法错误的是( )
A . 100g质量分数为46%的乙醇水溶液中,含有4NA个氧原子
B . 1mol Cl2溶于水,溶液中Cl-、HClO、ClO- 粒子数之和小于2NA
C . 2.24 L(标准状况)2H2中含有0.2NA个中子
D . 25℃时Ksp(CaSO4)=9×10-6 , 则该温度下CaSO4饱和溶液中含有3×10-3NA个Ca2+
|
|
| 3. 单选题 | |
|
短周期主族元素W、X、Y、Z的原子序数依次增大,W的某种单质是自然界中最硬的物质,X的某种单质是生物呼吸必需的气体,Y是活泼的金属元素,Z元素原子的K层和M层电子数相同。下列说法正确的是( )
A . X、Y、Z的简单离子半径由大到小的顺序是Y>Z>X
B . 含有Y的盐溶液可能呈酸性、碱性或中性
C . W的简单氢化物的热稳定性比X的强
D . WX2跟X、Y形成的化合物发生的反应都不是氧化还原反应
|
|
| 4. 单选题 | |
|
下列关于有机化合物的说法正确的是( )
A . 环己烷的二氯代物和十氯代物均只有4种
B . 油脂在水解过程中发生了加成反应
C . 蔗糖是葡萄糖的同系物
D . 溴水可用来区分乙醇、乙酸、苯
|
|
| 5. 单选题 | |
|
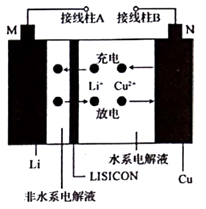
一种Cu- Li可充电电池的工作原理如图所示,其中非水系电解液和水系电解液被锂离子固体电解质陶瓷片( LISICON)隔开。下列说法正确的是( )
A . 陶瓷片允许水分子通过
B . 电池充电时,阴极反应为Li++e-=Li
C . 电池放电时,N极发生氧化反应
D . 电池充电时,接线柱B应与外接直流电源的负极相连
|
|
| 6. 单选题 | |||||||||||||||||||||
|
下列实验中,对应的现象以及结论都正确但两者不具有因果关系的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 7. 单选题 | |
|
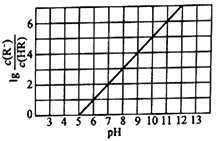
常温下,向1L0.1mol·L-1一元酸HR溶液中逐渐通入氨气[已知常温下Kb(NH3·H2O)=1.76×10-5],使溶液温度和体积保持不变,混合溶液的pH与离子浓度变化的关系如下图所示。下列叙述正确的是( )
A . 0.1mol·L-1HR溶液的pH约为5
B . HR为弱酸,常温时Ka(HR)=1.0×10-7
C . 当通入0.1molNH3时,溶液中c(R-)<c(NH4+)
D . 当c(HR)=c(R-)时,溶液呈中性
|
|
| 8. 综合题 | |
|
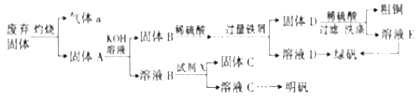
工业上用废弃固体(含有Cu2S、Al2O3、Fe2O3、SiO2 等)制取粗铜、绿矾(FeSO4·7H2O)和明矾[KAl(SO4)2·12H2O],操作流程如下:
|
|
| 9. 综合题 | |
|
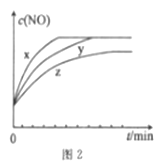
为有效提升空气质量,国家强制各燃煤企业要对燃媒烟气进行脱硫、脱硝处理后排放。回答下列问题:
|
|
| 10. 综合题 | |
|
铜、银、金与社会生活联系密切。
|
|
高中化学 试卷推荐
- 吉林省长春市北京师范大学长春附属学校2020-2021学年高二下学期化学第一次月考试卷
- 山西太原市2021-2022学年高一下学期期中测试化学试题
- 四川省泸州市2021-2022学年高二上学期期末统考化学试题
- 广东省佛山顺德市2021-2022学年高三第一次模拟化学试题
- 山东省济宁邹城市2021-2022学年高一下学期期中考试化学试题
- 浙江省长兴县华盛高级中学2020-2021学年高一下学期化学5月月考试卷
- 河北省保定市2021年高考化学一模试卷
- 山东省日照市五莲县2020-2021学年高一上学期化学期中考试试卷
- 安徽省蚌埠市2020-2021学年高三上学期化学第一次月考试卷(一模)
- 北京市石景山区2020-2021学年高一上学期期末调研化学试卷题
- 河北省唐山市2022届高三第三次模拟考试化学试题
- 北京市西城区2021届高三上学期期末考试化学试题
最近更新
 5N2(g)+6H2O(g)△H1
5N2(g)+6H2O(g)△H1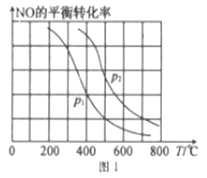
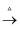 CH3COONH4+2Ag↓+3NH3+H2O。1个CH3CHO分子中所含π键的数目为,碳原子的杂化轨道类型为;CH3 CH2OH、CH3CHO的相对分子质量仅相差2,但沸点相差很大(分别为78.5℃,20.8℃),其主要原因是;NH3的VSEPR模型为。
CH3COONH4+2Ag↓+3NH3+H2O。1个CH3CHO分子中所含π键的数目为,碳原子的杂化轨道类型为;CH3 CH2OH、CH3CHO的相对分子质量仅相差2,但沸点相差很大(分别为78.5℃,20.8℃),其主要原因是;NH3的VSEPR模型为。



