人教高中化学一轮复习:专题8
人教高中化学一轮复习:专题8
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 填空题 | |
|
有下列七种物质:A、干冰 B、氧化镁 C、氯化铵 D、固态碘 E、烧碱 F、冰 G、过氧化钾
|
|
| 2. 填空题 | |||||||||||||||||||||||||||||||||||||||||
|
下表是中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题。
|
|||||||||||||||||||||||||||||||||||||||||
| 3. 填空题 | |
|
下列五种物质中 ①Ne ②H2O
③NH3 ④KOH ⑤Na2O(填写序号):只存在共价键的是 ,只存在离子键的是 ,既存在共价键又存在离子键的是 ,不存在化学键的是。
|
|
| 4. 填空题 | |
|
下列物质中:①MgCl2②金刚石③NaCl④H2O⑤Na2O2⑥O2⑦H2SO4⑧CO2⑨NH4Cl⑩Ne。只含离子键的是,只含共价键的是,既含离子键又含共价键的是,不存在化学键的是,属于离子化合物的是,属于共价化合物的是。
|
|
| 5. 实验探究题 | |||||
|
研究发现,NO在心脑血管调节、免疫调节等方面有着十分重要的作用,但NO无法直接作为药物使用。科学家发现NO
 有着与NO相似的功效,可以用作药物。某研究小组对亚硝酸盐转化为NO的反应进行了研究。 有着与NO相似的功效,可以用作药物。某研究小组对亚硝酸盐转化为NO的反应进行了研究。
|
|||||
| 6. 多选题 | |||||||||||||||||||||||||||
|
利用如图所示装置进行实验,能达到相应实验目的的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||||||||
| 7. 多选题 | |
|
短周期主族元素X、Y、Z、W原子序数依次增大,X与Z可以形成两种常见液态化合物,W的原子半径在矩周期主族元素中最大,由Y、Z、W三种元素形成的化合物A的结构如图所示。下列叙述错误的是( )
A . Y的氢化物沸点一定低于Z的氢化物
B . X与Z可能形成由极性键与非极性键构成的极性分子
C . 化合物
 可以与乙二醇在一定条件下发生缩聚反应
D . 0.1 可以与乙二醇在一定条件下发生缩聚反应
D . 0.1  化合物A与足量酸性高锰酸钾溶液完全反应转移电子数是0.1 化合物A与足量酸性高锰酸钾溶液完全反应转移电子数是0.1 
|
|
| 8. 多选题 | |
|
短周期元素X、Y、Z、R的原子序数依次增大,离子化合物YR可用于调味和食品保存,X、Y、Z三种元素组成的两种化合物A、B的性质如图,X的基态原子中s能级与p能级上的电子数相等。下列说法正确的是( )
A . X与Z形成的三原子分子为直线形分子
B . 简单离子半径:Y<R<Z
C . X、Z、R的氢化物的分子间均能形成氢键
D . X、Y、Z、R中,Y的第一电离能最小
|
|
| 9. 多选题 | ||||||||||||||||
|
下列操作能达到实验目的的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 10. 多选题 | |
|
短周期主族元素
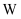 、 、 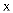 、 、 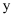 、 、 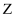 的原子序数依次增大, 的原子序数依次增大, 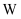 的阴离子与锂离子具有相同的电子层结构, 的阴离子与锂离子具有相同的电子层结构, 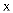 的一种核素常用于考古断代, 的一种核素常用于考古断代, 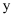 原子的最外层电子数是内层电子数的3倍, 原子的最外层电子数是内层电子数的3倍, 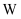 、 、 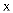 、 、 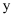 原子的最外层电子数总和等于 原子的最外层电子数总和等于 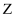 的原子序数。下列推断错误的是( ) 的原子序数。下列推断错误的是( )
A . 原子半径:
 B . 化合物
B . 化合物  中既含离子键又含共价键
C . 最简单气态氢化物的稳定性: 中既含离子键又含共价键
C . 最简单气态氢化物的稳定性:  D . 由上述四种元素组成的化合物的水溶液不可能呈碱性
D . 由上述四种元素组成的化合物的水溶液不可能呈碱性
|
|
高中化学 试卷推荐
- 2016年江西省宜春市万载二中高考化学三模试卷
- 安微省黄山市2018-2019学年高考理综-化学二模考试试卷
- 2015-2016学年江苏省无锡市江阴市四校联考高二下学期期中化学试卷
- 2015-2016学年江西省上饶市四校高一上学期第三次联考化学试卷
- 江西省四校协作体2017-2018学年高一上学期化学期中考试试卷
- 人教版化学高二选修3第二章第三节分子的性质同步练习
- 高中化学人教版(2019)必修第一册 第三章测试卷
- 专题5:氯及其化合物、卤素
- 广东省揭阳市2017-2018学年高三理综-化学第一次模拟考试试卷
- 2015年四川省成都市崇州市崇庆中学高考化学“一诊”模拟试卷(四)
- 2015年吉林省长春市高考化学模拟试卷(四)
- 河南省平顶山市、许昌市、汝州2017-2018学年高二上学期化学期中考试试卷
最近更新




 生成
生成 或
或 
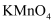
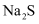 溶液
溶液 悬浊液
悬浊液 与
与 





