辽宁省抚顺市2020-2021学年高二上学期化学期中考试试卷
辽宁省抚顺市2020-2021学年高二上学期化学期中考试试卷
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
下列叙述不能证明乙酸是弱电解质的是( )
A . 常温时0.1mol/L乙酸溶液的pH=3
B . 常温时0.1mol/L的乙酸钠溶液能使红色石蕊试纸变蓝
C . 0.1mol/L的乙酸溶液与同体积0.1mol/L的氢氧化钠溶液恰好反应
D . 0.1mol/L乙酸溶液的导电性比0.1mol/L盐酸弱
|
|
| 2. 单选题 | |
|
下列说法或表示方法中正确的是( )
A . H2O(g)变成H2O(l)的过程中,断键吸收的能量小于成键放出的能量
B . 由C(金刚石)=C(石墨)△H=-1.9kJ▪mol-1可知,金刚石比石墨稳定
C . 在101 KPa时,2 g H2完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l) △H=-285.8kJ▪mol-1
D . 在稀溶液中:H+(aq)+OH-(aq)= H2O(l) △H=-57.3kJ▪mol-1 , 若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量大于57.3kJ
|
|
| 3. 单选题 | |
|
下列指定化学用语正确的是( )
A . NaHCO3水解的离子方程式:HCO3-+H2O = CO32-+H3O+
B . Ba(OH)2的电离方程式:Ba(OH)2
 Ba2++2OH-
C . NaHSO4在水中的电离方程式:NaHSO4= Na++H++SO42-
D . Na2S水解的离子方程式:S2-+2H2O = H2S+2OH- Ba2++2OH-
C . NaHSO4在水中的电离方程式:NaHSO4= Na++H++SO42-
D . Na2S水解的离子方程式:S2-+2H2O = H2S+2OH-
|
|
| 4. 单选题 | |
|
如图表示的是某离子X的水解过程示意图,则离子X可能是( )
A . CO
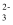 B . HCO
B . HCO  C . Na+
D . NH
C . Na+
D . NH |
|
| 5. 单选题 | |
|
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
A . 0.1mol/LCH3COONa溶液与0.1mol/L HCl溶液等体积混合:c(Na+)>c(Cl-)>c(CH3COO-)>c(OH-)
B . 0.1mol/L NH4Cl溶液与0.1mol/L氨水等体积混合(pH>7):c(NH3.H2O)>c(
 )>c(Cl-)>c(OH-)
C . 0.1mol/L Na2CO3与0.1mol/LNaHCO3溶液等体积混合:2c(Na+)=3c( )>c(Cl-)>c(OH-)
C . 0.1mol/L Na2CO3与0.1mol/LNaHCO3溶液等体积混合:2c(Na+)=3c( 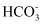 )+3c( )+3c( 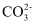 )+3c(H2CO3)
D . 0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) )+3c(H2CO3)
D . 0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH)
|
|
| 6. 单选题 | |
|
室温时,下列说法正确的是( )
A . pH=11的氨水和pH=11的Na2CO3溶液中,由水电离产生的c(OH-)均为1×10−11 mol·L−1
B . 分别把100 mL pH=11的NaOH溶液和pH=11的氨水加水稀释至1 L,所得溶液pH均为10
C . 分别向等体积的0.1 mol·L−1 HCl溶液和0.1 mol·L−1 CH3COOH溶液中加入等浓度的NaOH溶液,恰好为中性时,消耗NaOH溶液的体积相等
D . 分别向1 mL pH=3的盐酸和pH=3的CH3COOH溶液中加入少量CH3COONa固体,两溶液的pH均增大
|
|
| 7. 单选题 | |
|
蒸干并灼烧下列物质的水溶液,仍能得到该物质的是( )
A . 氯化铝
B . 碳酸氢钠
C . 硫酸亚铁
D . 碳酸钠
|
|
| 8. 单选题 | |
|
下列有关仪器的使用方法或实验操作正确的是( )
A . 洗净的锥形瓶和容量瓶可以放进烘箱中烘干
B . 用容量瓶配溶液时,若加水超过刻度线,立即用滴定管吸出多余液体
C . 测定新制氯水的pH,用玻璃棒取液体滴在pH试纸上,再对照标准比色卡读数
D . 酸碱中和滴定时,滴定管使用前需用待装液润洗而锥形瓶不用
|
|
| 9. 单选题 | |||||||||||||||||||||
|
下表所示实验,现象和结论均正确的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 10. 单选题 | ||||||||||||||||
|
常温下浓度均为0.1mol/L 的四种盐溶液,其pH 如表所示,下列说法正确的是( )
A . 等浓度的CH3COOH 和HClO溶液,pH小的是HClO
B . Na2CO3和NaHCO3溶液中粒子种类不同
C . 溶液水的电离程度:①>②>④>③
D . NaHCO3溶液中:c (Na+) =c (CO32- )+c (HCO3- )+c (H2CO3)
|
||||||||||||||||
高中化学 试卷推荐
- 浙江省诸暨市2021年高考化学5月模拟试卷
- 山西省临汾市2022届高三下学期考前适应性训练考试(三)理科综合化学试题
- 辽宁省六校2020-2021学年高一上学期化学期中考试试卷
- 江苏高邮市2021-2022学年高一下学期期中考试化学试题
- 吉林省吉林市第二中2020-2021学年高一上学期化学9月月考试卷
- 广东省普宁市2020-2021学年高一下学期化学期中考试试卷
- 湖北省黄冈市2020-2021学年高一下学期化学期末考试试卷
- 广东省汕尾市海丰县2020-2021学年高一下学期化学期中考试试卷
- 广东省广州市2022届高三一模考试化学试题
- 广东省湛江市2021-2022学年高一上学期期中考试化学试题
- 江苏省盐城市2021年高考化学三模试卷
- 广东省茂名市2022届高三第二次综合测试(二模)化学试题
最近更新





