2016年山东省菏泽市成武一中高考化学三模试卷
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
化学与生活密切相关,下列叙述正确的是( )
A . 光纤通信使用的光缆主要成分是Si,太阳能电池使用的材料主要是SiO2
B . 点燃爆竹后,硫燃烧生产SO3
C . 海水中含有溴元素,只进行物理变化就可以得到溴单质
D . “地沟油”禁止使用,但可以用来制取肥皂
|
|
| 2. 单选题 | |
|
NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A . 标准状况下2.24L氯气与水充分反应转移电子数为0.1NA
B . 标况下,2.24LNO2分子总数小于0.1NA
C . 标准状况下2.24L的CCl4中含有的C﹣Cl键数为0.4NA
D . 6.8g液态KHSO4中含有0.1NA个阳离子
|
|
| 3. 单选题 | |
|
X、Y、Z、W为四种短周期主族元素,且原子序数依次递增,其中X、Z同族,Y是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,下列说法正确的是( )
A . Y、Z、W单核离子均能破坏水的电离平衡
B . W元素氧化物对应水化物的酸性一定强于Z
C . 南X、Y、Z三种元素组成的化合物不止2种
D . 因为X的氢化物分子间有氢键,所以X的氢化物较Z的氢化物稳定
|
|
| 4. 单选题 | |
|
已知电离平衡常数:H2CO3>HClO>HCO
 .下列离子反应方程式正确的是( ) .下列离子反应方程式正确的是( ) ①NaClO溶液中通入少量二氧化碳:2ClO﹣+CO2+H2O═2HClO+CO ②Na2CO3溶液中加入HClO溶液:CO ③等物质的量的Cl2与Na2CO3溶液恰好反应:Cl2+CO ④Cl2通入NaHCO3溶液中:Cl2+2HCO
A . ②④
B . ①③
C . ②③
D . ①④
|
|
| 5. 单选题 | |||||||||||||||||||||
|
向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 6. 单选题 | |
|
下列溶液中微粒浓度关系正确的是( )
A . 含有NH
 、Cl﹣、H+、OH﹣的溶液中,离子浓度是c(Cl﹣)>c(NH 、Cl﹣、H+、OH﹣的溶液中,离子浓度是c(Cl﹣)>c(NH  )>c(OH﹣)>c(H+)
B . pH=5的NH4Cl溶液与pH=5的硫酸中,水电离的c(H+)相同
C . pH=9的NaHCO3溶液中:c(Na+)>c(HCO )>c(OH﹣)>c(H+)
B . pH=5的NH4Cl溶液与pH=5的硫酸中,水电离的c(H+)相同
C . pH=9的NaHCO3溶液中:c(Na+)>c(HCO  )>c(CO )>c(CO  )>c(H2CO3)
D . 将0.2 mol•L﹣1 CH3COOH溶液和0.1 mol•L﹣1NaOH溶液等体积混合,则反应后的混合溶液中:2c(OH﹣)+c(CH3COO﹣)=2c(H+)+c(CH3COOH) )>c(H2CO3)
D . 将0.2 mol•L﹣1 CH3COOH溶液和0.1 mol•L﹣1NaOH溶液等体积混合,则反应后的混合溶液中:2c(OH﹣)+c(CH3COO﹣)=2c(H+)+c(CH3COOH)
|
|
| 7. 实验探究题 | |
|
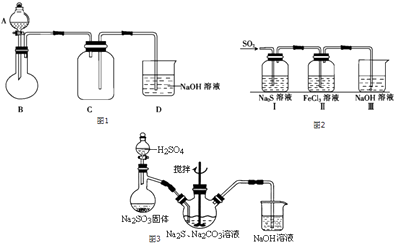
二氧化硫为无色气体,有强烈刺激性气味,是大气主要污染物之一.某化学兴趣小组欲制备并探究SO2的某些性质.
【SO2的制备】用亚硫酸钠与较浓的硫酸反应制备SO2的装置图如图1(夹持仪器省略):
|
|
| 8. 综合题 | |||||||||||||||
|
NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,根据题意回答下列问题:
Ⅰ.利用催化技术将尾气中的NO和CO转变成CO2和N2 , 化学方程式如下: 2NO(g)+2CO(g) 为了测定某催化剂作用下的反应速率,在一定温度下,向某恒容密闭容器中充入等物质的量的NO和CO发生上述反应.用气体传感器测得不同时间NO浓度如表:
|
|||||||||||||||
| 9. 综合题 | ||||||||||||||||||||||||||
|
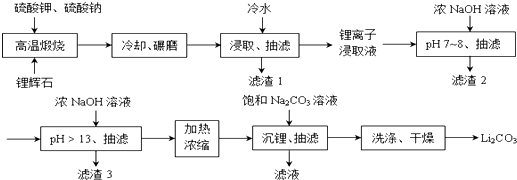
锂元素被誉为“能源元素”.锂及锂盐具有的优异性能和特殊功能,在化工、电子、宇航、核能、能源等领域都得到广泛应用.
|
||||||||||||||||||||||||||
| 10. 实验探究题 | |
|
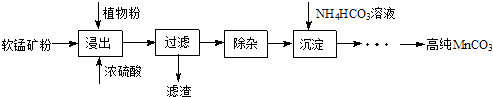
高纯碳酸锰在电子工业中有重要的应用,湿法浸出软锰矿(主要成分为MnO2 , 含少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的实验过程如下:
|
|
- 陕西省西安市莲湖区2019-2020学年高一下学期化学期末考试试卷
- 上海中学2016-2017学年高一上学期化学期末考试试卷
- 2017年天津市南开区高考化学模拟试卷
- 浙江省慈溪市六校2018-2019学年高二上学期化学期中考试试卷
- 2018年4月浙江省普通高校招生选考科目考试化学试卷
- 2015-2016学年山东省枣庄市滕州十一中高三上学期期末化学模拟试卷(三)
- 安徽省皖南八校2019-2020学年高三上学期化学第二次月考试卷
- 2015-2016学年湖北省武汉市华中师大一附中高三上学期期中化学试卷
- 人教高中化学一轮复习:专题5 金属Na、Fe以及其化合物
- 陕西省榆林市第二中学2018-2019学年高二下学期化学期中考试试卷
- 2018年高考理综化学真题试卷(全国Ⅲ卷)
- 天津市红桥区2017-2018学年高一上学期化学期末考试试卷

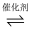 2CO2(g)+N2(g)△H=﹣748kJ/mol
2CO2(g)+N2(g)△H=﹣748kJ/mol