江苏省南京市盐城市2021年高考化学一模试卷
江苏省南京市盐城市2021年高考化学一模试卷
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
大国重器彰显中国实力,化学材料助力科技成果转化运用。下列说法正确的是( )
A . “蛟龙号”载人潜水器使用的钛合金是金属材料
B . “C919”大飞机使用的氮化硅陶瓷是传统硅酸盐材料
C . “玉兔二号”月球车使用的太阳能电池板材料是二氧化硅
D . “山东舰”航母使用的碳纤维是一种新型有机高分子材料
|
|
| 2. 单选题 | |
|
侯氏制碱法主要反应原理:NH3+NaCl+CO2+H2O=NaHCO3↓+NH4Cl。下列有关说法错误的是( )
A . CO2空间构型为直线形
B . NaCl固体为离子晶体
C . Na的原子结构示意图为
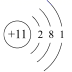 D . NH4Cl的电子式为
D . NH4Cl的电子式为 
|
|
| 3. 单选题 | |
|
下列有关物质的性质与用途具有对应关系的是( )
A . 氢氟酸显弱酸性,可用于雕刻玻璃
B . Na2CO3溶液呈碱性,可用于去除油污
C . Al2O3熔点高,可用作电解冶炼铝的原料
D . S2-具有还原性,可用于去除水体中Pb2+等重金属离子
|
|
| 4. 单选题 | |
|
下列有关二氧化硫的说法正确的是( )
A . SO2属于电解质
B . SO2为非极性分子
C . SO2既有氧化性又有还原性
D . SO2易溶于水是因为与水能形成分子间氢键
|
|
| 5. 单选题 | |
|
实验室制取SO2时,下列装置不能达到相应实验目的的是( )
A . 图1:生成SO2
B . 图2:检验SO2
C . 图3:干燥SO2
D . 图4:收集SO2
|
|
| 6. 单选题 | |
|
蓝天保卫战—持续三年的大气治理之战,其中低成本、高效率处理SO2、NO2等大气污染物一直是化学研究的重点课题,研究它们的性质、制备在工业生产和环境保护中有着重要意义。一种处理SO2、NO2的研究成果,其反应原理为( )SO2(g)+NO2(g)=SO3(g)+NO(g) ΔH1=-41.8kJ·mol-1 , 标准状况下,SO2(g)+NO2(g)=SO3(s)+NO(g) ΔH2.下列有关说法错误的是
A . 该反应的ΔS>0
B . ΔH2<-41.8kJ·mol-1
C . SO2的生成速率和NO2的消耗速率相等说明该反应达到平衡状态
D . 标准状况下,该反应中每生成22.4L NO转移电子的数目约等于2×6.02×1023
|
|
| 7. 单选题 | |
|
如图为元素周期表中短周期的一部分,下列说法错误的是( )
A . 离子半径:M->Z2->Y-
B . 电负性:Y>M>Z
C . 简单气态氢化物的稳定性:Y>M>Z
D . Y元素基态原子的简化电子排布式:[X]2s22p5
|
|
| 8. 单选题 | |
|
用久置于空气中的生石灰[主要成分为CaO,还含有Ca(OH)2和CaCO3]制取KClO3的流程如下。下列有关说法错误的是( )
A . “打浆”的目的是为了提高“氯化”时的反应速率
B . “氯化”中主要发生的化学反应为6Cl2+6Ca(OH)2
 Ca(ClO3)2+5CaCl2+6H2O
C . “过滤”后滤液中存在的阳离子有Ca2+、H+
D . “转化”时发生的化学反应属于氧化还原反应 Ca(ClO3)2+5CaCl2+6H2O
C . “过滤”后滤液中存在的阳离子有Ca2+、H+
D . “转化”时发生的化学反应属于氧化还原反应
|
|
| 9. 单选题 | |
|
对固体电解质体系的研究是电化学研究的重要领域之一、用离子交换膜H+/
 型 Nafion膜作电解质,在一定条件下实现了常温常压下电化学合成氨,原理如下图所示。下列说法错误的是( ) 型 Nafion膜作电解质,在一定条件下实现了常温常压下电化学合成氨,原理如下图所示。下列说法错误的是( )
A . 电极M接电源的正极
B . 离子交换膜中H+、
 浓度均保持不变
C . H+/ 浓度均保持不变
C . H+/  型离子交换膜具有较高的传导质子能力
D . 阴极的电极反应式:N2+6e-+6H+=2NH3 , 2H++2e-=H2↑ 型离子交换膜具有较高的传导质子能力
D . 阴极的电极反应式:N2+6e-+6H+=2NH3 , 2H++2e-=H2↑
|
|
| 10. 单选题 | |
|
乙醛与新制氢氧化铜悬浊液反应的实验如下:
步骤1:向试管中加入2mL10%NaOH溶液,边振荡边滴加4~6滴2%CuSO4溶液,观察到有蓝色絮状沉淀产生。 步骤2:再向试管中加入0.5mL乙醛溶液,加热,观察到有红色沉淀产生。 下列说法错误的是( )
A . 步骤1中必须加入过量的NaOH溶液
B . 步骤2中观察到的红色沉淀为Cu2O
C . 上述实验说明乙醛能被新制氢氧化铜氧化
D . 上图所示Cu2O的晶胞中
|
|
高中化学 试卷推荐
- 2016-2017学年山东省德州市夏津一中高一下学期期中化学试卷
- 2015-2016学年四川省达州市铁路中学高一下学期期中化学试卷
- 第31讲:化学实验基础知识
- 浙江省温州市十五校联合体2017-2018学年高一下学期化学期中考试试卷
- 高中化学人教版(2019)选择性必修1 第三章第三节 盐类的水解
- 2017年湖北省重点高中协作校高考化学模拟试卷
- 陕西省渭南韩城市2019-2020学年高二上学期化学期中考试试卷
- 湖南省衡阳市2016-2017学年高二上学期化学期末考试试卷
- 吉林省榆树一中2017-2018学年高一上学期化学期中考试试卷
- 2015-2016学年安徽省六安市舒城县晓天中学高一下学期第一次月考化学试卷
- 2017_2018学年高中化学人教版选修四 第四章电化学基础4.1原电池b
- 专题14:化学反应速率与化学平衡
最近更新








