2016年江西省萍乡市上栗县高考化学四模试卷
2016年江西省萍乡市上栗县高考化学四模试卷
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
为验证无还原性的蔗糖能水解,且水解的生成物具有还原性,可能有如下实验步骤:①加入稀硫酸;②加入几滴CuSO4;③加热;④加入蒸馏水;⑤加入烧碱溶液至碱性;⑥加入新制Cu(OH)2悬浊液,最佳顺序( )
A . ④①③⑥③
B . ④③①⑥⑤③
C . ①③②⑥③
D . ④①③⑤⑥③
|
|
| 2. 单选题 | |
|
amol H2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为( )
A . (
 )mol﹣1
B . ( )mol﹣1
B . ( )mol﹣1
C . ( )mol﹣1
C . ( )mol﹣1
D . ( )mol﹣1
D . (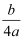 )mol﹣1 )mol﹣1
|
|
| 3. 单选题 | |
|
如表是某矿物质饮用水的部分标签说明主要成分
钾离子(K+)20~27.3mg•L﹣1 氯离子(Cl﹣)30~34.2mg•L﹣1 镁离子(Mg2+)20.2~24.9mg•L﹣1 硫酸根离子(SO42﹣)24~27.5mg•L﹣1 则该饮用水中还可能较大量存在( )
A . OH﹣
B . Ag+
C . Na+
D . Ca2+
|
|
| 4. 单选题 | |
|
硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发展水平的一种标志.目前的重要生产方法是“接触法”,有关接触氧化反应2SO2+O2
 2SO3 , 的说法不正确的是( ) 2SO3 , 的说法不正确的是( )
A . 该反应为可逆反应,故在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫
B . 达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零
C . 一定条件下,向某密闭容器中加入2molSO2和1molO2 , 则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等
D . 在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
|
|
| 5. 单选题 | |
|
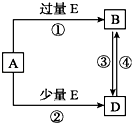
已知A、B、D、E 均为中学化学常见物质,它们之间的转化关系如图所示(部分产物略去,①②③④的反应条件相同).则A、E 可能的组合为( )
①CO2、NaOH 溶液 ②NaCl溶液、Ca(OH)2 溶液③Fe、稀HNO3 ④Na、O2 ⑤CuO,C ⑥AlCl3 溶液、NH3•H2O.
A . ②③④⑤
B . ①③④⑤⑥
C . ①②③⑤⑥
D . ①③⑤
|
|
| 6. 单选题 | |
|
下列反应中,说明氨有还原性和碱性的是( )
A . 2NH3+3CuO
 3Cu+N2↑+3H2O
B . 8NH3+3Cl2═6NH4Cl+N2
C . 4NH3+6NO 3Cu+N2↑+3H2O
B . 8NH3+3Cl2═6NH4Cl+N2
C . 4NH3+6NO  5N2+6H2O
D . NH3+HCl═NH4Cl 5N2+6H2O
D . NH3+HCl═NH4Cl
|
|
| 7. 单选题 | |
|
某种碳酸饮料中主要含柠檬酸、碳酸、白砂糖、苯甲酸钠等成分,常温下测得其pH约为3.5,下列说法不正确的是( )
A . 柠檬酸的电离会抑制碳酸的电离
B . 该碳酸饮料中水的电离受到抑制
C . 常温下,该碳酸饮料中KW的值大于纯水中KW的值
D . 打开瓶盖冒出大量气泡,是因为压强减小,降低了CO2的溶解度
|
|
| 8. 单选题 | |
|
有关下列两套装置的描述不正确的是( )
A . 甲装置为铁的析氢腐蚀,若将铁换成铜,则甲装置就是铜的吸氧腐蚀
B . 若将甲装置中的电流表改为电源,无论电源怎么连接,C电极上都会有气体放出
C . 乙装置中K关闭后,a极附近颜色逐渐加深变黑
D . 若将乙装置中的NaOH溶液换为HCl溶液,则K关闭后b极颜色变浅
|
|
| 9. 综合题 | |
|
周期表前20号元素中有A、B、C、D、E五种不同主族元素.已知它们原子半径依次增大,其中A与D、C与E原子的电子层数都相差2,且D与E原子的最外层电子数之比为2:1,C与E能形成离子化合物EC.
|
|
| 10. 推断题 | |
|
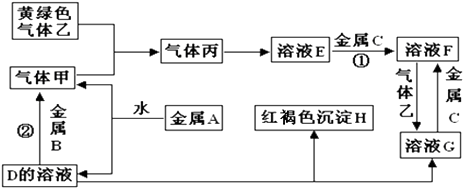
有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属.三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有全部标出).
请根据以上信息回答下列问题:
|
|
高中化学 试卷推荐
- 2016-2017学年吉林省辽源市普通高中高一上学期期中化学试卷
- 吉林省白城市通榆县第一中学2019-2020学年高三上学期化学第一次月考试卷
- 2015-2016学年山东省聊城市临清二中高三上学期开学化学试卷
- 2015-2016学年湖南省长沙市望城区高二上学期期末化学试卷(理科)
- 广东省东莞市2017-2018学年高三上学期理综-化学期末考试试卷
- 辽宁省大连市2017-2018学年高考理综-化学二模考试试卷
- 高中化学人教版(2019)必修第二册 第八章第三节 环境保护与绿色化学
- 上海市青浦区2020年高考化学二模试卷
- 2016年江苏省徐州市铜山区高考化学模拟试卷(5月份)
- 2016-2017学年陕西省宝鸡市岐山县高三上学期期中化学试卷
- 广西2017-2018学年高三理综-化学4月模拟考试试卷
- 广东省韶关市新丰县第一中学2018-2019学年高一下学期化学期中考试试卷
最近更新