河南省开封市五县2020-2021学年高二上学期化学期中考试试卷
河南省开封市五县2020-2021学年高二上学期化学期中考试试卷
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | |||||||||||||||||||||||||||||||||||||
|
某可逆反应:2A(g)
 B(g)+D(g)在3种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表: B(g)+D(g)在3种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
|
|||||||||||||||||||||||||||||||||||||
| 2. 单选题 | |
|
①pH=2的CH3COOH溶液;②pH=2的H2SO4溶液;③pH=12的氨水;④pH=12的NaOH溶液。相同条件下,有关上述溶液的比较中,正确的是( )
A . 水电离的c(H+):①=②=③=④
B . 将②、④溶液混合后,pH=7,消耗溶液的体积:②<④
C . 等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大
D . 向10mL上述四溶液中各加入90mL水后,溶液的pH:③>④>①>②
|
|
| 3. 单选题 | |
|
下列诗句或谚语中包含吸热反应过程的是( )
A . 野火烧不尽,春风吹又生
B . 春蚕到死丝方尽,蜡炬成灰泪始干
C . 千锤万凿出深山,烈火焚烧若等闲
D . 爆竹声中一岁除,春风送暖入屠苏
|
|
| 4. 单选题 | |
|
已知反应4CO+2NO2
 N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( ) N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
A . v(CO)=1.5mol•L-1•min-1
B . v(NO2)=0.7mol•L-1•min-1
C . v(N2)=0.4mol•L-1•min-1
D . v(CO2)=1.1mol•L-1•min-1
|
|
| 5. 单选题 | |
|
已知:NO2(g)+ SO2(g)
 SO3(g) +NO(g)。现将体积之比为1:2的NO2和SO2的混合气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是( ) SO3(g) +NO(g)。现将体积之比为1:2的NO2和SO2的混合气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是( )
A . 混合气体总物质的量保持不变
B . 混合气体密度保持不变
C . NO2(g)和SO2(g)的体积比保持不变
D . 每消耗1 molSO2 , 同时消耗0.5 molSO3(g)
|
|
| 6. 单选题 | |
|
氧化亚铜是一种重要的工业原料。已知1 g C(s)燃烧生成一氧化碳放出9.2 kJ的热量,氧化亚铜与氧气反应的能量变化如图所示。下列有关判断正确的是( )
A . 碳[C(s)]的燃烧热△H = -110.4 kJ·mol-1
B . 氧化亚铜与氧气的反应为吸热反应
C . 氧化亚铜与氧气反应的活化能为292 kJ·mol-1
D . C(s)+2CuO(s)=Cu2O(s)+CO(g) △H= +35.6 kJ·mol-1
|
|
| 7. 单选题 | |
|
对于xA(g)+yB(g)
 zC(g)+wD(g)的平衡体系,当升高温度时,体系的平均相对分子质量从26变成39,则下列说法正确的是( ) zC(g)+wD(g)的平衡体系,当升高温度时,体系的平均相对分子质量从26变成39,则下列说法正确的是( )
A . x+y>z+w,正反应是放热反应
B . x+y>z+w,正反应是吸热反应
C . x+y<z+w,逆反应是放热反应
D . x+y>z+w,逆反应是吸热反应
|
|
| 8. 单选题 | |
|
在恒容密闭容器中进行反应2CO2(g) +6H2(g)
 C2H5OH(g)+3H2O(g) △H。 在某压强下起始时按不同氢碳比[ C2H5OH(g)+3H2O(g) △H。 在某压强下起始时按不同氢碳比[  ]投料(如图中曲线①②③),测得CO2的平衡转化率与温度的关系如图所示,下列有关说法正确的是( ) ]投料(如图中曲线①②③),测得CO2的平衡转化率与温度的关系如图所示,下列有关说法正确的是( )
A . 该反应的△H>0
B . 氢碳比:①<②<③
C . 同压时,H2的体积分数:ψa<ψb
D . 平衡常数:Ka=Kb=Kc
|
|
| 9. 单选题 | |
|
25℃、101kPa 下:①2Na(s)+1/2O2(g)=Na2O(s) △H1=-414kJ/mol
②2Na(s)+O2(g)=Na2O2(s) △H2=-511kJ/mol 下列说法正确的是( )
A . ①和②产物的阴阳离子个数比不相等
B . ①和②生成等物质的量的产物,转移电子数不同
C . 25℃、101kPa 下,Na2O2(s)+2 Na(s)= 2Na2O(s)△H=-317kJ/mol
D . 常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
|
|
| 10. 单选题 | |
|
25℃、101 kPa时,1 g甲醇完全燃烧生成CO2和液态H2O,同时放出22.68 kJ热量。下列表示该反应的热化学方程式中正确的是( )
A . 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) △H=+1451.52 kJ·mol-1
B . CH3OH(l)+
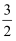 O2(g)=CO2(g)+2H2O(l) △H=-725.76 kJ·mol-1
C . 2CH3OH+O2=2CO2+4H2O △H=-22.68 kJ·mol-1
D . CH3OH(l)+ O2(g)=CO2(g)+2H2O(l) △H=-725.76 kJ·mol-1
C . 2CH3OH+O2=2CO2+4H2O △H=-22.68 kJ·mol-1
D . CH3OH(l)+ 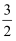 O2(g)=CO2(g)+2H2O(g) △H=-725.76 kJ·mol-1 O2(g)=CO2(g)+2H2O(g) △H=-725.76 kJ·mol-1
|
|
高中化学 试卷推荐
- 福建省福州市2017-2018学年高考理综-化学5月模拟考试试卷
- 2015-2016学年云南省曲靖市陆良二中高二上学期期末化学试卷(理科)
- 2016-2017学年上海市杨思中学高二上学期期中化学试卷
- 2016-2017学年江苏省苏州市高二上学期期中化学试卷
- 安徽省合肥市2020年高三化学一模试卷
- 2016年江西省宜春市宜丰县二中实验班高考化学五模试卷
- 上海市闵行区2016-2017学年高考化学二模考试试卷
- 2015-2016学年河北省邯郸市大名一中高二下学期第一次月考化学试卷
- 2015-2016学年海南省灵山中学高一上学期期末化学模拟试卷
- 2016-2017学年浙江省杭州市西湖高中高二上学期期中化学试卷
- 北京市西城2016-2017学年区高一上学期化学期末考试试卷
- 2015-2016学年吉林省吉林市毓文中学高一下学期期中化学试卷(理科)
最近更新





