四川省德阳市2021年高考化学三模试卷
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
化学与生活密切相关。下列说法正确的是( )
A . 在炖排骨时加醋,利于钙、铁的吸收
B . 为防止薯片被挤碎,在其包装袋中充氧气
C . 为改变面食外观,多加含铝蓬松剂
D . 为保持食物水分,用聚氯乙烯保鲜膜罩住食物加热
|
|
| 2. 单选题 | |
|
有机物R是合成达菲的中间体,它的合成过程如图所示。下列说法正确的是( )
A . “一定条件”是指稀硫酸、加热
B . 莽草酸可发生加成和水解反应
C . R含3种官能团
D . R的同分异构体中可能含苯环
|
|
| 3. 单选题 | |
|
NA为阿伏加德罗常数的值。下列说法错误的是( )
A . 常温常压下,3.2g N2H4所含共价键的数目为 0.5NA
B . 7g乙烯与7g环丙烷组成的混合物中所含氢原子数为2 NA
C . 0.5mol SO2与足量O2在适宜条件下充分反应转移电子数小于NA
D . 1L0.1mol/L的NaHSO3溶液中HSO
 和SO 和SO  的粒子数之和为0.1NA 的粒子数之和为0.1NA
|
|
| 4. 单选题 | |
|
用下列实验装置进行相应的实验,能达到实验目的的是( )
A . 装置甲:从溶液中分离出纳米铁
B . 装置乙:实验室焙烧硫酸铜晶体
C . 装置丙:测定中和反应反应热
D . 装置丁:收集二氧化氮气体
|
|
| 5. 单选题 | |
|
主族元素V、W、X、Y、Z的原子序数依次增大,且均不大于20,ZX3Y4W12是硅酸盐,X2+和W2-的电子层结构相同,V与Y的质子数之和等于Z的质子数。下列判断正确的是( )
A . Y在周期表中位于第3周期第IV族
B . V2W
 含极性键和非极性键
C . 最简氢化物的热稳定性:Y>V
D . 原子半径:Z>Y>X>W 含极性键和非极性键
C . 最简氢化物的热稳定性:Y>V
D . 原子半径:Z>Y>X>W
|
|
| 6. 单选题 | |
|
“免加水铅蓄电池”其寿命可长达4年,放电时总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。下列有关判断错误的是( )
A . 充电时,a电极发生氧化反应
B . 放电时,溶液中H+向PbO2电极迁移
C . 充电时,阴极反应为PbSO4+2e-=Pb+SO
 D . 放电时,当负极转移1mole-时,正极消耗1molH+
D . 放电时,当负极转移1mole-时,正极消耗1molH+
|
|
| 7. 单选题 | |
|
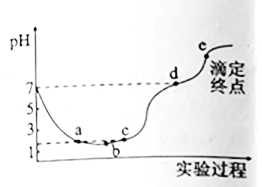
25℃时,向100mL水中缓慢通入0.01molCl2 , 然后用0.1mol/LNaOH溶液滴定所得氯水,整个过程中溶液pH的变化如图。下列说法正确的是( )
A . Ca2+、NO
 、S2O 、S2O  能在该氯水中大量共存
B . b点对应溶液所含溶质为HCl和HClO
C . 对应溶液中水的电离程度:a=c
D . d点对应溶液中:c(Na+)=c(HClO)+c(ClO-) 能在该氯水中大量共存
B . b点对应溶液所含溶质为HCl和HClO
C . 对应溶液中水的电离程度:a=c
D . d点对应溶液中:c(Na+)=c(HClO)+c(ClO-)
|
|
| 8. 综合题 | |
|
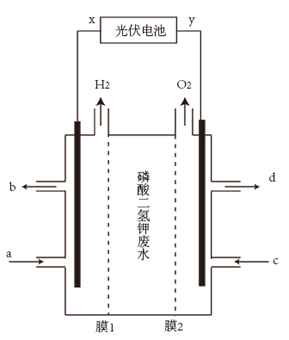
氮的循环在自然界元素的循环中具有重要的意义,但减少含氮化合物对空气的污染也是重要的课题之一。
已知:N2(g)+O2(g)⇌2NO(g) ΔH1=+180.0kJ·mol-1 N2(g)+3H2(g)⇌2NH3(g) ΔH2=-92.4kJ·mol-1 H2的燃烧热为285.8kkJ·mol-1。 回答下列问题:
|
|
| 9. 实验探究题 | |||||||||||||
|
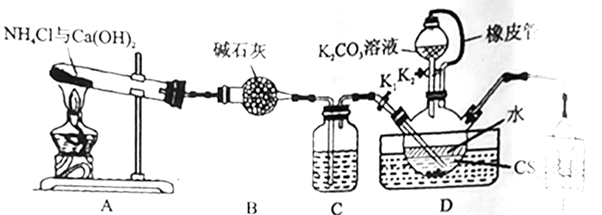
硫氰化钾(KSCN)是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置(部分夹持仪器略去)如下图所示:
已知:①NH3不溶于CS2; ②在水溶液中,NH4HS、(NH4)2CO3受热易分解,NH4SCN在高于170℃时易分解; ③D中缓慢反应:CS2+3NH3 回答下列问题:
|
|||||||||||||
| 10. 综合题 | |
|
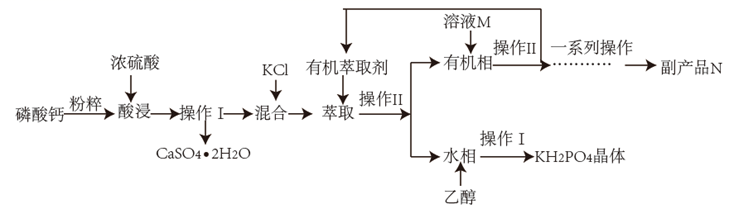
以磷酸钙为原料可制备缓冲试剂磷酸二氢钾(KH2PO4),其工艺流程如图所示:
已知:①Ca(H2PO4)2能溶于水,CaHPO4和Ca3(PO4)2均难溶于水。 ②萃取原理:KCl+H3PO4⇌KH2PO4+HCl,HCl易溶于有机萃取剂。 回答下列问题:
|
|
- 广西桂林、崇左市2021年高考理综-化学二模试卷
- 江西省上饶市2021-2022学年高一上学期期末质量检测化学试题
- 黑龙江省齐齐哈尔市2021年高考理综-化学一模试卷
- 安徽省安庆市2021年高考理综-化学一模试卷
- 浙江省2022 年1月普通高校招生选考科目考试化学试题
- 宁夏石嘴山市2021年高考化学一模试卷
- 浙江省诸暨市2021年高考化学5月模拟试卷
- 山西省临汾市2022届高三下学期考前适应性训练考试(三)理科综合化学试题
- 辽宁省六校2020-2021学年高一上学期化学期中考试试卷
- 江苏高邮市2021-2022学年高一下学期期中考试化学试题
- 吉林省吉林市第二中2020-2021学年高一上学期化学9月月考试卷
- 广东省普宁市2020-2021学年高一下学期化学期中考试试卷





 NH4HS+NH4SCN。
NH4HS+NH4SCN。