福建省泉州市2020年高考化学5月模拟试卷
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
化学与生活密切相关。下列叙述正确的是( )
A . 硫磺皂中的硫单质具有杀菌的功效
B . 食品袋中放置的CaO可防止食品氧化变质
C . 草木灰与硝酸铵混合施用效果更好
D . 用碳酸钡、碳酸镁和氢氧化铝等作抗酸药
|
|
| 2. 单选题 | |
|
管道工人曾经用浓氨水检查氯气管道是否漏气,发生反应:8NH3+3Cl2=6NH4Cl+N2。下列叙述正确的是( )
A . NH3的电子式为
|
|
| 3. 单选题 | |
|
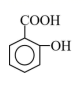
水杨酸(结构如图所示)为柳树皮提取物之一,是一种天然的消炎药,主要作为医药工业的原料。下列关于水杨酸的叙述错误的是( )
A . 分子式为C7H6O3
B . 能发生加成、酯化、中和等反应
C . 苯环上的二氯取代物有5种
D . 所有原子均可能在同一平面上
|
|
| 4. 单选题 | |
|
前20号元素M、N、R、Q、Z的原子序数依次递增,M与Z、N与Q分别同主族,M、N形成的常见化合物有M2N、M2N2 , 由该5种元素组成的某结晶化合物X常用作净水剂。下列叙述错误的是( )
A . 化合物X中含有离子键和共价键
B . 简单离子半径由大到小的顺序为Z˃R˃Q˃N
C . N、Q分别与Z形成化合物的水溶液均呈碱性
D . R、Q、Z的最高价氧化物的水化物间能相互反应
|
|
| 5. 单选题 | |
|
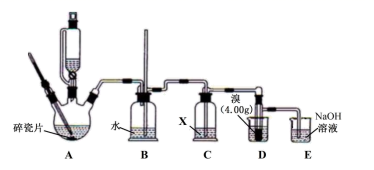
卤素互化物如ICl、ICl3等具有与卤素单质相似的性质。利用反应I2+Cl2=2ICl,实验室可用如图所示装置(夹持仪器已略去)制取少量ICl3。已知:ICl的熔点为27.2℃,沸点为97.40C,容易水解,能发生反应:ICl+Cl2=ICl3。下列叙述错误的是( )
A . 圆底烧瓶中的固体可以为KMnO4或KClO3
B . 装置B、C中的试剂分别为饱和食盐水和浓硫酸
C . 装置E的作用为吸收尾气,可用装置F替代
D . 盐酸的滴加速度过快,ICl的产率会明显降低
|
|
| 6. 单选题 | |
|
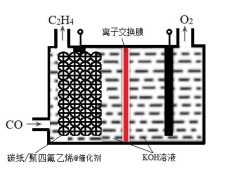
某研究团队在优化催化剂的基础上,通过调节电极的孔道和疏水性增加CO的扩散速率,实现了高选择性将CO电解还原制备乙烯,如图所示。下列叙述错误的是( )
A . 碳纸/聚四氟乙烯电极为阴极
B . 聚四氟乙烯的作用是吸附并增加CO的浓度
C . 为了维持电解的效率,离子交换膜应为阳离子交换膜
D . 碳纸上生成C2H4的电极反应式为:2CO+6H2O+8e-=C2H4+8OH-
|
|
| 7. 单选题 | |
|
常温下,用0.010mol/L的NaOH溶液滴定10.00mL 0.010mol/L的酸H2A,滴定过程中加入NaOH溶液的体积(V)与溶液中lg
 的关系如图所示(10mL之后的曲线未画出)。下列叙述正确的是( ) 的关系如图所示(10mL之后的曲线未画出)。下列叙述正确的是( )
A . H2A
 H++HA-
B . Ka(HA-)的数量级为10-5
C . 滴定过程中,水的电离程度最大的为B点溶液
D . V(NaOH)=15mL时的溶液中:c(Na+)>c(A2-)>c(HA-) H++HA-
B . Ka(HA-)的数量级为10-5
C . 滴定过程中,水的电离程度最大的为B点溶液
D . V(NaOH)=15mL时的溶液中:c(Na+)>c(A2-)>c(HA-)
|
|
| 8. 实验探究题 | |
|
1,2—二溴乙烷[BrCH2CH2Br,常温下为无色液体,难溶于水,密度比水大,熔点9℃,沸点132℃]常用作熏蒸消毒的溶剂。利用以下原理可在实验室制取:2C2H5OH
 CH2=CH2 CH2=CH2  BrCH2CH2Br。 BrCH2CH2Br。 已知:140℃时发生副反应生成乙醚(C2H5OC2H5),局部过热会生成SO2、CO2。 实验步骤如下: ①按如图组装仪器(夹持装置略),检查气密性后添加试剂。 ②在冰水浴冷却、搅拌下,将20mL浓硫酸缓慢加到10mL95%乙醇中,取出5mL混合液加入三颈烧瓶中,将剩余部分移入恒压滴液漏斗。 ③加热A至175℃,打开恒压滴液漏斗活塞,慢慢滴加混合液至D中液溴反应完全。 ④将D中产物移到分液漏斗,依次用水、NaOH溶液、水洗涤并分液,往有机相加入适量MgSO4固体,过滤、操作Y,收集到BrCH2CH2Br4.23g。 请回答以下问题:
|
|
| 9. 综合题 | |
|
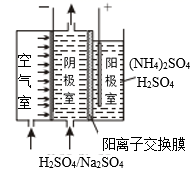
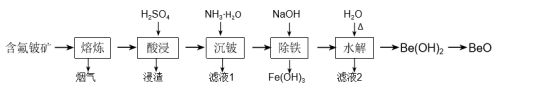
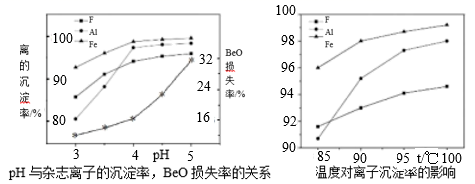
铍是原子能、火箭、导弹、航空、宇宙航行以及冶金工业中不可缺少的一种新兴材料。以某地的含氟铍矿(主要成分为BeO、CaF2、Al2O3、Fe2O3、SiO2及少量的硫酸盐)为原料,生产工业氧化铍的一种工艺流程如图:
已知:①25℃,Ksp(CaCO3)=8.7×10-9;Ksp(CaSO4)=2.5×10-5; ②Be(OH)2与Al(OH)3性质相似。 回答下列问题:
|
|
| 10. 综合题 | ||||||||||||||||||||||||||||||||||||||
|
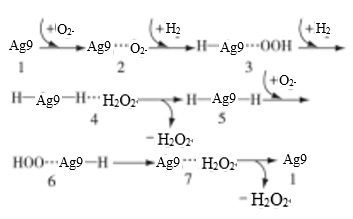
H2O2作为绿色氧化剂被应用于废水处理、造纸和化学合成等行业。
|
||||||||||||||||||||||||||||||||||||||
- 上海市金山区2020年高考化学二模试卷
- 2016-2017学年湖北省重点高中联考协作体高二上学期期中化学试卷
- 2015-2016学年山西省大同市阳高一中高一下学期期中化学试卷
- 河南省洛阳市2019-2020学年高二下学期化学期末考试试卷
- 高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第三节 化学平衡 化学平衡第二课时(化学平衡状态)
- 2016年四川省巴中市平昌中学高考化学二诊试卷
- 人教版化学高二选修1第四章第三节垃圾资源化同步练习
- 湖北省黄冈市2016-2017学年高二上学期化学期末考试试卷
- 2016-2017学年吉林省吉林五十五中高二上学期期中化学试卷
- 江苏省盐城市2017-2018学年高考化学三模考试试卷
- 福建省厦门市2017-2018学年高一下学期化学期末考试试卷
- 2017_2018学年高中化学新人教版必修二 第三章 第一节 最简单的有机化合物—甲烷


 O2(g)=H2O(l) ΔH1=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH1=-285.8kJ·mol-1 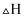
 mol-1
mol-1 O2+H2
O2+H2  Ag9
Ag9