人教高中化学一轮复习:专题2 物质分类及变化
人教高中化学一轮复习:专题2 物质分类及变化
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 多选题 | |
|
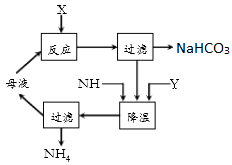
侯氏制碱法是连续循环生产的过程,主要流程见图,有关该流程的叙述中正确的是( )
A . 母液中含有大量的Na+、NH4+、Cl﹣、CO32﹣
B . 通入NH3只是为了增加NH4+浓度
C . 加入的Y物质为CO2
D . 生产过程中还需要补充水
|
|
| 2. 填空题 | |
|
(1)化学实验操作的“先”与“后”,对化学实验结果、师生安全等具有十分重要的意义.我们在进行化学实验时,若遇到下列情况,应如何操作.
①给试管中的药品加热,必须先 ,后集中加热. ②点燃可燃性气体(如H2、CO等)时,都要先 , 后点燃. ③H2还原CuO实验结束时,要先 ,后移去导气管. (2)要分离下列四组混合物:a.饱和食盐水与沙子 b.从KNO3和NaCl的混合溶液中获得KNO3 c.水和汽油的混合物 d.CCl4液体与甲苯液体的混合物(已知CCl4与甲苯互溶,沸点分别为76.75℃和110.6℃) ①分离a、b的操作分别为 、 . ②上述四组分离时需使用酒精灯的有 和 (填序号). ③分离c时所使用仪器中有一种在其他组分分离时无需使用,这种仪器是 |
|
| 3. 综合题 | |
|
有反应:4Zn+10HNO3(极稀过量)→4Zn(NO3)2+NH4NO3+3H2O
|
|
| 4. 填空题 | |
|
3molNH3与2molH2S所含氢原子的数目之比为;它们的质量之比为;在标准状况下,3molNH3的体积为L。
|
|
| 5. 填空题 | |
|
下面所列物质中,属于强电解质的是(填序号,下同),属于弱电解质的是,属于非电解质的是。
①氯化钾②乙醇③醋酸④氨气⑤蔗糖⑥硫化氢⑦硫酸氢钠⑧一水合氨⑨氯气⑩碳酸钡⑪铁 |
|
| 6. 填空题 | |
|
取3支试管并标记甲、乙、丙,分别依次倒入H2SO4 , Na2SO4溶液,Na2CO3溶液,然后各加入几滴BaCl2溶液,观察现象。再分别加入少量稀盐酸,振荡,观察现象。写出加入稀盐酸后的离子反应方程式:。
|
|
| 7. 多选题 | |
|
NaCl是一种化工原料,可以制备一系列物质(见图)。下列说法正确的是( )
A . 25 ℃时,NaHCO3在水中的溶解度比Na2CO3的大
B . 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂
C . 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应
D . 如图所示转化反应不都是氧化还原反应
|
|
| 8. 多选题 | |
|
每年10月23日上午6∶02到晚上6∶02被誉为“摩尔日"(MoleDay),这个时间的美式写法为6∶0210/23,外观与阿伏加德罗常数近似值6.02×1023相似。用NA代表阿伏加德罗常数的值,下列说法正确的是( )
A . 1molO2作为氧化剂参与反应,得到的电子数一定为4NA
B . 46gNO2和N2O4的混合气体所含的原子数为3NA
C . 0.4mol/LNa2SO4溶液中所含Na+和
 总数为1.2NA
D . 标准状况下,18g水所占的体积小于22.4L 总数为1.2NA
D . 标准状况下,18g水所占的体积小于22.4L
|
|
| 9. 多选题 | |
|
下列电离方程式或离子方程式书写正确的是( )
A . NaHSO4(熔融)=Na++H++SO
 B . 氯化铁溶液腐蚀铜电路板:Cu+2Fe3+=Cu2++2Fe2+
C . 过量Ca(HCO3)2溶液与NaOH溶液反应:HCO
B . 氯化铁溶液腐蚀铜电路板:Cu+2Fe3+=Cu2++2Fe2+
C . 过量Ca(HCO3)2溶液与NaOH溶液反应:HCO  +OH-+Ca2+=CaCO3↓+H2O
D . Na2O加入稀硫酸中:O2-+2H+=H2O +OH-+Ca2+=CaCO3↓+H2O
D . Na2O加入稀硫酸中:O2-+2H+=H2O
|
|
| 10. 多选题 | |
|
废水脱氮工艺中有一种方法是在废水中加入过量的NaClO使NH
 完全转化为N2 , 该反应可表示为2NH 完全转化为N2 , 该反应可表示为2NH  +3ClO-=N2↑+3Cl-+2H++3H2O。下列说法中错误的是( ) +3ClO-=N2↑+3Cl-+2H++3H2O。下列说法中错误的是( )
A . 反应中每生成1molN2 , 转移3mol电子
B . 还原性:NH
 <Cl-
C . 反应中NH <Cl-
C . 反应中NH  被氧化,ClO-被还原
D . 经此法处理过的废水不可以直接排放 被氧化,ClO-被还原
D . 经此法处理过的废水不可以直接排放
|
|
高中化学 试卷推荐
- 2015-2016学年辽宁省锦州市高二下学期期末化学试卷
- 广东省汕头市金山中学2019-2020学年高二下学期化学6月月考试卷
- 2016-2017学年贵州省黔南州都匀一中高二上学期开学化学试卷
- 人教版高中化学选修五 第四章第三节:蛋白质和核酸
- 四川省内江市威远县自强中学2015-2016学年高三上学期化学期中考试试卷
- 高中化学鲁科版(2019)选择性必修2 第2章第3节 离子健、配位键与金属键
- 湖北省荆州市部分区县2019-2020学年高一上学期化学期末考试试卷
- 高中化学人教版(2019)选择性必修1第四章实验活动4简单的电镀实验
- 人教版化学高二选修5第五章第二节应用广泛的高分子材料同步练习
- 高中化学人教版(新课标)选修4 第二章第一节 化学反应速率
- 备考2018年高考化学二轮专题复习 综合复习:物质结构与性质
- 辽宁省锦州市2019-2020学年高一下学期化学期末考试试卷
最近更新