жұҹиӢҸзңҒиҝһдә‘жёҜеёӮдёңжө·еҺҝ2021-2022еӯҰе№ҙй«ҳдәҢдёӢеӯҰжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰиҜ•йўҳ
жұҹиӢҸзңҒиҝһдә‘жёҜеёӮдёңжө·еҺҝ2021-2022еӯҰе№ҙй«ҳдәҢдёӢеӯҰжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰиҜ•йўҳ
ж•ҷжқҗзүҲжң¬пјҡеҢ–еӯҰ
иҜ•еҚ·еҲҶзұ»пјҡеҢ–еӯҰй«ҳдәҢдёӢеӯҰжңҹ
иҜ•еҚ·еӨ§е°Ҹпјҡ1.0 MB
ж–Ү件зұ»еһӢпјҡ.doc жҲ– .pdf жҲ– .zip
еҸ‘еёғж—¶й—ҙпјҡ2024-05-01
жҺҲжқғж–№ејҸпјҡе…Қиҙ№дёӢиҪҪ
дёӢиҪҪең°еқҖпјҡзӮ№жӯӨдёӢиҪҪ
ж•ҷжқҗзүҲжң¬пјҡеҢ–еӯҰ
иҜ•еҚ·еҲҶзұ»пјҡеҢ–еӯҰй«ҳдәҢдёӢеӯҰжңҹ
иҜ•еҚ·еӨ§е°Ҹпјҡ1.0 MB
ж–Ү件зұ»еһӢпјҡ.doc жҲ– .pdf жҲ– .zip
еҸ‘еёғж—¶й—ҙпјҡ2024-05-01
жҺҲжқғж–№ејҸпјҡе…Қиҙ№дёӢиҪҪ
дёӢиҪҪең°еқҖпјҡзӮ№жӯӨдёӢиҪҪ
д»ҘдёӢдёәиҜ•еҚ·йғЁеҲҶиҜ•йўҳйў„и§Ҳ
| 1. еҚ•йҖүйўҳ | |
|
жҲ‘еӣҪеҢ–е·Ҙ专家дҫҜеҫ·жҰңеҸ‘жҳҺзҡ„дҫҜж°ҸеҲ¶зўұжі•(еҸҲз§°иҒ”еҗҲеҲ¶зўұжі•)пјҢе…¶дёӯж¶үеҸҠзҡ„еҸҚеә”д№ӢдёҖдёәNaCl+ CO2 + NH3+ H2O= NaHCO3вҶ“+ NH4ClгҖӮдёӢ еҲ—жңүе…іиҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү
A . CO2еұһдәҺз”өи§ЈиҙЁ
B . NH4Clжә¶ж¶ІжҳҫзўұжҖ§
C . NaHCO3дёӯеҸӘеҗ«зҰ»еӯҗй”®
D . иҜҘеҸҚеә”еұһдәҺйқһж°§еҢ–иҝҳеҺҹеҸҚеә”
|
|
| 2. еҚ•йҖүйўҳ | |
|
еҸҚеә”SiO2+4HF=SiF4вҶ‘+2H2OеҸҜз”ЁдәҺйӣ•еҲ»зҺ»з’ғгҖӮдёӢеҲ—жңүе…іиҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү
A . SiеңЁе‘ЁжңҹиЎЁдёӯдҪҚдәҺ第3е‘ЁжңҹVIAж—ҸгҖӮ
B . HFзҡ„зҡ„з”өеӯҗејҸдёәHпјҡF
C . SiF4жҳҜйқһжһҒжҖ§еҲҶеӯҗ
D . H2Oдёӯж°§еҺҹеӯҗиҪЁйҒ“жқӮеҢ–зұ»еһӢдёәsp2
|
|
| 3. еҚ•йҖүйўҳ | |
|
дёӢеҲ—жңүе…ізү©иҙЁзҡ„жҖ§иҙЁдёҺз”ЁйҖ”дёҚе…·жңүеҜ№еә”е…ізі»зҡ„жҳҜпјҲ пјү
A . NaClOжңүж°§еҢ–жҖ§пјҢеҸҜз”ЁдәҺж¶ҲжҜ’жқҖиҸҢ
B . Na2CO3жҳ“жә¶дәҺж°ҙпјҢеҸҜз”ЁдәҺйҷӨжІ№жұЎ
C . Na2SO3 жңүиҝҳеҺҹжҖ§пјҢеҸҜз”ЁдҪңжҠ—ж°§еҢ–еүӮ
D . NaHCO3 еҸ—зғӯжҳ“еҲҶи§ЈпјҢеҸҜз”ЁдәҺеҲ¶еҸ‘й…өзІү
|
|
| 4. еҚ•йҖүйўҳ | |
|
еңЁжҢҮе®ҡжқЎд»¶ дёӢпјҢдёӢеҲ—йҖүйЎ№жүҖзӨәзү©иҙЁй—ҙиҪ¬еҢ–иғҪе®һзҺ°зҡ„жҳҜпјҲ пјү
A . Fe(s)
 FeCl2(s)
B . FeO(s) FeCl2(s)
B . FeO(s) Fe(NO3)2(aq)
C . Fe(OH)2(s) Fe(NO3)2(aq)
C . Fe(OH)2(s)  Fe(OH)3(s)
D . FeCl3(aq) Fe(OH)3(s)
D . FeCl3(aq)  Fe(s) Fe(s)
|
|
| 5. еҚ•йҖүйўҳ | |
|
дёӢ еҲ—жңүе…іеҸҚеә”N2(g)+ 3H2(g)
 2NH3(g)О”H= -92.4 kJВ·mol-1зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү 2NH3(g)О”H= -92.4 kJВ·mol-1зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү
A . NH3еҲҶеӯҗй—ҙиғҪеҪўж°ўй”®
B . еҸҚеә”дёӯN2дҪ“зҺ°дәҶиҝҳеҺҹжҖ§
C . жҸҗй«ҳ
 зҡ„еҖјеҸҜеўһеӨ§N2зҡ„иҪ¬еҢ–зҺҮ
D . еҸҜд»ҘдҪҝз”Ёй…¶дҪңиҜҘеҸҚеә”зҡ„еӮ¬еҢ–еүӮ зҡ„еҖјеҸҜеўһеӨ§N2зҡ„иҪ¬еҢ–зҺҮ
D . еҸҜд»ҘдҪҝз”Ёй…¶дҪңиҜҘеҸҚеә”зҡ„еӮ¬еҢ–еүӮ
|
|
| 6. еҚ•йҖүйўҳ | |
|
еүҚ4е‘Ёжңҹдё»ж—Ҹе…ғзҙ XгҖҒYгҖҒZгҖҒWзҡ„еҺҹеӯҗеәҸж•°дҫқж¬ЎеўһеӨ§пјҢXжҳҜең°еЈідёӯеҗ«йҮҸжңҖеӨҡзҡ„е…ғзҙ пјҢYеҺҹеӯҗзҡ„жңҖеӨ–еұӮз”өеӯҗж•°дёҺжңҖеҶ…еұӮз”өеӯҗж•°зӣёзӯүпјҢеҹәжҖҒж—¶ZеҺҹеӯҗ3pеҺҹеӯҗиҪЁйҒ“дёҠжңү2дёӘжңӘжҲҗеҜ№з”өеӯҗпјҢWжҳҜеүҚ4е‘ЁжңҹдёӯйҮ‘еұһжҖ§жңҖејәзҡ„е…ғзҙ гҖӮдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү
A . еҺҹеӯҗеҚҠеҫ„пјҡr(X)пјңr(Y)пјңr(Z)пјңr(W)
B . Xзҡ„з®ҖеҚ•ж°”жҖҒж°ўеҢ–зү©зҡ„зғӯзЁіе®ҡжҖ§жҜ”Zзҡ„ејә
C . Yзҡ„第дёҖз”өзҰ»иғҪжҜ”Zзҡ„еӨ§
D . Wзҡ„жңҖй«ҳд»·ж°§еҢ–зү©еҜ№еә”зҡ„ж°ҙеҢ–зү©зҡ„зўұжҖ§жҜ”Yзҡ„ејұ
|
|
| 7. еҚ•йҖүйўҳ | |
|
CuSO4еёёз”ЁдҪңеҶңдёҡжқҖиҸҢеүӮгҖҒеҲҶжһҗиҜ•еүӮгҖҒеӘ’жҹ“еүӮе’ҢйҳІи…җеүӮзӯүгҖӮе®һйӘҢе®ӨеҲ©з”Ёеәҹй“ңеұ‘еҲ¶еӨҮCuSO4жңүдёүз§ҚйҖ”еҫ„пјҡдёҖжҳҜе°Ҷеәҹй“ңеұ‘дёҺжө“зЎ«й…ёе…ұзғӯпјҢжӯӨж–№жі•дјҡдә§з”ҹжұЎжҹ“жҖ§ж°”дҪ“SO2пјӣдәҢжҳҜе…Ҳе°Ҷеәҹй“ңеұ‘еҠ зғӯж°§еҢ–жҲҗCuOпјҢ然еҗҺеҶҚз”ЁзЁҖзЎ«й…ёжә¶и§ЈпјҢиҜҘж–№жі•иҖ—иғҪиҫғеӨҡпјӣдёүжҳҜеңЁеёёжё©дёӢз”ЁH2O2е’ҢH2SO4зҡ„ж··еҗҲжә¶ж¶ІжөёеҸ–еәҹй“ңеұ‘иҺ·еҫ—CuSO4 пјҢ иҜҘж–№жі•з»ҝиүІзҺҜдҝқдё”иҠӮиғҪпјҢеҸҚеә”дёәCu(s)+ H2O2(l) + 2H+ (aq)= Cu2+(aq)+ 2H2O(1) О”H =-319.68 kJВ·mol-1гҖӮдёӢеҲ—жңүе…іCuгҖҒSO
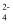 гҖҒCu2+зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү гҖҒCu2+зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү
A . CuеҸҜд»ҘдҪҝиӣӢзҷҪиҙЁеҸҳжҖ§
B . CuеҹәжҖҒд»·з”өеӯҗжҺ’еёғејҸдёә3d94s2
C . SO
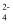 зҡ„з©әй—ҙжһ„еһӢдёәжӯЈеӣӣйқўдҪ“
D . Cu2+дёҺNH3еҪўжҲҗзҡ„[Cu(NH3)4]2+дёӯй…ҚдҪҚж•°жҳҜ2 зҡ„з©әй—ҙжһ„еһӢдёәжӯЈеӣӣйқўдҪ“
D . Cu2+дёҺNH3еҪўжҲҗзҡ„[Cu(NH3)4]2+дёӯй…ҚдҪҚж•°жҳҜ2
|
|
| 8. еҚ•йҖүйўҳ | |
|
CuSO4еёёз”ЁдҪңеҶңдёҡжқҖиҸҢеүӮгҖҒеҲҶжһҗиҜ•еүӮгҖҒеӘ’жҹ“еүӮе’ҢйҳІи…җеүӮзӯүгҖӮе®һйӘҢе®ӨеҲ©з”Ёеәҹй“ңеұ‘еҲ¶еӨҮCuSO4жңүдёүз§ҚйҖ”еҫ„пјҡдёҖжҳҜе°Ҷеәҹй“ңеұ‘дёҺжө“зЎ«й…ёе…ұзғӯпјҢжӯӨж–№жі•дјҡдә§з”ҹжұЎжҹ“жҖ§ж°”дҪ“SO2пјӣдәҢжҳҜе…Ҳе°Ҷеәҹй“ңеұ‘еҠ зғӯж°§еҢ–жҲҗCuOпјҢ然еҗҺеҶҚз”ЁзЁҖзЎ«й…ёжә¶и§ЈпјҢиҜҘж–№жі•иҖ—иғҪиҫғеӨҡпјӣдёүжҳҜеңЁеёёжё©дёӢз”ЁH2O2е’ҢH2SO4зҡ„ж··еҗҲжә¶ж¶ІжөёеҸ–еәҹй“ңеұ‘иҺ·еҫ—CuSO4 пјҢ иҜҘж–№жі•з»ҝиүІзҺҜдҝқдё”иҠӮиғҪпјҢеҸҚеә”дёәCu(s)+ H2O2(l) + 2H+ (aq)= Cu2+(aq)+ 2H2O(l) О”H =-319.68 kJВ·mol-1гҖӮеҜ№дәҺеҸҚеә” Cu(s)+ H2O2(l) +2H+ (aq)= Cu2+(aq)+ 2H2O(l) О”H = -319.68kJВ·mol-1 пјҢ дёӢеҲ—жңүе…іиҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү
A . еҸҜд»ҘйҮҮз”Ёй«ҳжё©жқЎд»¶еҠ еҝ«иҜҘеҸҚеә”зҡ„йҖҹзҺҮ
B . еҸҚеә”еҗҺеҸҜд»ҘйҮҮз”ЁеҠ зғӯж–№жі•йҷӨеҺ»еӨҡдҪҷзҡ„H2O2
C . иҜҘеҸҚеә”еңЁеёёжё©дёӢиғҪиҮӘеҸ‘иҝӣиЎҢпјҢеҲҷеҸҚеә”зҡ„О”SдёҖе®ҡеӨ§дәҺ0
D . еҸҚеә”дёӯжҜҸиҪ¬з§»1mol з”өеӯҗпјҢзҗҶи®әдёҠиҮіе°‘йңҖж¶ҲиҖ—1mol H2O2
|
|
| 9. еҚ•йҖүйўҳ | |
|
CuSO4еёёз”ЁдҪңеҶңдёҡжқҖиҸҢеүӮгҖҒеҲҶжһҗиҜ•еүӮгҖҒеӘ’жҹ“еүӮе’ҢйҳІи…җеүӮзӯүгҖӮе®һйӘҢе®ӨеҲ©з”Ёеәҹй“ңеұ‘еҲ¶еӨҮCuSO4жңүдёүз§ҚйҖ”еҫ„пјҡдёҖжҳҜе°Ҷеәҹй“ңеұ‘дёҺжө“зЎ«й…ёе…ұзғӯпјҢжӯӨж–№жі•дјҡдә§з”ҹжұЎжҹ“жҖ§ж°”дҪ“SO2пјӣдәҢжҳҜе…Ҳе°Ҷеәҹй“ңеұ‘еҠ зғӯж°§еҢ–жҲҗCuOпјҢ然еҗҺеҶҚз”ЁзЁҖзЎ«й…ёжә¶и§ЈпјҢиҜҘж–№жі•иҖ—иғҪиҫғеӨҡпјӣдёүжҳҜеңЁеёёжё©дёӢз”ЁH2O2е’ҢH2SO4зҡ„ж··еҗҲжә¶ж¶ІжөёеҸ–еәҹй“ңеұ‘иҺ·еҫ—CuSO4 пјҢ иҜҘж–№жі•з»ҝиүІзҺҜдҝқдё”иҠӮиғҪпјҢеҸҚеә”дёәCu(s)+ H2O2(l) + 2H+ (aq)= Cu2+(aq)+ 2H2O(1) О”H =-319.68 kJВ·mol-1гҖӮе®һйӘҢе®ӨеҲ©з”Ёеәҹй“ңеұ‘дёҺжө“зЎ«й…ёеҸҚеә”еҲ¶еӨҮCuSO4并иҝӣиЎҢжңүе…іе®һйӘҢж—¶пјҢдёӢеҲ—иЈ…зҪ®иғҪиҫҫеҲ°зӣёеә”е®һйӘҢзӣ®зҡ„зҡ„жҳҜпјҲ пјү
A . з”ЁиЈ…зҪ®з”ІеҲ¶еҸ–CuSO4
B . з”ЁиЈ…зҪ®д№ҷи§ӮеҜҹCuSO4жә¶ж¶Ізҡ„йўңиүІ
C . з”ЁиЈ…зҪ®дёҷиҝҮж»Өеҫ—еҲ°CuSO4жә¶ж¶ІгҖӮ
D . з”ЁиЈ…зҪ®дёҒеҗёж”¶еӨҡдҪҷзҡ„SO2
|
|
| 10. еҚ•йҖүйўҳ | |
|
е·ҘдёҡдёҠеёёз”ЁвҖңзғӯз©әж°”жі•вҖқе°Ҷд»Һжө·ж°ҙдёӯжҸҗеҸ–зҡ„зІ—жәҙзІҫеҲ¶еҫ—еҲ°й«ҳзәҜеәҰзҡ„жәҙеҚ•иҙЁгҖӮдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү
A . Br2дёҺSO2гҖҒH2OеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸпјҡ Br2+ SO2+ 2H2O=4H++2Br- + SO
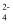 B . з”ЁCO2д»ЈжӣҝжөҒзЁӢдёӯзҡ„SO2д№ҹеҸҜд»ҘиҫҫеҲ°еҗҢж ·зҡ„зӣ®зҡ„
C . йҖҡе…ҘCl2зҡ„зӣ®зҡ„жҳҜе°ҶBr-иҝҳеҺҹдёәBr2
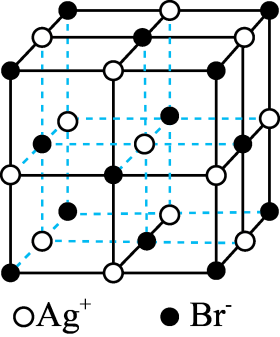
D . еҗ‘вҖңBr2жә¶ж¶ІвҖқдёӯеҠ е…ҘAgNO3жә¶ж¶Ідјҡз”ҹжҲҗAgBrжІүж·ҖпјҢ1дёӘAgBrжҷ¶иғһ(еҰӮеӣҫжүҖзӨә)дёӯеҗ«жңү14дёӘBr -
B . з”ЁCO2д»ЈжӣҝжөҒзЁӢдёӯзҡ„SO2д№ҹеҸҜд»ҘиҫҫеҲ°еҗҢж ·зҡ„зӣ®зҡ„
C . йҖҡе…ҘCl2зҡ„зӣ®зҡ„жҳҜе°ҶBr-иҝҳеҺҹдёәBr2
D . еҗ‘вҖңBr2жә¶ж¶ІвҖқдёӯеҠ е…ҘAgNO3жә¶ж¶Ідјҡз”ҹжҲҗAgBrжІүж·ҖпјҢ1дёӘAgBrжҷ¶иғһ(еҰӮеӣҫжүҖзӨә)дёӯеҗ«жңү14дёӘBr -
|
|
й«ҳдёӯеҢ–еӯҰ иҜ•еҚ·жҺЁиҚҗ
- жөҷжұҹзңҒжөҷеҚ—еҗҚж ЎиҒ”зӣҹ2020-2021еӯҰе№ҙй«ҳдёҖдёӢеӯҰжңҹеҢ–еӯҰ3жңҲжңҲиҖғиҜ•еҚ·
- е№ҝдёңзңҒдёңиҺһеёӮ2020-2021еӯҰе№ҙй«ҳдёҖдёӢеӯҰжңҹжңҹжң«иҒ”иҖғжөӢиҜ•еҢ–еӯҰиҜ•йўҳ
- жұҹиӢҸзңҒжі°е·һеёӮ2020-2021еӯҰе№ҙй«ҳдёүдёҠеӯҰжңҹеҢ–еӯҰжңҹдёӯиҖғиҜ•иҜ•еҚ·
- жөҷжұҹзңҒд№Ӣжұҹж•ҷиӮІиҜ„д»·2020-2021еӯҰе№ҙй«ҳдёүдёӢеӯҰжңҹеҢ–еӯҰејҖеӯҰиҖғиҜ•иҜ•еҚ·
- е®үеҫҪзңҒеҗҲиӮҘеёӮе…ӯж Ў2020-2021еӯҰе№ҙй«ҳдәҢдёӢеӯҰжңҹжңҹжң«иҒ”иҖғеҢ–еӯҰиҜ•йўҳ
- жұҹиӢҸзңҒе®ҝиҝҒеёӮ2021е№ҙй«ҳиҖғеҢ–еӯҰдәҢжЁЎиҜ•еҚ·
- еҢ—дә¬еёӮжө·ж·ҖеҢә2021е№ҙй«ҳиҖғеҢ–еӯҰдәҢжЁЎиҜ•еҚ·
- еӨ©жҙҘеёӮж»Ёжө·ж–°еҢәеӨ§жёҜ油田第дёүдёӯеӯҰ2020-2021еӯҰе№ҙй«ҳдәҢдёҠеӯҰжңҹеҢ–еӯҰжңҹдёӯиҖғиҜ•иҜ•еҚ·
- еҢ—дә¬еёӮйҖҡе·һеҢә2021е№ҙй«ҳиҖғеҢ–еӯҰдёҖжЁЎиҜ•еҚ·
- еӣӣе·қзңҒйҒӮе®ҒеёӮ2020-2021еӯҰе№ҙй«ҳдёҖдёҠеӯҰжңҹжңҹжң«ж•ҷеӯҰж°ҙе№ізӣ‘жөӢеҢ–еӯҰиҜ•йўҳ
- иҫҪе®ҒзңҒзӣҳй”ҰеёӮиӮІжүҚеӯҰж Ў2020-2021еӯҰе№ҙй«ҳдәҢдёӢеӯҰжңҹеҢ–еӯҰејҖеӯҰиҖғиҜ•иҜ•еҚ·
- ж–°з–ҶеЎ”еҺҝ2020-2021еӯҰе№ҙй«ҳдёҖдёӢеӯҰжңҹеҢ–еӯҰжңҹжң«иҖғиҜ•иҜ•еҚ·
жңҖиҝ‘жӣҙж–°