江苏省苏州市2022届高考考前模拟化学试卷题
江苏省苏州市2022届高考考前模拟化学试卷题
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
工业可通过Al2O3+N2+3C
 2AlN+3CO制得高温陶瓷材料AlN。下列说法正确的是( ) 2AlN+3CO制得高温陶瓷材料AlN。下列说法正确的是( )
A . 传统陶瓷主要成分是硅酸盐
B . AlN是分子晶体
C . N2发生氧化反应
D . 反应为复分解反应
|
|
| 2. 单选题 | |
|
反应Cl2+Na2SO3+H2O=Na2SO4+2HCl可用于污水脱氯。下列说法正确的是( )
A . 中子数为20的氯原子:
 Cl
B . H2O分子中含极性共价键
C . Na+的结构示意图: Cl
B . H2O分子中含极性共价键
C . Na+的结构示意图: D . HCl的电子式:
D . HCl的电子式: |
|
| 3. 单选题 | |
|
侯氏制碱法原理为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。下列有关模拟侯氏制碱法的实验原理和装置能达到实验目的的是( )
A . 制取氨气
 B . 制NaHCO3
B . 制NaHCO3 C . 分离NaHCO3
C . 分离NaHCO3 D . 制Na2CO3
D . 制Na2CO3
|
|
| 4. 单选题 | |
|
SO2、NOx是重要化工原料,可用于硫酸、硝酸的生产。工业制硫酸时,接触室中主要反应为:2SO2(g)+O2(g) =2SO3(g) ΔH=-196.6 kJ·mol-1 , SO2、NOx也是大气主要污染物,NOx可与NH3混合,通过选择性催化剂高温脱除,SO2可通过碱液吸收去除。下列关于SO2、SO3、NH3、NH
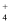 说法中正确的是( ) 说法中正确的是( )
A . SO2水溶液能导电,SO2是电解质
B . NH
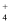 中含有配位键
C . SO3中硫原子轨道杂化类型为sp3
D . NH3为非极性分子 中含有配位键
C . SO3中硫原子轨道杂化类型为sp3
D . NH3为非极性分子
|
|
| 5. 单选题 | |
|
SO2、NOx是重要化工原料,可用于硫酸、硝酸的生产。工业制硫酸时,接触室中主要反应为:2SO2(g)+O2(g) =2SO3(g) ΔH=-196.6 kJ·mol-1 , SO2、NOx也是大气主要污染物,NOx可与NH3混合,通过选择性催化剂高温脱除,SO2可通过碱液吸收去除。在指定条件下,下列选项所示的物质间转化能实现的是( )
A . NO(g)
 HNO3(aq)
B . SO2(g) HNO3(aq)
B . SO2(g) H2SO4(aq)
C . SO2 H2SO4(aq)
C . SO2 NH4HSO3(aq)
D . NOx NH4HSO3(aq)
D . NOx N2(g) N2(g)
|
|
| 6. 单选题 | |
|
SO2、NOx是重要化工原料,可用于硫酸、硝酸的生产。工业制硫酸时,接触室中主要反应为:2SO2(g)+O2(g) =2SO3(g) ΔH=-196.6 kJ·mol-1 , SO2、NOx也是大气主要污染物,NOx可与NH3混合,通过选择性催化剂高温脱除,SO2可通过碱液吸收去除。对于反应 2SO2(g)+O2(g)
 2SO3(g),下列说法正确的是( ) 2SO3(g),下列说法正确的是( )
A . 该反应ΔH<0 ΔS>0
B . 2 mol SO2(g)和1 mol O2(g)所含键能总和比2 mol SO3(g)所含键能小
C . 反应在高温、催化剂条件下进行可提高SO2的平衡转化率
D . 该反应中每生成22.4 L SO3转移电子的数目约等于2×6.02×1023
|
|
| 7. 单选题 | |
|
卤族元素包括F、Cl、Br、I等元素。下列说法正确的是( )
A . 电负性:F<Cl<Br<I
B . 键能:HF<HBr
C . 失电子能力:Cl-<Br-<I-
D . 键的极性:Cl-I<Br-I
|
|
| 8. 单选题 | |
|
用低品铜矿(主要含CuS、FeO)制备Cu2O的一种工艺流程如下:
下列说法正确的是( )
A . “酸浸”过程中CuS发生反应的离子方程式为: S2-+MnO2+4H+
 Mn2++S+2H2O
B . “酸浸”所得溶液中的阳离子主要有H+、Mn2+、Cu2+和Fe2+
C . 1个Cu2O晶胞(如图)中含4个氧原子
D . 水合肼浓度过大,Cu2O产率下降,可能的原因是Cu2O进一步被还原成单质铜 Mn2++S+2H2O
B . “酸浸”所得溶液中的阳离子主要有H+、Mn2+、Cu2+和Fe2+
C . 1个Cu2O晶胞(如图)中含4个氧原子
D . 水合肼浓度过大,Cu2O产率下降,可能的原因是Cu2O进一步被还原成单质铜
|
|
| 9. 单选题 | |
|
科学家发明了如图所示的新型Zn—CO2水介质电池,电极为金属锌和选择性催化材料,放电时,CO2被转化为储氢物质甲酸等。下列说法正确的是( )
A . 放电时,负极反应式为:Zn+2e-+4OH-=Zn(OH)
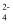 B . 放电时,1 mol CO2完全转化为HCOOH,理论上转移4 mol电子
C . 充电时,正极溶液中OH−浓度升高
D . 充电时,电池总反应为:2Zn(OH)
B . 放电时,1 mol CO2完全转化为HCOOH,理论上转移4 mol电子
C . 充电时,正极溶液中OH−浓度升高
D . 充电时,电池总反应为:2Zn(OH)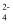  2Zn+O2↑+4OH-+2H2O 2Zn+O2↑+4OH-+2H2O
|
|
| 10. 单选题 | |
|
在催化剂作用下,HCOOH分解生成CO2和H2可能的反应机理如图所示。下列说法错误的是( )
A . 若用HCOOD催化释氢,反应除生成CO2外,还生成HD
B . 第一步转化N与H间形成配位键
C . 若用HCOOK溶液代替HCOOH释氢的速率加快
D . 若用HCOOK溶液代替HCOOH最终所得气体中H2的纯度会降低
|
|
高中化学 试卷推荐
- 四川省遂宁市高中2016-2017学年高一下学期化学期末考试试卷
- 高中化学鲁科版(2019)选择性必修2 第1章第2节 原子结构与元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.1金属矿物的开发利用课时作业
- 2015-2016学年河北省邢台市高一上学期期末化学试卷
- 内蒙古呼和浩特市2017-2018学年高考理综-化学二模考试试卷
- 山东省菏泽市2016-2017学年高一上学期化学期末考试试卷(B卷)
- 北京市西城区2017-2018学年高考理综-化学二模考试试卷
- 2015年河南河北山西三省高考化学考前模拟试卷
- 浙江省嘉兴市2018-2019学年高一下学期化学期末考试试卷
- 2015-2016学年吉林省延边州汪清六中高二下学期期中化学试卷
- 河南省郑州市2016-2017学年高一下学期化学期末考试试卷
- 江西省上饶市横峰中学2020年高考化学模拟试卷
最近更新







