山东省临沂市兰陵县2021-2022学年高二上学期期中考试化学试题
山东省临沂市兰陵县2021-2022学年高二上学期期中考试化学试题
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
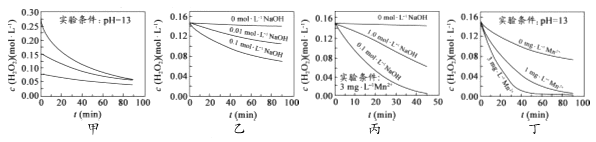
H2O2分解速率受多种因素影响.实验测得 70℃时不同条件下H2O2浓度随时间的变化如图所示.下列说法正确的是( )
A . 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B . 图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C . 图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快
D . 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
|
|
| 2. 单选题 | |
|
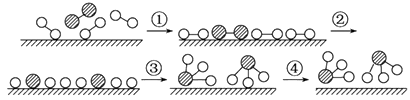
化学家格哈德·埃特尔证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如下:
下列关于合成氨反应的叙述中错误的是( )
A . 该过程表明,在化学反应中存在化学键的断裂与形成
B . 在催化剂的作用下,反应物的化学键变得容易断裂
C . 过程②需吸收能量,过程③则放出能量
D . 常温下该反应难以进行,是因为常温下生成物的化学键难以形成
|
|
| 3. 单选题 | |
|
在一定温度下的恒容容器中,加入少量A发生反应
 。当下列物理量不再发生变化,可以判断达到化学平衡的是( ) 。当下列物理量不再发生变化,可以判断达到化学平衡的是( )①B的体积分数;②混合气体的压强;③混合气体的总质量;④混合气体的平均相对分子质量;⑤混合气体的密度
A . 仅②③
B . 仅②③⑤
C . 仅①④⑤
D . ①②③④⑤
|
|
| 4. 单选题 | |
|
下列说法或表示方法正确的是( )
A . 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的能量多
B . 由C(石墨)→C(金刚石)ΔH= +1.9kJ•mol-1可知,金刚石比石墨稳定
C . 在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,则H2燃烧热的化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ•mol-1
D . 在稀溶液中,H+(aq)+OH-(aq)═H2O(l) ΔH= -57.3kJ•mol-1 , 若将含0.5mol H2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ
|
|
| 5. 单选题 | |
|
为了探索外界条件对反应aX(g)+bY(g)⇌cZ(g)的影响,以X和Y物质的量比为a:b开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。以下判断正确的是( )
A . ΔH>0,a+b>c
B . ΔH>0,a+b<c
C . ΔH<0,a+b>c
D . ΔH<0,a+b<c
|
|
| 6. 单选题 | |
|
某温度下,发生反应N2(g)+3H2(g)
 2NH3(g) ΔH=-92.4 kJ·mol-1 , N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是( ) 2NH3(g) ΔH=-92.4 kJ·mol-1 , N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是( )
A . 将1 mol N2和3 mol H2置于1L密闭容器中发生反应,放出的热量为92.4 kJ
B . 平衡状态由A到B时,平衡常数K(A)<K(B)
C . 增大压强,H2的平衡转化率增大
D . 降低温度,平衡常数K减小
|
|
| 7. 单选题 | |||||||||
|
已知25℃时有关弱酸的电离平衡常数如下:
则下列有关说法正确的是( )
A . pH相同的三种溶液,物质的量浓度的关系为c(CH3COOH)>c(H2CO3)>c(HCN)
B . 1 mol/L的醋酸溶液加水稀释,其中醋酸的电离程度先增大后减小
C . NaCN溶液中通入少量CO2发生的化学反应为
 D . 稀释HCN溶液过程中,
D . 稀释HCN溶液过程中, 减小 减小
|
|||||||||
| 8. 单选题 | |
|
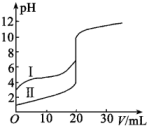
室温下,用
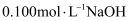 溶液分别滴定 溶液分别滴定 的盐酸和醋酸,滴定曲线如图所示,下列说法错误的是( ) 的盐酸和醋酸,滴定曲线如图所示,下列说法错误的是( )
A . Ⅱ表示的是滴定盐酸的曲线
B .
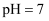 时,滴定醋酸溶液消耗的 时,滴定醋酸溶液消耗的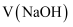 等于 等于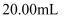 C . 滴定醋酸溶液过程中,当消耗
C . 滴定醋酸溶液过程中,当消耗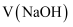 等于 等于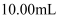 时,此时溶液中 时,此时溶液中 D . 滴定醋酸溶液、盐酸时,均可选择酚酞溶液作为指示剂
D . 滴定醋酸溶液、盐酸时,均可选择酚酞溶液作为指示剂
|
|
| 9. 单选题 | |
|
0.1mol·L-1氨水10 mL,加蒸馏水稀释到1 L后,下列变化正确的是( )
①电离程度增大 ②c(NH3·H2O)增大 ③
A . ①②③
B . ①③⑤
C . ①③⑥
D . ②④⑥
|
|
| 10. 单选题 | |
|
已知碘酸( HIO3)为弱酸,以下事实不能说明碘酸是弱酸的是( )
A . 常温下,1 L浓度为0.1 mol· L-1的HIO3溶液的pH > 1
B . 等体积、等物质的量浓度的碘酸溶液和盐酸,与同浓度、同体积的小苏打溶液反应,开始时加入盐酸的溶液中放出气体的速率快,加入碘酸溶液的较慢
C . 用HIO3溶液进行导电性实验,灯泡很暗
D . 取等体积、等pH的盐酸和碘酸溶液,分别用一定浓度的NaOH溶液进行滴定,恰好反应完全时,后者消耗碱液的体积较大
|
|
最近更新









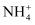 数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥
数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥ 增大
增大


