第7节 元素符号表示的量 知识点题库
某化合物的化学式为R2O3 , 它的相对分子质量是160,则R的相对原子质量是( )
A . 56
B . 112
C . 114
D . 72
某物质由碳、氢、氧三种元素组成,图甲是该物质的元素质量分数圆饼图,图乙为该物质的分子结构模型图。据图分析,下列关于该物质的说法正确的是( )

A . 元素A、B、C分别表示碳、氢、氧
B . 该物质化学式可表示为CH6O2
C . 该物质相对分子质量为105
D . 分子中碳、氢、氧三种原子个数比为2:6:1
若碳原子的质量为a克,A原子的质量为b克,则A原子的相对原子质量为( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题。某化学研究小组的同学欲对某种塑料袋的组成进行分析探究(资料显示该塑料只含C、H两种元素),他们设计了如图所示的实验装置,使该塑料试样在纯氧中燃烧,观察实验现象,分析有关数据,推算元素含量。
-
(1) 仪器E中的现象。仪器E中所发生的反应化学方程式为。
-
(2) 仪器B的作用是。
-
(3) 若仪器C的玻璃管中放入的塑料试样质量为Wg,塑料试样充分燃烧后,若仪器D增重ag,则Wg该塑料试样中含氢元素的质量为g(计算结果可为分数形式)。
-
(4) 若装置中没有连接仪器B,将使该塑料试样中氢元素的质量测算结果(填“偏小”“偏大”或“无影响”中之一)。
-
(5) 碱石灰的成分是氢氧化钠和氧化钙,则装置连接正确时F装置的作用是。
央视曾曝光河南孟州等地养猪场采用违禁动物药品瘦肉精;瘦肉精通常是指盐酸克伦特罗,化学式为:C12H18Cl2N2O,结构简式如右图所示。盐酸克伦特罗是一种肾上腺类神经兴奋剂,属于非蛋白质激素,耐热,使用后会在猪体组织中形成残留,尤其是在猪的肝脏等内脏器官残留较高,食用后直接危害人体健康。其主要危害是:出现肌肉振颤、心慌、战栗、头疼、恶心、呕吐等症状,特别是对高血压、心脏病、甲亢和前列腺肥大等疾病患者危害更大,严重的可导致死亡。目前全球136个国家和地区都规定肉品不得检出瘦肉精。根据上述材料分析计算下列问题:

-
(1) 酸克伦特罗的结构简式是(选填“符号”或“模型”)
-
(2) 每个盐酸克伦特罗分子含有 个原子;
-
(3) 盐酸克伦特罗含有氮元素,试计算其氮元素的质量分数(列式计算,精确到0.1%)。
相对原子质量是一个比值.假设一个C-12原子质量的1/12为Mkg,以此为标准时,氧原子的相对原子质量是16。若以原子质量为2Mkg的某种原子作为标准,则氧原子的相对原子质量是( )
A . 8
B . 16
C . 32
D . 64
某物质的化学式为HnRO2n-1,他的相对分子质量为M,则R的相对原子质量为,R元素的化合价为。
上海医药商业行业协会发布防治甲型H1N1流感消毒剂中有过氧乙酸(C2H4O3).如图为某市出售的过氧乙酸标签上的部分文字说明,请回答:

-
(1) 一瓶这种溶液中含过氧乙酸的质量是 g.
-
(2) 过氧乙酸中碳、氢、氧元素的质量比为
-
(3) 过氧乙酸受热易分解,放出氧气并生成醋酸(C2H4O2),其受热分解的化学方程式为
我国科学家屠呦呦发现的青蒿素(化学式:C15H22O5),是一种用于治疗疟疾的药物,挽救了全球数百万人的生命,因而获得2015年诺贝尔生理学或医学奖。磺胺(化学式为C6H8N2O2S)是青蒿素发现之前最热门的抗疟药物之一。回答下列问题。
-
(1) 一个青蒿素分子中含有个原子。
-
(2) 青蒿素中的氢元素与氧元素的质量比是。
-
(3) 14.1克青蒿素中含有碳元素的质量和多少克磺胺中含有碳元素的质量相等?
科技人员成功研制出一种新型催化剂,可将二氧化碳转化成液体燃料,反应的微观示意图如下,有关该反应的说法正确的是( )

A . 该反应属于化合反应
B . 反应前碳元素的化合价为+2价
C . 生成物的化学式可用C2H2O表示
D . 参加反应的两物质的质量比为1:1
奥司他韦(C16H28N2O4)可抑制流感病毒在人体内的传播,起到治疗流行性感冒的作用。下列对奥司他韦的说法不正确的是( )
A . 从量的角度看:氢元素的质量分数约为20.5%
B . 从组成角度看:由碳、氢、氮、氧四种元素组成
C . 从构成角度看:每个奥司他韦分子是由50个原子构成
D . 从结构角度看:分子中碳、氢、氮、氧原子个数比为8:14:1:2
测得人尿中氮元素的质量分数为0.93%,如果这些氮都以尿素[CO(NH2)2]的形式存在,则人尿中尿素的质量分数为( )
A . 0.2%
B . 1%
C . 2%
D . 3%
A、B两种元素的相对原子质量之比是7:2,它们组成的一种化合物中,两种元素的质量之比是7∶3,则该化合物的化学式为( )
A . AB
B . A2B3
C . A3B2
D . A3B4
利巴韦林(化学式C8H12N4O5)是一种抗病毒的药物,
只能够治疗腮腺炎、水痘等病毒性感染的疾病。请计算:
-
(1) 利巴韦林分子中含有种原子;
-
(2) 利巴韦林的相对分子质量是;
-
(3) 122克利巴韦林中含氢元素多少克?(写出计算过程)
科学兴趣小组利用如图装置对FeSO4·nH2O晶体中的结晶水的含量进行测定(铁架台等己省略)。已知:①FeSO4和FeSO4·nH2O加热时易被空气氧化;②FeSO4·nH2O 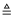 FeSO4+nH2O。实验步骤如下:
FeSO4+nH2O。实验步骤如下:
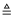 FeSO4+nH2O。实验步骤如下:
FeSO4+nH2O。实验步骤如下:


请回答:
-
(1) 步骤Ⅰ打开K1导入二氧化碳气体,排尽装置中的空气,其目的是 。
-
(2) 步骤Ⅳ中的操作乙是通二氧化碳直至C装置冷却至室温,则操作甲指的是。
-
(3) 有同学建议,为加快产生CO2的速率,可将A中装置中盐酸浓度增大、石灰石磨成粉状。制取气体时反应速度是否越快越好?其理由是。
-
(4) 步骤Ⅵ称量,若晶体FeSO4·nH2O质量为m,反应前后C装置质量减少了m1 , D装置
质量增加了m2 , 则此晶体中的结晶水的百分含量为。(用字母表示)
茶叶中含有茶氨酸(化学式为C7H14O3N2),它有降低血压、提高记忆力、保护神经细胞、减肥等效果。下列有关它的说法中,正确的是( )
A . 茶氨酸由C,H,O、N四种原子直接组成
B . 茶氨酸的相对分子质量为174g
C . 茶氨酸中碳、氮元素的质量比为7:2
D . 茶氨酸中氧元素质量分数的计算  ×100%
×100%
 ×100%
×100%
小明在学习了元素和物质的知识后,进行了梳理,其中正确的是( )
A . 铁元素的质量分数由高到低:FeO、Fe2O3、FeS
B . 钙的化合物在水中的溶解性由大到小:CaCl2、CaCO3、Ca(OH)2
C . 氮元素的化合价由高到低:HNO3、NH3、NO
D . 空气中主要气体的体积分数由大到小:O2、N2、CO2
维生素C,化学式为C6H8O6 , 在人体中具有维持免疫、促进非血红素铁吸收、抗氧化等功能,并起到美白、淡斑的功效。
-
(1) 维生素C的相对分子质量为;
-
(2) 维生素C中氧元素的质量分数为(用百分数表示,保留一位小数);
-
(3) 计算多少克维C中所含碳元素的质量与66g二氧化碳中所含碳元素质量相等?
某物质的分子式为HnRO2n-1 , 它的相对分子质量是m,则R元素的相对原子质量是。
2022年“3·15”晚会曝光了老坛酸菜,号称老坛工艺,足时发酵,实则在土坑腌制而来,除了制作过程卫生不达标,添加的防腐剂也是超标的,其防腐剂的主要成分是焦亚硫酸钠(Na2S2O5),是一种无机化合物,为白色或黄色结晶,带有强烈的刺激性气味,溶于水,水溶液呈酸性,久置空气中会被氧化成硫酸钠。
-
(1) 焦亚硫酸钠(Na2S2O5)的相对分子质量是。
-
(2) 焦亚硫酸钠(Na2S2O5)溶于水呈酸性体现其性质。(填“物理”或“化学”)
-
(3) 请将该防腐剂久置空气中发生的化学反应方程式补充完整。
2Na2S2O5 + O2 = Na2SO4 + SO2
-
(4) 防腐剂超标会破坏人体消化道菌群,如图是肠道益生菌——双歧杆菌,有关说法正确的是。

①双歧杆菌属于原核生物,没有成型的细胞核
②双歧杆菌是单细胞
③双歧杆菌可以用光学显微镜观察
④从生物成分分析,双歧杆菌属于分解者
最近更新



