第三单元 物质构成的奥秘 知识点题库
下列说法正确的是( )
A . 所有原子核都由质子、中子构成
B . 花香四溢主要是分子之间有间隔
C . 保持水化学性质的微粒是氢分子和氧原子
D . 原子是化学变化中的最小粒子
-
(1) 科学家在100℃合成了物质X(分子模型如图),其中
 代表碳原子,
代表碳原子,  代表氯原子。请从宏观和微观两个层面描述物质X的组成和构成,
代表氯原子。请从宏观和微观两个层面描述物质X的组成和构成, 
宏观:;微观:
-
(2) 锶元素的粒子结构示意图和在元素周期表中显示的信息如下图所示。
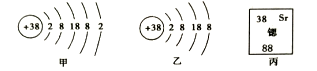
①锶元素的原子序数为,原子核内中子数为
②图乙所表示的粒子的化学符号是
“宏观-微观-符号”三重表征是化学视角认识物质及其变化的方法。
-
(1) 右图是两种元素在元素周期表中的信息以及氟原子的原子结构示意图,Y是,X=。氟原子在化学反应中容易形成(写离子符号)。

-
(2) 下图是某密闭容器中氢气在氧气中燃烧的微观示意图,根据图示回答下列问题。
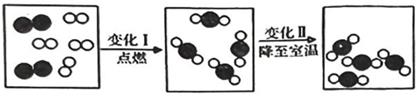
①变化Ⅰ前后,没有发生改变的粒子是(填粒子名称);变化Ⅰ和变化Ⅱ的本质区别是。
②上述变化过程中共有种元素,共有种物质。
5G商用加速推出,“中国芯”崛起,“中国创造”绽放异彩!芯片的主要成分是纯度极高的硅,如图为硅在元素周期表中的部分信息,下列说法错误的是()

A . 硅元素属于金属元素
B . 硅原子的核电荷数是14
C . 硅原子的核外电子数为14
D . 硅的相对原子质量为28.09
中国科学院院士张青莲教授主持测定了钢等元素的相对原子质量的新值,为相对原子质量的测定做出了卓越贡献。铟元素(In)的部分信息如图,下列有关铟的说法正确的是( )
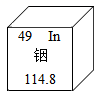
A . 铟属于非金属元素
B . 铟原子的中子数为49
C . 铟原子核内有49个质子
D . 铟的相对原子质量为114.8g
如图为镍的原子结构示意图,关于该原子的叙述错误的是( )

A . 核电荷数为28
B . 核外有4个电子层
C . 质子数大于核外电子数
D . 易失去2个电子
生活中常接触到“加碘食盐”、“富硒茶叶”、“含氟牙膏”等用品,这里的碘、硒、氟指的是( )
A . 物质
B . 元素
C . 分子
D . 原子
下列符号既能表示一种元素,又能表示一个原子,还表示一种物质的是( )
A . O2
B . 2He
C . Mg2+
D . Fe
用化学符号表示:
-
(1) 磷元素;
-
(2) 2个钠原子;
-
(3) 锌离子;
-
(4) n个硫酸根离子;
-
(5) 海水中含量最多的金属元素。
分析推理是化学学习过程中的常用方法,下列推理正确的是( )
A . 可燃物燃烧时温度需要达到着火点,所以可燃物的温度达到着火点一定能燃烧
B . 有氧气参加的反应一定是氧化反应,所以发生氧化反应一定有氧气参加
C . 元素的种类由质子数决定,则质子数相同的微粒一定属于同种元素
D . 化合物是含有不同元素的纯净物,所以含有不同种元素的纯净物一定是化合物
实验是科学探究的重要途径,请根据下图实验回答相关问题。

-
(1) 实验甲中,铁丝没有点燃,可能的原因是氧气,若铁丝燃烧,发生反应的化学方程式。
-
(2) 根据实验乙现象得到的实验结论是。
-
(3) 根据实验丙现象,说明二氧化碳的化学性质是。
如下图所示,甲、乙、丙、丁是四种粒子的结构示意图。下列说法错误的是( )

A . 乙、丁具有相似的化学性质
B . 甲、乙属于同种元素
C . 乙表示阴离子
D . 丁中x=8
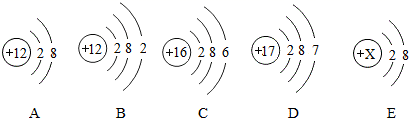
根据下列粒子结构示意图,回答问题。
-
(1) 如图A、B、C、D四种粒子共表示种元素。
-
(2) D原子在化学反应中易(填“得到”或“失去”)电子。
-
(3) 在A,B,C,D四种粒子中具有稳定结构的是。
-
(4) E粒子带1个单位正电荷,则X=。
现有①氧气②氖气③二氧化碳④氯化钠⑤二氧化硫五种物质,选择适当序号填空。
-
(1) 可用于制作霓虹灯的气体是。
-
(2) 能使澄清石灰水变浑浊的气体是。
-
(3) 通常具有助燃性的气体是。
-
(4) 由离子构成的物质是。
-
(5) 随着工业的发展,排放到空气中的有害物质是。
从分子的角度分析,下列对事实或现象的解释错误的是( )
| 事实或现象 | 解释 | |
| A | 香味扑鼻 | 分子在不断地运动 |
| B | 气体能被压缩 | 分子之间有间隔 |
| C | 热胀冷缩 | 分子的大小随温度的改变而改变 |
| D | 过氧化氢分解生成水和氧气 | 分子可以分成原子原子再重新构成新分子 |
A . A
B . B
C . C
D . D
“三星堆遗址”被称为20世纪人类最伟大的考古发现之一。
-
(1) 下列三星堆遗址出土的文物中,所用材料主要为金属材料的是(填字母序号)。

-
(2) 出土的黄金面具仍金光灿灿,而青铜神树已锈迹斑斑,这说明金的活动性比铜(选填“强”或“弱”)。
-
(3) 铜制品长期暴露在空气中能与空气中的O2、H2O和化合生成铜锈(主要成分是Cu(OH)2CO3)。
-
(4) 考古专家利用铅元素示踪法探求三星堆青铜器的矿源地。其中涉及到的一种铅原子的原子核内有82个质子和126个中子,该原子的核外电子数为。
根据下列粒子结构示意图,回答问题。

-
(1) 若A,E属于同种元素,则x=。
-
(2) 若E粒子带一个单位正电荷,E粒子符号为,E元素位于元素周期表中第周期。
-
(3) D粒子与B粒子能形成由离子构成的化合物,该物质的化学式为。
“北斗”三号卫星导航系统应用了星载氢原子钟和铷原子钟。铷在元素周期表中的信息如图所示,下列有关铷的说法不正确的是( )

A . 属于金属元素
B . 铷原子核外电了数为37
C . 原子核内有37个质子
D . 相对原子质量为85.47g
从微观的角度解释下列现象。
-
(1) 蔗糖在热水比在冷水中溶解的快。
-
(2) K2SO4溶液是无色的,而KMnO4溶液是紫色的。
“南风之时兮,可以阜吾民之财兮”这首上古歌谣说的是夏季南风一吹,盐池隔宿成盐,带来巨大财富。
-
(1) 食盐是由(填“分子”、“原子”或“离子”)构成。
-
(2) 从盐水中得到食盐,需进行的操作是。能反映水在该操作中发生变化的微观示意图是(填标号,“
 ”表示氧原子,“
”表示氧原子,“ ”表示氢原子)
”表示氢原子)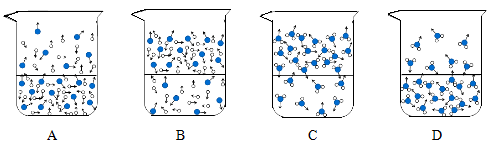
-
(3) 劳动致富过程中,用溶质质量分数为16%的NaCl溶液来选种。若配制5kg这种溶液,需要NaCl的质量是根据NaCl溶解度曲线判断,此溶液(填“是”或“不是”)20℃时NaCl的饱和溶液。

-
(4) 写出氯化钠在生理健康上的一种用途。
最近更新



