课题2 原子的结构 知识点题库
-
(1) 化学用语是国际通用语言.请用化学用语填空:
①氮元素;②3个甲烷分子;③氢氧根离子;④SO2中硫元素的化合价为+4;
-
(2)
如图是两种粒子的结构示意图,请回答下列问题:

①在化学反应中容易失去电子的是(填序号);
②图中两种元素组成的化合物的化学式是.
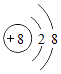 B .
B . 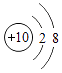 C .
C .  D .
D . 

-
(1) 在A、B、C、D四个结构示意图中,达到相对稳定结构的是,属于同种元素的是,属于离子的是,在化学反应中容易得电子的是.
-
(2) 对图E中提供的信息理解不正确的是A . 属于非金属元素 B . 质子数为20 C . 元素符号为Ca D . 相对原子质量为40.08.
-
(1) 下图是镓在元素周期表中的信息以及原子结构示意图。

镓的相对原子质量为;下列原子结构示意图所对应的元素与镓元素的化学性质相似的是(填序号);
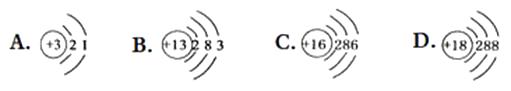
-
(2) 氮化镓(GaN)中镓元素的化合价为+3价,则氮元素的化合价为价 ;
-
(3) 传统制备氮化镓的化学原理是:GaCl3+NH3
 GaN+3X ,其中X的化学式为。
GaN+3X ,其中X的化学式为。

-
(1) 中国工程院院士袁隆平宣布了一项重大突破成果——水稻亲本去镉技术。如图A所示为元素周期表中镉元素的信息示意图,该元素的相对原子质量为。
-
(2) B,C,D,E中化学性质相似的微粒是(填字母)。
-
(3) C,E两种元素组成的化合物的化学式为。


-
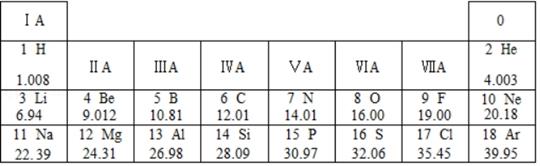
(1) 不同种元素最本质的区别是_____(填字母)。A . 质子数不同 B . 中子数不同 C . 电子数不同 D . 相对原子质量不同
-
(2) 表中第11号元素和第17号元素位于同一周期的原因是(填字母):第9号元素和第17号元素位于同一族的原因是由于(填字母)
A.质子数相同B,中子数相同C.原子的电子层数相同D.最外层电子数相同
-
(3) 有一种原子内有20个中子,核外电子有19个,它的相对原子质量是。
-
(4) 在元素周期表中,同一周期(横行)中的元素,除0族元素(稀有气体元素)外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强,则原子半径,钠镁(选填“>”、“=”或“<”,下同);原子得电子能力:硫氯。
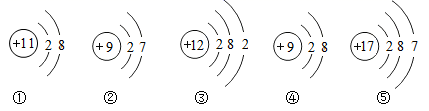
-
(1) 以上示意图中,共有种元素。
-
(2) 在化学反应中易失电子的粒子是。(填序号,下同)
-
(3) 具有相对稳定结构的粒子是。
-
(4) 化学性质相似的原子是。(填一组)
| 选项 | 事实 | 解释 |
| A | 用水银温度计测量温度 | 原子间的间隔随温度的升降而增减 |
| B | 过氧化氢溶液是混合物 | 溶液中所含有的分子的种类不同 |
| C | 盐酸和硫酸有相似的化学性质 | 溶液中都含有相同的氢离子 |
| D | 氯化钠溶解于水后“消失”不见了 | 氯化钠分子是不断运动的 |
-
(1) 我国科学家张青莲教授主持测定的铟等多种元素的相对原子质量已成为国际标准。铟是银白色并略带淡蓝色的金属,质地非常软,金属铟主要用于制造低熔合金、轴承合金、半导体、电光源等的原料。请回答下列问题:

镓可以和铟合成液态金属,形成一种固溶合金,有望用于帮助修复人类切断的神经,该变化属于(填“物理”或“化学”)变化。铟原子的相对原子质量是,铟元素的化学性质与铝元素的化学性质相似,原因是;粉末状的铟可与水加热缓慢的作用,生成一种碱并放出一种可燃性气体,写出铟与水反应的化学方程式。
-
(2) 石墨烯一层层叠起来就是石墨,1mm厚的石墨大约包含300万层石墨烯。实际上石墨烯本来就存在于自然界中,只是难以剥离出单层结构。石墨烯的制备方法之一是低温扩张法,把石墨粉、钠、液氨按照一定比例混合,在特定装置中进行剥离,然后用去离子水清洗至中性,再放入烘箱内烘干即得石墨烯。制得的石墨烯的比表面积越大,质量越好。科学家测定了烘干温度对制得的石墨烯的比表面积的影响如图1所示。

石墨烯具有强度高、透光率高、导电性强、韧性好的特点,是构成其它新型碳材料的基本组成单元,如图2所示。将含有石墨烯和碳纳米管两种纳米材料的水溶液低温环境下冻干,去除水分、保留骨架,制造出的一种超轻固体材料被称为“全碳气凝胶”,是迄今为止世界上最轻的材料。“全碳气凝胶”还是吸油能力最强的材料之一,吸收量可高达自身质量的900倍。

随着石墨烯制备方法的研发,石墨烯必将广泛应用到各领域中。依据文章内容回答下列问题。
①石墨烯由(填“原子”或“分子”)构成;
②“1mm厚的石墨大约包含300万层石墨烯”,说明构成物质的微粒;
③由图1可知:制备石墨烯时最佳的烘千温度约为℃;
④下列说法正确的是(填字母)
A.自然界中不存在石墨烯
B.石墨烯可用于制作新能源电池,主要利用石墨烯的导电性
C.碳纳米管具有可燃性,充分燃烧生成二氧化碳
D.“全碳气凝胶”可处理海上石油泄漏
-
(1) 构成氧气的粒子是(填“氧原子”或“氧分子”)。
-
(2) 下图是钠、镁、氯、溴四种原子的结构示意图。

①镁原子的结构示意图中x的数值为。
②溴原子在化学反应中容易电子(填“得到”或“失去”);溴化钠是由钠元素和溴元素组成的化合物,溴化钠的化学式为。
-
(3) 下图为某化学反应的微观示意图。
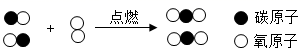
根据图示写出反应的化学方程式。
 ,一根氧烛大约可以供100个人呼吸1小时,下列说法错误的是( )
,一根氧烛大约可以供100个人呼吸1小时,下列说法错误的是( )
 C . 氧烛分解产生的高纯氧气不仅可以供给呼吸,还可以用作高能燃料
D . 从实验室制O2的原理推测氧烛中的催化剂可能为MnO2
C . 氧烛分解产生的高纯氧气不仅可以供给呼吸,还可以用作高能燃料
D . 从实验室制O2的原理推测氧烛中的催化剂可能为MnO2




