课题2 原子的结构 知识点题库
元素周期表是学习和研究化学的重要工具.认真分析信息,回答:

-
(1) 地壳中含量最多的金属元素的符号是
-
(2)
 表示的是 (填名称)
表示的是 (填名称)
-
(3) 由1、8、12号元素组成化合物的化学式
如图是四种粒子的结构示意图,说法正确的是( )

A . ①和③属于同种元素
B . ①和③表示的元素是金属元素
C . ①和③化学性质相似
D . ②和④表示的是阳离子
1991年,我国著名化学家张青莲教授与另一位科学家合作,测定了(In)铟元素的相对原子质量新值.铟原子的核电荷数为49,相对原子质量为115.铟原子的核外电子数为( )
A . 164
B . 115
C . 66
D . 49
今年五月,广州对餐饮食品抽检,45%的大米被检出重金属辐超标.下图A为周期表中的镉元素,图B为镉原子结构示意图,下列说法正确的是( )

A . 镉原子的相对原子质量为112.4g
B . 符号“Cd”可以表示金属镉、一个镉原子
C . 金属镉能使蛋白质失去生理活性
D . 镉位于周期表的第五周期,图B中X=4
在微观、宏观和符号之间建立联系是化学学科的特点。
-
(1) 在O2、CO2、SO2三种微粒中,都含有;
-
(2) 在H2、H2O、H2SO4三种物质中,都含有;
-
(3) 在Mg2+、2C、NO2三种符号中,兼有宏观、微观意义的是;
下列微粒结构示意图中,表示阳离子的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
过氧化钠(化学式为Na2O2)在工业上常用作漂白剂、消毒剂、氧化剂等。某化学小组将少量过氧化钠粉末加入盛水的试管中,看到有大量气泡产生。
(提出问题)过氧化钠与水反应生成的气体是什么物质?
作出猜想)猜想I:生成H2;猜想Ⅱ:生成O2;猜想Ⅲ:生成CO2。
-
(1) 大家一致认为猜想Ⅲ错误,理由是。
-
(2) (实验验证)
实验结论
实验现象
实验结论
用试管收集生成的气体,堵住试管口,移近酒精灯火焰,点燃
无现象
用试管收集生成的气体,将带火星的木条伸入试管内
猜想Ⅱ成立
-
(3) (拓展延伸)
同学们经查阅资料得知,过氧化钠与水反应,除了产生气体,还有氢氧化钠生成,试写出该反应的文字表达式。
-
(4) 构成氢氧化钠的粒子是(填粒子符号)。
-
(5) 过氧化钠保存时应注意的问题是。
“见著知微,见微知著”是化学思维方法。
-
(1) 从宏观知微观。
①50mL水与50mL乙醇混合后,溶液体积小于100mL,微观解释为;
②气体X在氧气中燃烧生成氮气和水,X分子中一定含有的元素有(填符号)。
-
(2) 从微观知宏观。

①微粒A在化学反应中容易(填“得”或“失”)电子:微粒C的符号是。
②A-E五种微粒所含元素,对应单质化学性质最稳定的是(填单质化学式)。
③甲和乙在催化剂、高温高压条件下反应生成丙,三种物质微观结构示意图如图2所示,该反应的化学方程式:。
根据下列粒子结构示意图,回答下列问题:

-
(1) A,B,C,D所示粒子共表示种元素
 填数字
填数字  。
。
-
(2) C的粒子符号为。
-
(3) 若E中
 时,则该粒子属于
时,则该粒子属于  填“原子”或“离子”
填“原子”或“离子”  。
。
据报道,“火星快车”号探测器在火星大气层中发现一种二氧化碳分子,它的化学式为:  (元素符号左上角的数字代表该原子中的质子数和中子数之和).
(元素符号左上角的数字代表该原子中的质子数和中子数之和).
 (元素符号左上角的数字代表该原子中的质子数和中子数之和).
(元素符号左上角的数字代表该原子中的质子数和中子数之和).
-
(1)
 中的质子数是;中子数是;
中的质子数是;中子数是;
-
(2) 相同分子个数的
 和
和  ,所含氧元素的质量:前者后者(选填“大于”、“小于”或“等于”).
,所含氧元素的质量:前者后者(选填“大于”、“小于”或“等于”).
有六种粒子的结构示意图分别是:

-
(1) A,B,C,D,E,F中表示原子结构示意图的有种。
-
(2) 表示阳离子的粒子是(填序号),符号为
-
(3) 表示稀有气体元素的粒子是(填序号)。
锶元素的粒子结构示意图和在元素周期表中显示的信息如图所示,则下列说法错误的是( )

A . 图1所表示的粒子在化学反应中容易失去电子
B . 图2是锶离子结构示意图
C . 从图3中可以看出这种元素是金属元素
D . 该元素在化合物中通常显-2价
图中A、B分别是某微粒的结构示意图,回答下列问题:

-
(1) 若A表示某稀有气体元素的原子,则该元素的单质的化学式为。
-
(2) 若B表示某元素的原子,则y=,该元素的原子在化学反应中容易(填“失去”或“得到”)电子,形成(填离子符号)。
-
(3) 若A是阳离子的结构示意图,则x可能是下列中的(填字母序号)。
a.8 b.10 c. 11 d.12
-
(4) 若A中x=11,则A、B所表示的元素形成化合物的名称为。
-
(5) 决定元素化学性质的是。
如图为六种原子的结构示意图。

请回答下列问题:
-
(1) 图中六种元素之间的最本质区别是;
-
(2) 镁原子在化学反应中容易失去2个电子形成镁离子,镁离子的化学式为;氧化钠由钠离子和氧离子构成,氧化钠的化学式为。
-
(3) 从原子结构上分析,图中哪两组元素具有相似的化学性质(填元素符号)、。
-
(4) 在上述碘的原子结构示意图中,x=。
宏观和微观相结合是认识物质结构与性质的重要方法。
-
(1) 氧原子的结构示意图为
 ,硫原子的结构示意图为
,硫原子的结构示意图为  。
。 ①一个硫原子得到二个电子形成一种新粒子,该粒子的符号为。
②氧气和硫单质分别与氢气反应生成H2O和H2S。H2O、H2S中氧与硫元素的化合价均为-2价,从原子结构上分析它们化合价相同的原因是。
-
(2) Na2CO3溶液和H2SO4溶液反应的微观示意图如图1所示。该反应中实际参加反应的离子是(填离子符号)。


-
(3) 硫及其化合物的“化合价-物质类别”关系图如图2所示。物质X的化学式为。
宜昌磷矿资源丰富。已知一个磷原子核内含有15个质子,相对原子质量为31,则磷原子的核外电子数为( )
A . 8
B . 15
C . 16
D . 31
元素周期表是学习化学的重要工具,如图是元素周期表中的一部分,请回答下列问题:
|
第一 周期 |
1H |
2He |
||||||
|
第二 周期 |
3Li |
4Be |
5B |
6C |
7N |
8O |
9F |
10Ne |
|
第三 周期 |
11Na |
12Mg |
13Al |
① |
15P |
16S |
17Cl |
18Ar |
-
(1) 表中,①所示元素的名称
-
(2) X2- 与Ar的核外电子排布相同,则X的元素符号是,它处于元素周期表中的第周期。
-
(3) 元素周期表中同族和同周期元素的性质具有一定的相似性和变化规律,同族元素化学性质相似的原因是相同。
-
(4) 化学上用符号
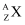 表示原子构成,其中X代表元素符号,Z表示原子核内质子数,A表示原子核内质子数与中子数之和。已知
表示原子构成,其中X代表元素符号,Z表示原子核内质子数,A表示原子核内质子数与中子数之和。已知  和
和  电子层排布完全相同,则下列关系正确的是
电子层排布完全相同,则下列关系正确的是 A b - a = d - c B a - n = c + m C a + n = c - m D b - n = d + m
某元素R的原子序数为m,能够形成Rn+ , 另一元素M能够形成与Rn+具有相同电子层结构的Ma- , 且则M原子的质子数是( )
A . m-n+a
B . m-n-a
C . m+n+a
D . m+n-a
锰(Mn)是维持人体正常生命活动所必须的微量元素,含锰化合物在生产、生活中也被广泛应用。结合图中所示信息,下列叙述正确的是( )

A . 锰原子核内有25个质子,一个锰原子的质量是54.94g
B . 锰原子核外有4个电子层,其化学性质由最内层电子数决定
C . 锰元素在元素周期表的位置一定不在第三周期
D . 锰离子的符号为Mn2-
如图1是元素周期表的一部分,据此回答下列问题。


-
(1) 质子数为2的氦元素
 应在表中(填“①”或“②”)位置。
应在表中(填“①”或“②”)位置。
-
(2) 地壳中含量最多的金属元素的原子序数为,该原子在化学反应中容易(“失去”或“得到”)个电子,表现出的化合价为。
-
(3) 元素周期表中每一个横行叫作一个周期,每一个纵行叫作一个族。以下说法正确的是____。A . 每一周期,各元素原子的电子层数相同 B . 每一周期,从左到右各元素原子的原子序数依次增加 C . 每一族,从上到下,各元素原子的电子层数依次增加
-
(4) 如图2是元素锶(Sr)的原子结构示意图,则x=,锶元素位于元素周期表第周期,写出第三周期中与锶化学性质相似的元素名称,锶元素与9号元素形成化合物的化学式是,名称为。
最近更新



