第3章 物质构成的奥秘 知识点题库
-
(1) 实验室用下列装置制取氧气。

①仪器a的名称是。
②用高锰酸钾制氧气。请将图A方框中气体发生装置补画完整;写出反应的符号表达式: ;任意写出一种可选用的装置组合(填字母代号);此组合还适用于另一反应原理制氧气,写出所选用物质的化学式。
③用制取的氧气做木炭在氧气中燃烧实验,红热的木炭插入过快,很难达到预期的实验效果,主要原因是什么?
-
(2) 常用的氮肥有尿素(CO[NH2]2)、硝酸铵、碳酸氢铵(NH4HCO3)等。
①碳酸氢铵的相对分子质量是。
②尿素中C、H、O、N四种元素的质量最简整数比是。
③农民用尿素给耕地的玉米施加氮肥,需要尿素120Kg尿素,若改用碳酸氢铵,要达到相同的肥效,则需要碳酸氢铵的质量是Kg。
④某化肥销售点提供的硝酸铵含氮为28.0%,则该化肥中硝酸铵的纯度是%。
-
(1) x的值为;
-
(2) 每个乳酸分子中碳、氢原子个数比为;
-
(3) 乳酸中碳、氢、氧元素的质量比为 ;
-
(4) 180g乳酸中含碳元素为g。
① 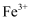 ②
②  ③
③  ④
④ 
-
(1) 草甘膦中磷元素的质量分数为。(精确到0.1%)
-
(2) 33.8g草甘膦中含有多少克磷元素?(写出计算步骤,精确到小数点后一位)
-
(1) 下列各种“水”中,属于纯净物的是______(填字母序号)。A . 矿泉水 B . 自来水 C . 蒸馏水 D . 渠江水
-
(2) 水通电可分解生成氢气和氧气。在图1所示的实验装置中,生成的氢气存在于玻璃管(填“a”或“b”)中。


-
(3) 水和天然气重整可以得到合成气,其反应的微观示意图如图2所示。
①在微观模型A、B、C、D中,表示水分子的是(填字母序号)。
②该反应的化学方程式为;生成物中C和D的质量比为。
-
(4) 为了保护西溪河流域的水质,下列做法合理的是______(填字母序号)。A . 大量开采地下水 B . 抑制水中所有动、植物的生长 C . 任意排放生活污水 D . 工业废水经过净化后再排放
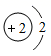 B .
B . 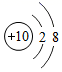 C .
C . 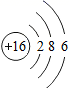 D .
D . 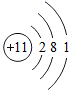

-
(1) 根据你对补钙产品的调查和已有的化学知识,这里的“钙”指(填字母序号)。
A 原子 B 分子 C 单质 D 元素
-
(2) CaCO3相对分子质量为。(写计算过程)
-
(3) CaCO3中钙、碳、氧元素的质量比为。(写计算过程)
-
(4) 计算每片高钙片中含钙元素的质量分数为。
-
(5) 某种牛奶中含Ca≥0.1g/100g.若改用该牛奶补钙(假设钙元素在体内完全被吸收),则每天至少喝盒牛奶才与该钙片的补钙效果相当?(假设每盒牛奶250g)

-
(1) 硝酸铵中氮元素和氧元素的质量比为(填最简比);
-
(2) 若硝酸铵中含有28g氮元素,则该硝酸铵的质量为g。
-
(1) 保持乙醇化学性质的微粒是;
-
(2) 构成氯化钠的微粒是。
-
(3) 分析过氧化氢
 )和过氧化钠(
)和过氧化钠(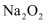 )中氧元素的化合价,写出过氧化钙的化学式为。
)中氧元素的化合价,写出过氧化钙的化学式为。
制造葡萄酒的原料葡萄中富含K、Ca、Na、Fe、Zn、Mg等元素。葡萄酒是以鲜葡萄或葡萄汁为原料,经酿酒酵母菌株将葡萄汁中的糖转化为酒精,同时生成了高级醇、酯类、单萜等香气化合物。葡萄酒香气主要受酿造菌种、酿造工艺、发酵条件等因素的影响。研究人员以发酵汁中残糖量为指标,研究不同种类的酿酒酵母的发酵动力(即发酵过程的速率),其测定结果如图1所示。
为防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动,葡萄酒酿制中还会适量添加SO2 , 其添加量对主要香气物质总量影响如图2所示。

葡萄在栽种过程中容易产生病虫害,可通过定期施肥、中和酸性土壤、喷洒农药等方法来增强葡萄抗病能力。若发病,可用硫酸铜配制农药波尔多液进行喷洒。
人们发现二氧化硫可以完成上面所有的需求。在酵母发酵的过程中,会产生一定量的二氧化硫,不过这个量比较少,还需要额外添加。这里添加的并不一定是二氧化硫气体,可以是它的其他化合物一各种亚硫酸盐、焦亚硫酸盐、亚硫酸氢盐等。这些物质能够实现跟二氧化硫有类似的功能。部分国家葡萄酒中二氧化硫含量上限标准如下表。
(1ppm=1mg·kg-1 , 1ppm=1mg·L-1)
国家 | 干红 | 甜酒 |
澳洲 | 250ppm | 350ppm |
中国 | 250ppm | 400ppm |
国际葡萄栽培与酿酒组织 | 300ppm | 450ppm |
国际食品添加剂联合专家委员会(JECFA)制定的二氧化硫安全摄入限是每天每公斤体重0.7mg。“安全摄入限”的意思是,不超过这个含量的二氧化硫,即使长期食用,也不会带来可见的危害。
-
(1) 在上述金属元素中,属于人体中微量元素的有。
-
(2) 配制农药波尔多液时,不宜用铁制容器,其原因是(用化学方程式表示)。
-
(3) 在酿造葡萄酒的过程中,加入一定量SO2的作用是。
-
(4) 对于一个体重62.5kg的成年人,每天二氧化硫安全摄入量是g。
-
(5) 下列说法正确的是____。A . SO2添加量在100mg·L-1时,高级醇总量最高 B . 酯类总量随着SO2添加量的增大而增大 C . 单萜总量随着SO2添加量的增加,先增大后减小 D . 氯化钠能代替二氧化硫添加到葡萄酒中 E . 在其他条件相同时,发酵动力最好的酿酒酵母菌株是LA-FR
-
(6) 红葡萄酒具有养颜,软化血管、抗癌等保健功能。红葡萄酒中含有花色苷,其化学式为C16H16O6 , 通过计算花色苷中质量分数最高的是元素。
-
(7) 葡萄酒的酿制最终转化为乙醇和二氧化碳,所以可认为葡萄酒本身应该呈微弱的酸性,其理由是(用化学方程式表示)。
-
(1) 2个磷原子;
-
(2) 3个钙离子;
-
(3) 空气中体积含量最多的物质;
-
(4) 醋酸。




