8.4 常用的盐 知识点题库
请回答下列问题:
(1)用化学用语表示:干冰常用于人工降雨,干冰中的“冰”是指 ;纯碱在工业中常用于制玻璃,纯碱中的“碱”是指 ;食盐常用作调味品,食盐中的“盐”是指 。
(2)下列微粒的结构示意图能表示镁原子的是(填序号,下同) 。
(3)根据元素的原子结构示意图,可以直接获得的信息是 。
| A.核电荷 |
| B.相对原子质量 |
| C.电子层数 |
| D.最外层电子数 |
E.核内中子数
F.核外电子总数
(4)地震发生的成因很复杂。研究表明,孕震过程中比较活跃的物质有CO2、氢等。氢在目前的地震预测中被公认为是一种灵敏元素,地壳中水蒸气和氧化亚铁(FeO)作用会产生氢气和氧化铁(Fe2O3),该反应的化学方程式为 。
a.可用于人工降雨的物质是;
b.能除去冰箱中异味的物质是;
c.被认为最清洁最理想的燃料是;
d.可用来制造人造骨的是.
e.可除去热水瓶胆里水垢的是;
f.常用作建筑材料的是.
已知:温度过高过氧化物会分解生成氧化物和氧气.
方法1:由Ca(OH)2为原料最终反应制得,其制备流程如图1: 
方法2:由鸡蛋壳(含CaCO3高达90%)为原料最终反应制得,其制备流程如图2:

-
(1) 方法1中搅拌的目的是.请将搅拌过程中发生反应的化学方程式补充完整:CaCl2+H2O2+2NH3•H2O+6═CaO2•8H2O↓+2NH4Cl.制备过程中除水外可循环使用的物质是(填化学式).
-
(2) 方法2中气体X是,实验室常用溶液来吸收.煅烧后的反应是化合反应,也能生成CaO2•8H2O,反应的化学方程式为.该反应需控制温度在0~2℃,可将反应器放置在,获得的CaO2产品中主要含有的固体杂质是(填化学式).
-
(3) 这两种制法均要求在低温下进行(除煅烧外),温度过高会造成氨水挥发外,还能.
-
(4) “绿色化学”一般是指反应物的原子全部转化为期望的最终产物,则上述两种方法中生成CaO2•8H2O的反应符合“绿色化学”的是(填“方法1”或“方法2”).
南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为“504双吸剂”,其标签如下图所示.南南和北北对这包久置的“504双吸剂”固体样品很好奇,设计如下实验进行探究.

【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3 .
-
(1) 【实验探究】南南同学的方案:
实验操作
实验现象
实验结论
取少量固体放于试管中,滴加足量的.
固体逐渐消失,有无色气体产生,得到浅绿色溶液.
固体中一定含有,一定不含Fe2O3 .
北北同学认为南南同学的实验并不能得出一定不含Fe2O3的结论,理由是,并设计如下实验方案继续验证.
-
(2) 步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是增大接触面积,使反应充分.
步骤②中固体溶解时放出大量热,由此可以判断固体一定含有.写出该过程中的化学方程式.
-
(3) 步骤③中反应的化学方程式是.
北北同学对滤渣B又进行探究.
实验操作
实验现象
实验结论
①取滤渣B于试管中,加入适量
②生成的气体通入
①
②该溶液变浑浊.
固体中一定含有CaCO3和Fe2O3 .
【实验结论】综合上述实验及所给数据,该久置固体中一定含有的物质是Fe、Fe2O3、CaO、CaCO3 .
-
(1) 【提出问题】白色粉末成分的猜想和成因分析.
【做出猜想】①可能是CaCO3:原因是石灰水与空气中的CO2反应.
②可能是:原因是溶剂蒸发,石灰水中的溶质结晶析出.
③还可能是.
-
(2) 【实验探究】甲同学取白色粉末于试管中,加少量的水、震荡,发现试管底部有白色固体,于是他得出白色粉末是CaCO3的结论.乙同学认为甲同学的结论不严密,理由是.
为了得出较严密的结论,他们进行了下表所示实验,请完成实验报告:
实验步骤
实验现象
实验结论
①取上述试管中的上层清液,滴加1~2滴无色酚酞试液
溶液呈红色
白色粉末中
②往上述试管残留的白色固体中加入
白色粉末中含有CaCO3
由上述实验可知,白色粉末成分的猜想是正确的.
-
(3) 【拓展反思】通过上述实验的探究,同学们向实验员提出了保存、使用易变质溶液的下列建议,合理的是.
a.密封保存 b.使用前临时配制 c.禁止使用该试剂.
 钠的氧化物
钠的氧化物  氢氧化钠溶液
氢氧化钠溶液 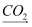 白色固体
白色固体【提出问题】常温下钠与氧气反应,产物有哪些?
【查阅资料】钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH;2Na2O2+2H2O═4NaOH+O2↑
-
(1) 【作出猜想】常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2CO3 ,
猜想3:①
-
(2) 【实验探究一】
实验操作
实验现象
实验结论
取少量钠的氧化物加入足量蒸馏水
②
猜想1正确
-
(3) 【继续探究】钠在空气中放置一段时间得到白色固体的成分
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】
实验操作
实验现象
实验结论
1.取少量白色固体加入足量
③
产生白色沉淀
白色固体成分为Na2CO3
和NaOH
2.过滤、取少量滤液加入④
⑤
-
(4) 【实验反思】
①类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式.
②过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为
③能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2碱性氧化物(填“是”或“不是”).
选项 | 物质 | 杂质 | 试剂 |
A | 木炭粉 | MnO2 | 适量水 |
B | Mg粉 | Cu粉 | 足量稀硫酸 |
C | FeCl3溶液 | CuCl2 | 过量铁粉 |
D | NaCl | MgCl2 | 足量饱和食盐水 |

查阅资料:在75℃左右,氯化步骤中氯气转化成Ca(ClO3)2时发生一系列的反应,其中Cl2与Ca(OH)2反应的总化学方程式可表示为:
6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+aH2O
-
(1) 氯化前,先将电石渣粉碎的目的是.
-
(2) 氯化步骤中所得产物氯酸钙Ca(ClO3)2中Cl的化合价为价,a数值为.
-
(3) 操作X为.转化步骤中Ca(ClO3)2与KCl反应生成KClO3的化学方程式为.(相关物质的溶解度见下表)
物质
Ca(ClO3)2
CaCl2
KClO3
KCl
T℃时溶解度/g
209.0
74.5
7.3
34.2
-
(4) 对滤渣M的成分进行探究
【提出问题】滤渣M中除了电石渣原有的不溶性杂质外,还含有什么物质?
【猜想假设】①CaCO3; ②Ca(OH)2; ③.
【实验验证】
实验步骤
实验现象
结论
步骤1:取少量滤渣M加入盛水的小烧杯中,搅拌,静置后先加入;
观察到现象
猜想①不正确
步骤2:向小烧杯中继续加入足量的稀盐酸
观察到现象
猜想③正确

-
(1) 鸡蛋表面产生大量气泡的主要原因是(用化学方程式表示)。
-
(2) 为进一步确定该气体,小明将一块玻璃片涂上滴有酚酞溶液的澄清石灰水,再将其盖在杯子口(有试剂的一面朝下),一段时间后,观察到。
 向一定量二氧化锰中滴加过氧化氢溶液
B .
向一定量二氧化锰中滴加过氧化氢溶液
B .  向一定量硫酸铜溶液中不断加入铁粉
C .
向一定量硫酸铜溶液中不断加入铁粉
C .  向一定量大理石(杂质不参加反应)中滴加稀盐酸
D .
向一定量大理石(杂质不参加反应)中滴加稀盐酸
D .  向一定量氯化钠和碳酸氢钠混合物中滴加稀盐酸
向一定量氯化钠和碳酸氢钠混合物中滴加稀盐酸
|
实验一 |
实验二 |
实验三 |
|
|
内容 |
| | |
| 现象 | 有气泡产生 | 溶液颜色由红色恰好变为无色 | 产生现象是: |
| 实验结论 | 化学方程式是: | 溶液X是 | 反应方程式略 |
将实验一、二、三结束后的上层澄清溶液倒入同一洁净的烧杯中,后续实验及现象如下图:

I.无色溶液B的pH7(填“<”、“>”或“=”)
II.白色沉淀A是。
III.无色溶液B中一定含有的溶质是。

-
(1) 已知滤液2主要成分是硫酸钠,则滤渣2的化学式为。
-
(2) 上述步骤中,步骤⑥的操作是(填操作名称)。此操作中用到的玻璃仪器有烧杯,玻璃棒、。
-
(3) 步骤④的反应,基本类型是反应。
-
(4) 步骤④中,若选用的稀硫酸溶质的质量分数为9.8%,则用100mL 98%的浓硫酸(密度为1.8g/cm3)配制该稀硫酸,需加水g。
-
(5) 步骤②③两步反应,可以写成一个总的化学反应的化学方程式,该总反应的化学方程式是。
A 生石灰 B 盐酸 C 熟石灰 D 一氧化碳
-
(1) 能帮助人体消化的一种酸;
-
(2) 常用于工业炼铁做还原剂的是;
-
(3) 食品袋中白色干燥剂的成分是;
-
(4) 为防止树木开春后发生病虫害,冬季在树干上涂刷的是。
-
(1) 由三种元素组成的一种盐(填化学式);
-
(2) 活性炭具有很强的,可以除去冰箱内的异昧;
-
(3) 碳酸氢钠是焙制糕点所用的发酵粉的主要成分之一,在医疗上它是治疗胃酸过多症的一种药剂,碳酸氢钠俗称;
-
(4) 氯化钠的用途是。


-
(1) 甲实验中滤渣的成分是,产生白色沉淀的化学反应方程式为。
-
(2) 乙实验中滤液中含有的金属离子为(填离子符号)。
 、Al3+、
、Al3+、  、
、  B . Na+、Cu2+、
B . Na+、Cu2+、  、OH-
C . Mg2+、K+、
、OH-
C . Mg2+、K+、  、Cl-
D . Ca2+、Na+、
、Cl-
D . Ca2+、Na+、  、Cl-
、Cl-
-
(1) 实验前,用砂纸打磨镁条的目的是。
-
(2) 将打磨后的镁条放入稀盐酸中,一段时间后发现有“灰白色沉淀”产生的异常现象。
【提出问题】灰白色沉淀可能含有什么物质?
【查阅资料】①Mg(OH)2受热分解生成MgO和H2O;
②变色硅胶遇水由蓝色变为粉红色;
③碱式氯化镁[化学式:Mg(OH)Cl]不溶于水,受热易分解生成MgO和HCl气体。
【提出假设】
甲同学认为灰白色沉淀中不含MgCl2 , 你认为原因是:。
猜想Ⅰ:Mg猜想Ⅱ:Mg(OH)Cl猜想Ⅲ:Mg(OH)2
-
(3) 【实验探究】乙同学将灰白色沉淀洗涤、干燥后,分别置于编号为①②③的试管中。
序号
实验操作
实验现象
实验结论
实验1
向试管①中加入适量(填物质名称)
沉淀消失无气泡产生
猜想Ⅰ不成立
实验2
加热试管②,并将蘸有紫色石蕊溶液的滤纸条置于试管口
滤纸条变红
猜想Ⅱ
实验3
加热试管③,将产生的气体通过变色硅胶
变色硅胶
猜想Ⅲ成立
-
(4) 【讨论分析】实验2中滤纸条变红是由于HCl气体溶于水使溶液呈性,生成HCl气体的原因是。(用化学方程式表示)






