13.1 离子的检验 知识点题库
下列各组离子在溶液中能大量共存的是( )
A . Cu2+、Mg2+、SO  、NO
、NO  B . H+、Mg2+、SO
B . H+、Mg2+、SO  、ClO﹣
C . Ag+、Na+、NO
、ClO﹣
C . Ag+、Na+、NO  、Cl﹣
D . NH4+、Ba2+、NO
、Cl﹣
D . NH4+、Ba2+、NO  、OH﹣
、OH﹣
 、NO
、NO  B . H+、Mg2+、SO
B . H+、Mg2+、SO  、ClO﹣
C . Ag+、Na+、NO
、ClO﹣
C . Ag+、Na+、NO  、Cl﹣
D . NH4+、Ba2+、NO
、Cl﹣
D . NH4+、Ba2+、NO  、OH﹣
、OH﹣
在溶液中能大量共存,加入OH﹣有沉淀析出,加入H+有气体放出的是( )
A . Na+、Cu2+、Cl﹣、SO42﹣
B . Fe3+、K+、SO42﹣、NO3﹣
C . H+、Al3+、OH﹣、NO3﹣
D . Na+、Ca2+、Cl﹣、HCO3﹣
已知有4种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重复:Ba2+、H+、Na+、NH4+、CO32﹣、NO3﹣、OH﹣、SO42﹣ , 将这4种溶液分别标记为A、B、C、D并进行如下实验:
①在A或D中滴入C,均有沉淀生成;②A和B反应生成的气体能被D吸收;③A和D反应生成的气体能被B吸收.
试回答下列问题:
-
(1) A的化学式是,判断理由是.
-
(2) 写出其他几种物质的化学式:B、C、D.
-
(3) 写出实验③中有关反应的离子方程式.
可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是( )
A . 澄清石灰水、浓硫酸
B . KMnO4酸性溶液、浓硫酸
C . 溴水、浓硫酸
D . 浓硫酸、KMnO4酸性溶液
为了检验某卤代烃(R﹣X)中的X元素,在下列实验操作中:①加热②加入硝酸银溶液③取少量卤代烃④加入稀硝酸溶液酸化⑤加入氢氧化钠溶液⑥冷却,所选择的正确的操作顺序是( )
A . ③⑤④②
B . ③⑤①④②
C . ③⑤①⑥②
D . ③⑤①⑥④②
对于某些离子的检验及结论一定正确的是( )
A . 通入Cl2后,溶液变为黄色,加淀粉液后溶液变蓝,则原溶液中一定有I﹣
B . 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液中一定有SO42﹣
C . 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32﹣
D . 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
A . Na+、K+、OH﹣、Cl﹣
B . Na+、Cu2+、SO42﹣、NO3﹣
C . Mg2+、Na+、SO42﹣、Cl﹣
D . Ba2+、HCO3﹣、NO3﹣、K+
下试剂不能一次性鉴别稀HCl、NaCl溶液、Ca(OH)2溶液的是( )
A . 紫色石蕊
B . 无色酚酞
C . pH试纸
D . Na2CO3
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A . 酸性溶液中:Mg2+、K+、SO42﹣、NO3﹣
B . 无色溶液中:Na+、Al3+、NO3﹣、MnO4﹣
C . FeCl溶液中:Na+、NH4+、SCN﹣ , SO42﹣
D . 与Al反应放出H2的溶液中:NH4+、Na+、NO3﹣、HCO3﹣
常温下,下列各组离子能大量共存的是( )
A . pH=12的溶液中:K+、Na+、Br-、  B . 无色溶液中:H+、K+、
B . 无色溶液中:H+、K+、  、
、  C . c(Fe3+)=0.1mol·L-1的溶液中:K+、H+、SCN-、I-
D . 由水电离出的c(OH-)=1.0×10-13mol·L-1的溶液中:Na+、
C . c(Fe3+)=0.1mol·L-1的溶液中:K+、H+、SCN-、I-
D . 由水电离出的c(OH-)=1.0×10-13mol·L-1的溶液中:Na+、  、
、  、
、 
 B . 无色溶液中:H+、K+、
B . 无色溶液中:H+、K+、  、
、  C . c(Fe3+)=0.1mol·L-1的溶液中:K+、H+、SCN-、I-
D . 由水电离出的c(OH-)=1.0×10-13mol·L-1的溶液中:Na+、
C . c(Fe3+)=0.1mol·L-1的溶液中:K+、H+、SCN-、I-
D . 由水电离出的c(OH-)=1.0×10-13mol·L-1的溶液中:Na+、  、
、  、
、 
在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
A . Na+、K+、OH-、Cl-
B . Na+、Cu2+、SO42-、NO3-
C . Ba2+、HCO3-、NO3-、K+
D . Mg2+、Na+、SO42-、Cl-
把金属钠加入到下列溶液中,还能大量共存的离子组是( )
A . Na+、  、
、  B .
B .  、Cu2+、Cl-
C . K+、
、Cu2+、Cl-
C . K+、  、Cl-
D .
、Cl-
D .  、
、  、Cl-
、Cl-
 、
、  B .
B .  、Cu2+、Cl-
C . K+、
、Cu2+、Cl-
C . K+、  、Cl-
D .
、Cl-
D .  、
、  、Cl-
、Cl-
室温下,下列各组离子在指定溶液中能大量共存的是( )
A . 0.1mol·L-1KI溶液:  B . 0.1
B . 0.1  溶液:
溶液:  C . 0.1
C . 0.1  溶液:
溶液:  D . 0.1
D . 0.1  溶液:Fe3+、Mg2+、SCN-、Cl-
溶液:Fe3+、Mg2+、SCN-、Cl-
 B . 0.1
B . 0.1  溶液:
溶液:  C . 0.1
C . 0.1  溶液:
溶液:  D . 0.1
D . 0.1  溶液:Fe3+、Mg2+、SCN-、Cl-
溶液:Fe3+、Mg2+、SCN-、Cl-
常温下,下列各组离子在指定溶液中能大量共存的是( )
A . 无色透明的溶液中:OH-、Na+、CrO  、SO
、SO  B . c(S2O
B . c(S2O  )=0.1mol·L-1的溶液中:Na+、K+、CO
)=0.1mol·L-1的溶液中:Na+、K+、CO  、SO
、SO  C . 水电离出的c(H+)=1.0×10-13mol·L-1的溶液中:Na+、Mg2+、HSO
C . 水电离出的c(H+)=1.0×10-13mol·L-1的溶液中:Na+、Mg2+、HSO  、NO
、NO  D . 能使蓝色石蕊试纸变红的溶液中:Na+、NH
D . 能使蓝色石蕊试纸变红的溶液中:Na+、NH  、F-、Cl-
、F-、Cl-
 、SO
、SO  B . c(S2O
B . c(S2O  )=0.1mol·L-1的溶液中:Na+、K+、CO
)=0.1mol·L-1的溶液中:Na+、K+、CO  、SO
、SO  C . 水电离出的c(H+)=1.0×10-13mol·L-1的溶液中:Na+、Mg2+、HSO
C . 水电离出的c(H+)=1.0×10-13mol·L-1的溶液中:Na+、Mg2+、HSO  、NO
、NO  D . 能使蓝色石蕊试纸变红的溶液中:Na+、NH
D . 能使蓝色石蕊试纸变红的溶液中:Na+、NH  、F-、Cl-
、F-、Cl-
已知某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,B、D是饮食中两种常见的有机物,F是一种有香味的物质,F中碳原子数是D的两倍。现以A为主要原料合成F和高聚物E,其合成路线如图所示。请回答下列问题
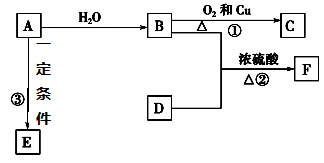
-
(1) A的结构式为,F的名称为。
-
(2) 写出反应的化学方程式
①,反应类型为。
②,反应类型为。
③
-
(3) 实验室怎样鉴别B和D?。
-
(4) 在实验室里我们可以用如图所示的装置来制取F,乙中所盛的试剂为,该装置图中有一个明显的不正确是。
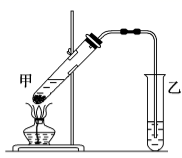
-
(5) 写出F的同分异构体中与D互为同系物的有机物的所有结构简式:。
某化学实验室产生的废液中含有 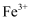 、Cu2+、
、Cu2+、  三种金属离子,小明设计了如下图所示的方案对废液进行处理,以回收金属,保护环境.据此分析,下列说法错误的是( )
三种金属离子,小明设计了如下图所示的方案对废液进行处理,以回收金属,保护环境.据此分析,下列说法错误的是( )
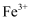 、Cu2+、
、Cu2+、  三种金属离子,小明设计了如下图所示的方案对废液进行处理,以回收金属,保护环境.据此分析,下列说法错误的是( )
三种金属离子,小明设计了如下图所示的方案对废液进行处理,以回收金属,保护环境.据此分析,下列说法错误的是( ) 
A . 沉淀A中含有3种金属单质
B . 可用 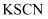 溶液来检验溶液B中所含的金属离子
C . 溶液A只经过操作③最终也可转化为沉淀C
D . 操作①②③中都需要用到玻璃棒、漏斗
溶液来检验溶液B中所含的金属离子
C . 溶液A只经过操作③最终也可转化为沉淀C
D . 操作①②③中都需要用到玻璃棒、漏斗
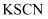 溶液来检验溶液B中所含的金属离子
C . 溶液A只经过操作③最终也可转化为沉淀C
D . 操作①②③中都需要用到玻璃棒、漏斗
溶液来检验溶液B中所含的金属离子
C . 溶液A只经过操作③最终也可转化为沉淀C
D . 操作①②③中都需要用到玻璃棒、漏斗
环丙烷可作为全身麻醉剂,环己烷是重要的有机溶剂。下表是部分环烷烃及烷烃衍生物的结构简式、键线式和某些有机化合物的反应式(其中Pt、Ni是催化剂)。
|
结构简式 |
| | |
| 键线式 | | | |
① ![]() +H2
+H2 
![]()
② ![]() +H2
+H2 
![]()
③ ![]() +H2
+H2 
![]()
④ ![]() +KMnO4
+KMnO4 
![]() +
+ ![]() +Mn2+
+Mn2+
回答下列问题:
-
(1) 环烷烃与是同分异构体。
-
(2) 从反应①~③可以看出,最容易发生开环加成反应的环烷烃是(填名称),判断依据为。
-
(3) 环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件下反应,其化学方程式为(不需注明反应条件)。
-
(4) 写出鉴别环丙烷与丙烯的一种方法:试剂;现象与结论 。
下列有关说法正确的是( )
A . 某试样焰色反应为黄色,则一定含Na元素,一定不含K元素
B . 配制溶液的过程中,如不慎加水超过了容量瓶的刻度线,可用胶头滴管吸出
C . 可用Ba(OH)2溶液来鉴别以下三种溶液:NH4Cl、(NH4)2SO4、K2SO4
D . 为测定某溶液中是否含有  向其中加入盐酸酸化的Ba(NO3)2溶液
向其中加入盐酸酸化的Ba(NO3)2溶液
 向其中加入盐酸酸化的Ba(NO3)2溶液
向其中加入盐酸酸化的Ba(NO3)2溶液
下列各组中的离子,能在透明的溶液中大量共存的是( )
A . Na+、Cu2+、NO 、SO
、SO B . Na+、Mg2+、Cl-、OH-
C . Fe2+、H+、Cl-、MnO
B . Na+、Mg2+、Cl-、OH-
C . Fe2+、H+、Cl-、MnO D . Fe3+、K+、OH-、SO
D . Fe3+、K+、OH-、SO
 、SO
、SO B . Na+、Mg2+、Cl-、OH-
C . Fe2+、H+、Cl-、MnO
B . Na+、Mg2+、Cl-、OH-
C . Fe2+、H+、Cl-、MnO D . Fe3+、K+、OH-、SO
D . Fe3+、K+、OH-、SO
现有5瓶失去标签的液体,已知它们分别是苯、乙醇、乙酸、葡萄糖溶液、乙酸乙酯中的一种,现通过如下实验来确定各试剂瓶中所装液体的成分。
实验步骤与方法 | 实验现象 |
①将5瓶液体分别依次标号为A、B、C、D、E,然后闻气味 | 只有E没有明显气味 |
②各取少量5种液体于试管中,加水稀释 | 只有C、D不溶解并浮在水面上 |
③各取少量5种液体于试管中,滴加新制Cu( OH)2悬浊液并加热 | 只有 B使悬浊液中的固体溶解,E中产生砖红色沉淀 |
④各取少量C、D于试管中,加NaOH稀溶液并加热 | 只有C仍有分层现象,在D的试管口闻到特殊香味 |
-
(1) A为,E中溶质的分子式为。
-
(2) B中所含官能团的名称为。
-
(3) C的二氯代物有种。
-
(4) 写出C在Ni做催化剂的条件下与H2反应的化学方程式。
-
(5) 乙醇可通过乙烯与水在一定条件下反应得到,其对应的化学方程式为,反应类型为。
最近更新






