第二节 化学平衡 知识点题库
(1)已知:2SO2(g)+O2(g)═2SO3(g)△H=﹣196.6kJ•mol﹣1
2NO(g)+O2(g)═2NO2(g)△H=﹣113.0kJ•mol﹣1
则反应NO2(g)+SO2(g)═SO3(g)+NO(g)△H= kJ•mol﹣1。
一定条件下,将NO2与SO2以体积比1:2置于恒温恒容的密闭容器中发生上述反应,下列能说明反应达到平衡状态的有 。
a.体系密度保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1mol SO3的同时生成1mol NO2
测得上述反应平衡时NO2与SO2体积比为1:5,则平衡常数K= 。
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)═CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图所示.实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
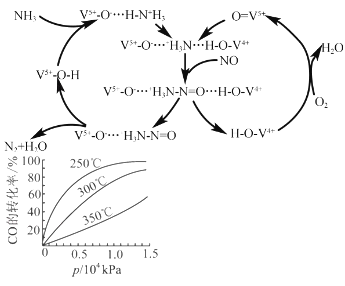
(3)如图是一种用NH3脱除烟气中NO的原理。
①该脱硝原理中,NO最终转化为H2O和 (填化学式)。
②当消耗1mol NH3和0.5molO2时,除去的NO在标准状况下的体积为 L。
(4)NO直接催化分解(生成N2和O2)也是一种脱硝途径.在不同条件下,NO的分解产物不同.在高压下,NO在40℃下分解生成两种化合物,体系中各组分物质的量随时间变化曲线如右图所示,写出NO分解的化学方程式 。
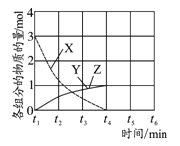
X | Y | W | |
起始状态(mol) | 2 | 1 | 0 |
平衡状态(mol) | 1 | 0.5 | 1.5 |
下列有关说法正确的是( )
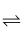 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示.下列说法中正确是( )
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示.下列说法中正确是( ) 
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 42.9 | 50.7 | 64.0 |
请回答下列问题:
-
(1) 该反应的平衡常数表达式 K= ,△H 0(填“>”、“<”或“=”)。
-
(2) 在一个容积为10L的密闭容器中,1300℃时加入 Fe、Fe2O3、CO、CO2各1mol , 反应经过10min 后达到平衡.求该时间范围内反应的平均反应速率 v(CO2)= ,CO 的平衡转化率为 。
-
(3) 欲提高(2)中CO的平衡转化率,可采取的措施是 ______。A . 增加Fe2O3的量 B . 加入合适的催化剂 C . 移出部分CO2 D . 提高反应温度.
-
(1) 已知25℃时:N2(g) + O2(g)
 2NO(g) ΔH = +183kJ/mol
2NO(g) ΔH = +183kJ/mol2H2(g) + O2(g) = 2H2O(l) ΔH = -571.6 kJ/mol
4NH3(g) + 5O2(g) = 4NO(g) +6H2O(l) ΔH = -1164.4 kJ/mol
则 N2(g) + 3H2(g)
 2NH3(g) ΔH = kJ/mol
2NH3(g) ΔH = kJ/mol -
(2) 在恒温恒容体系中进行的合成氨反应,下列能说明该反应已达到平衡状态的是___________A . 容器内N2、H2、NH3的浓度之比为1︰3︰2 B . 3v(N2)正=v(H2)逆 C . 容器内压强保持不变 D . 生成1mol N2的同时消耗2molNH3
-
(3) 在恒温恒容密闭容器中进行合成氨反应,起始投料时各物质浓度如下表:
N2
H2
NH3
投料Ⅰ
1.0 mol/L
3.0 mol /L
0
投料Ⅱ
0.5 mol/L
1.5 mol/L
1.0 mol/L
①按投料Ⅰ进行反应,测得达到化学平衡状态时H2的转化率为40%,则该温度下合成氨反应的平衡常数K=(只需代入数据,不用计算结果)
②按投料Ⅱ进行反应,起始时反应进行的方向为(填“正向”或“逆向”)
-
(4) 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下,写出电极a的电极反应式:

 2HI(g),能量变化如图所示,下列说法错误的是( )
2HI(g),能量变化如图所示,下列说法错误的是( )


下列说法正确的是( )
-
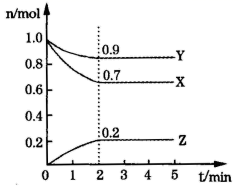
(1) 该反应的化学方程式为
-
(2) 反应开始至2min末,以气体X表示的平均反应速率为;反应开始时与反应达平衡状态时的压强之比为
-
(3) 若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中
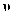 (X)=9mol·L-1·min-1 , 乙中
(X)=9mol·L-1·min-1 , 乙中 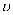 (Y)=6mol·L-1·min-1 , 则反应更快。
(Y)=6mol·L-1·min-1 , 则反应更快。
-
(4) 恒温恒容条件下,能说明该反应达到化学平衡状态的标志是________
①混合气体的压强不再变化 ②混合气体的密度不再变化 ③X的百分含量不再变化
④混合气体的平均相对分子质量不再变化 ⑤
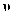 (X) :
(X) : 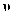 (Y)=3:1A . ①②⑤ B . ①③④ C . ②③④ D . ③④⑤
(Y)=3:1A . ①②⑤ B . ①③④ C . ②③④ D . ③④⑤
 CO(g)+3H2(g)△H1 , 反应Ⅱ:CO(g)+H2O(g)
CO(g)+3H2(g)△H1 , 反应Ⅱ:CO(g)+H2O(g)  CO2(g)+H2(g)△H2 , 恒压下,将等物质的量的CH4和H2O投入到密闭容器中发生反应,CH4和H2O的平衡转化率随温度变化的曲线如图所示。
CO2(g)+H2(g)△H2 , 恒压下,将等物质的量的CH4和H2O投入到密闭容器中发生反应,CH4和H2O的平衡转化率随温度变化的曲线如图所示。 
下列有关说法错误的是( )
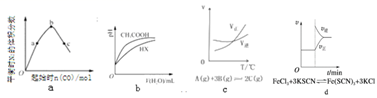
 N2(g)+4CO2(g),保持其他条件不变,改变CO的物质的量,平衡时N2的体积分数变化情况。由图可知,NO2的转化率:c>b>a
B . b表示25℃时,分别加水稀释体积均为100mL、pH=2的CH3COOH溶液和HX溶液,则25℃时HX的电离平衡常数小于CH3COOH的电离平衡常数
C . c是其他条件一定时,反应速率随温度变化的图像,正反应△H>0
D . d是在平衡体系的溶液中溶入少量KCl固体后化学反应速率随时间变化的图象
N2(g)+4CO2(g),保持其他条件不变,改变CO的物质的量,平衡时N2的体积分数变化情况。由图可知,NO2的转化率:c>b>a
B . b表示25℃时,分别加水稀释体积均为100mL、pH=2的CH3COOH溶液和HX溶液,则25℃时HX的电离平衡常数小于CH3COOH的电离平衡常数
C . c是其他条件一定时,反应速率随温度变化的图像,正反应△H>0
D . d是在平衡体系的溶液中溶入少量KCl固体后化学反应速率随时间变化的图象
-
(1) Johnson等人首次在1100℃下用镓与氨气制得氮化镓,该可逆反应每生成
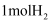 放出10.3kJ热量。该反应的热化学方程式是(已知金属镓的熔点是29.8℃,沸点是2403℃;氮化镓的熔点为1700℃)
放出10.3kJ热量。该反应的热化学方程式是(已知金属镓的熔点是29.8℃,沸点是2403℃;氮化镓的熔点为1700℃)
-
(2) 在恒容密闭容器中,加入一定量的液态镓与氨气发生上述反应,测得反应平衡体系中
 的体积分数与压强(p)、温度(T)的关系如图所示(已知图中T1和T2的温度均小于1700℃)。
的体积分数与压强(p)、温度(T)的关系如图所示(已知图中T1和T2的温度均小于1700℃)。
①下列说法正确的是(填标号)。
a.相同条件下,
 的碱性比
的碱性比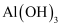 强
强b.当
 时,一定达到了化学平衡状态
时,一定达到了化学平衡状态c.A点和C点化学平衡常数的关系是:

d.温度一定时,达平衡后再充入氨气,
 的体积分数减小
的体积分数减小②气相平衡中用组分的平衡分压代替物质的量浓度也可以表示平衡常数(记作Kp),已知在T1℃时体系的压强初始压强为a Pa,则B点的Kp= Pa(用含a表示且保留2位有效数字)。
-
(3) 电解精炼法提纯镓是工业上常用的方法。具体原理如图所示:已知:镓化学性质与铝相似。
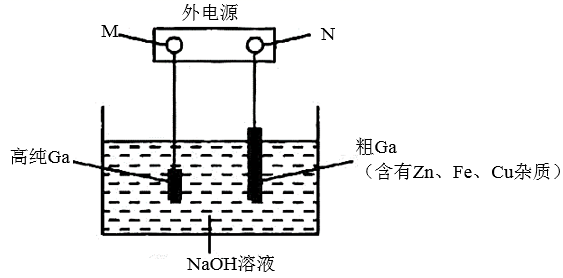
①M为电源的极,电解过程中阳极产生的离子迁移到达阴极并在阴极析出高纯镓。请写出电解过程的阴极的电极反应。
②电解过程中需控制合适的电压,电压太高会导致阴极电解效率下降,其可能的原因是。若外电路通过0.25mol e-时,阴极得到3.5g的镓。则该电解装置的电解效率
 (
( 生成目标产物消耗的电子数/转移的电子总数)
生成目标产物消耗的电子数/转移的电子总数)

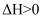 ;达到平衡后,改变下列条件,判断平衡移动的方向(向正反应方向、向逆反应方向、不移动)
;达到平衡后,改变下列条件,判断平衡移动的方向(向正反应方向、向逆反应方向、不移动)
-
(1) 升高温度,平衡移动;
-
(2) 增大压强,平衡移动:
-
(3) 增大H2(g)浓度,平衡移动:加入C,平衡移动;
-
(4) 加入催化剂,平衡移动。
 N2O4(g,无色)。各物质的物质的量随时间变化如图所示。下列说法正确的是( )
N2O4(g,无色)。各物质的物质的量随时间变化如图所示。下列说法正确的是( )
 的催化氧化(
的催化氧化( 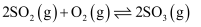
 )。回答下列问题:
)。回答下列问题:
-
(1) 补写完成
 在催化剂
在催化剂  表面反应生成
表面反应生成 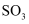 的历程:
的历程: ①
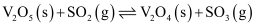

②

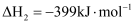
③。
-
(2) 下列关于工业上用
 和
和  反应合成
反应合成 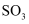 的理解错误的是___________(填标号)。
A . 该反应的实际工业生产条件是高温、常压和合适的催化剂 B . 当温度、压强一定时,混合气组分中
的理解错误的是___________(填标号)。
A . 该反应的实际工业生产条件是高温、常压和合适的催化剂 B . 当温度、压强一定时,混合气组分中 和
和 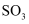 分压比不变,可作为反应达到化学平衡状态的判据
C . 反应过程中可将
分压比不变,可作为反应达到化学平衡状态的判据
C . 反应过程中可将 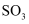 液化移去,有利于提高正反应速率
D . 可以把该反应设计成原电池,实现能量的转化
液化移去,有利于提高正反应速率
D . 可以把该反应设计成原电池,实现能量的转化
-
(3)
 的平衡转化率与反应温度和压强的关系如图所示。
的平衡转化率与反应温度和压强的关系如图所示。 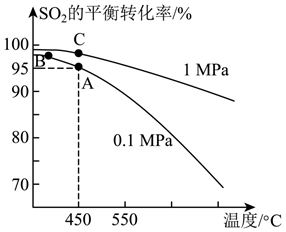
①实际生产选择图中A点的反应条件,不选择B、C点的理由分别是。
②在温度T℃下,向某恒容密闭容器中充入
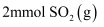 、
、  和
和  ,起始时压强为p,进行反应
,起始时压强为p,进行反应 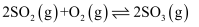 。平衡时,
。平衡时,  转化率为80%,则平衡时
转化率为80%,则平衡时 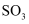 分压为(用含p的代数式表示,下同),平衡常数
分压为(用含p的代数式表示,下同),平衡常数  (以分压代替浓度计算,分压=总压×物质的量分数)。
(以分压代替浓度计算,分压=总压×物质的量分数)。 -
(4) 利用电化学原理可将
 直接转化为
直接转化为  ,其工作原理如图所示,
,其工作原理如图所示, 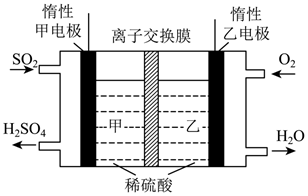
①为使电池持续工作,电解质溶液中的(填离子符号)从(填“甲”或“乙”,下同)室通过离子交换膜移向室。
②起始时,稀硫酸中含
 和
和 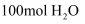 ,当甲电极消耗
,当甲电极消耗 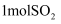 时,甲、乙两室中
时,甲、乙两室中 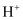 与
与  的总物质的量之比为。(两电极的产物均留在溶液中,忽略水的电离)
的总物质的量之比为。(两电极的产物均留在溶液中,忽略水的电离)
I.CO(g)+2H2(g)⇌CH3OH(g) ΔH1=-90.7kJ·mol-l
II.2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2=-24.5kJ·mol-1
回答下列问题:
-
(1) 由CO和H2直接合成CH3OCH3(g)的热化学反应方程式为。
-
(2) 一定条件下,向恒容容器中充入amolCO和bmolH2 , 反应1min后,测得不同温度下CO转化率如下表所示。则CO转化率在600K时达到最高的原因是。
温度/K
400
450
500
550
600
650
700
CO转化率
22%
28%
32%
40%
61%
50%
18%
-
(3) T℃下,向体积为2L的恒容密闭容器中充入2molCH3OH(g)发生反应II。20min时反应达平衡,测得体系中H2O(g)的体积分数为25%。
①0~20min内,用CH3OH表示的平均反应速率v(CH3OH)=mol·L-1·min-1;T℃下反应的平衡常数K=。若其他条件不变,向该平衡体系中再充入1molCH3OH和1molCH3OCH3 , 则平衡向(填“正”或“逆”)反应方向移动。
②实验测得该反应:v正=k正c2(CH3OH),v逆=k逆c(CH3OCH3)·c(H2O),k正、k逆为速率常数。若改变温度为Tˊ℃,测得平衡时k正=
 , 则TˊT(填“大于”或“小于”),判断的理由为。
, 则TˊT(填“大于”或“小于”),判断的理由为。 -
(4) 不同压强和温度下,将2.0molCO(g)和4.0molH2(g)充入容积为2L的恒温密闭容器中,平衡时体系中二甲醚的物质的量分数变化情况如下图所示,则H2的平衡转化率最大时应选择的条件是____(填标号)。
 A . p1、T4 B . p4、T2 C . P3、T3 D . P4、T1
A . p1、T4 B . p4、T2 C . P3、T3 D . P4、T1



