蒸发操作与粗盐提纯 知识点题库
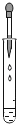 B .
B . 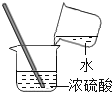 C .
C . 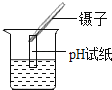 D .
D . 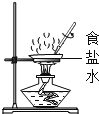
用下列实验操作可分别完成“粗盐中难溶性杂质的去除”和“一定溶质质量分数的氯化钠溶液的配制”两个实验.

-
(1) 操作E中得到的滤液仍浑浊,其原因可能是 (答出一点即可);
-
(2) 若图B所用的烧杯内壁沾有水,导致配制溶液中溶质的质量分数会 (填“偏大”、“偏小”或“不变”);
-
(3) 图D中玻璃棒的作用是 ;
-
(4) 图C中有一处明显的错误,请你改正: .

B . 检查装置气密性
B . 检查装置气密性
C . 滴管用毕即插回
C . 滴管用毕即插回
D . 测定溶液的pH
D . 测定溶液的pH
“粗盐中难溶性杂质的去除”实验中使用了下列仪器和装置,按要求完成下列问题:

-
(1) 仪器①的名称是 .
-
(2) 使用仪器②量取水时,正确的读数方法是 .
-
(3) 使用仪器③称量5.0g粗盐时,天平指针向右偏,接下来的操作是 .
-
(4) ④中玻璃棒不断搅拌的目的是 .

B . 稀释浓硫酸
B . 稀释浓硫酸
C . 蒸发食盐水
C . 蒸发食盐水
D . 铁丝在氧气中燃烧
D . 铁丝在氧气中燃烧

请根据提纯步骤回答下列问题.
-
(1) 步骤⑦的操作名称为;
-
(2) 步骤⑥中加入过量盐酸的目的是;
-
(3) 步骤②和步骤④(填“可以”或“不可以”)颠倒.
按如图完成“蒸馏法淡化海水”的实验,并思考.

-
(1) 向试管中加入5~10mL海水,塞好瓶塞加热,然后往小试管冷凝的水中加入硝酸银溶液,观察到的现象为.
-
(2) 下列哪种方法冷凝效果最好 . (填序号)A . 玻璃管加长 B . 在烧杯内加冰块 C . 使用冷凝器
-
(3) 实验结束时应该先(填“撤导管”或“熄灭酒精灯”),这样做的目的是.
-
(4) 某同学向海水里加入硝酸银溶液做对比实验,发现有白色沉淀产生,该反应的化学方程式:.

-
(1) 如图1是在河面上的“生态浮床”,上面种植着各种各样的水生植物,具有净化水质和美化景观等功能。漂浮在平静河面上的“生态浮床”受到的重力和浮力的大小关系是(选填“大于”、“等于”、“小于”)。
-
(2) 如图2所示是小红同学自制的一个简易净水器来净化含丰富镁元素的井水.他选择了活性炭,是因为它具有性。
-
(3) 法国科学家拉瓦锡在前人探索的基础上发现了水的组成。如图3所示为水电解器,电解水的表达式为 , 其中b管中产生的气体是。
 取固体药品
D .
取固体药品
D . 实验步骤 | 操作过程 |
粗盐提纯 | ①取粗盐放入烧杯中,加适量水,用玻璃棒搅拌直到粗盐充分溶解。 ②把浑浊的食盐水直接倒入已安装好的过滤器中。 ③再将得到的滤液在蒸发皿中加热,并用玻璃棒搅拌。 ④一直到滤液完全蒸干,停止加热。 |
配制溶液 | ⑤计算出配制200g 5%的氯化钠溶液需氯化钠5g、水200g。 ⑥然后用托盘天平和量筒分别称取和量取所需的氯化钠和水。 ⑦再把它们倒入烧杯中,用玻璃棒搅拌。 |
-
(1) ;
-
(2) ;
-
(3) 。

①过滤;②加过量的NaOH溶液;③加适量盐酸;④加过量Na2CO3;⑤加过量的BaCl2;⑥蒸发。
正确的顺序是( )
| 选项 | 实验目的 | 方案 |
| A | 鉴别硝酸钠溶液和硫酸钾溶液 | 取样,滴加Ba(NO3)2溶液,观察现象 |
| B | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、过滤、蒸发 |
| C | 除去CaO中的CaCO3 | 高温加热到固体质量不变 |
| D | 探究Mg、Ag、Cu金属的活动性顺序 | 将两根光亮的镁条分别伸入硫酸铜溶液和硝酸银溶液中 |
-
(1) 以上操作合理的先后顺序为(数字序号不能重复使用)。
-
(2) 上述试剂中Na2CO3不能用K2CO3代替,请说明原因。

-
(1) 实验一:如图是同学们做粗盐提纯实验的操作示意图。回答下列问题:
a.粗盐提纯实验的操作顺序为(填上述操作序号次序);
b.经操作⑥后滤液仍浑浊,原因可能是(答出一点即可);
c.④步骤中的玻璃棒有作用。
-
(2) 实验二:用提纯得到的精盐配制50克5%的氯化钠溶液。步骤如下:
a、计算:可计算出需精盐克,需水毫升。
b.称量和量取:称量氯化钠时,若发现天平指针向左偏,则应怎么处理?。
C.溶解:经检测,所配制的氯化钠溶液的溶质质量分数偏小,其可能原因是。
A.所用的氯化钠固体中含有杂质
B.量取水时,仰视读数
C.将水倒入烧杯时,有少量水溅出
D.将氯化钠固体倒入烧杯时,还有部分氯化钠固体粘在纸上
E.将配制好的溶液转移进试剂瓶时,有溶液洒落
炭还具有还原性,可以冶炼金属。冶炼金属一般有下列四种方法:①焦炭法;②水煤气(或H2 , 或CO)法;③活泼金属置换法;④电解法。四种方法各有优缺点,在工业上均有应用。
-
(1) 一种无色气体A与红热的炭反应,得到另一种无色气体B,B与灼热的氧化铜反应,又得到A,则A、B分别为 。(填序号)A . O2、CO2 B . O2、CO C . CO2、CO D . CO、CO2
-
(2) 钛(Ti)有“未来钢铁”之称,工业上常用活泼金属Mg去置换TiCl4 , 获得海绵状钛,请写出化学方程式。
-
(3) 由于钠的活泼性强,故工业上采用电解熔融氯化钠的方法生产单质钠,化学方程式为:2NaCl(熔融)
 2Na+Cl2↑。
2Na+Cl2↑。 归纳和演绎是重要的科学方法。下列关于金属冶炼的归纳或演绎合理的是( )
A . 由于铝的活泼性强,故工业上不采用活泼金属置换法生产单质铝 B . 将钠投入氯化镁饱和溶液中,可置换出镁单质 C . 冶炼金属的方法,本质上是由金属的活泼性决定的 D . 金属冶炼的实质是将金属元素从其化合物中氧化出来 -
(4) 工业制氯气是用电解饱和食盐水的方法,用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质,在除杂操作时,往粗盐水中先加入过量的 (填化学式),至沉淀不再产生后,再加入过量的(填化学式)和NaOH,充分反应后将沉淀一并滤去,再加入稀盐酸调节食盐水的pH。


-
(1) 操作①、②、③依次为如图乙中的(填字母)。
-
(2) 若食盐的产率偏高(产率=所得晶体的质量/所取样品的质量×100%),则可能的原因是。
-
(3) 用盐水选种子是我国古代劳动人民发明的一种挑选种子的方法,要求盐水的质量分数为12%,现将12克食盐溶解在100克水中,请分析后判断这种盐水是否符合挑选种子的要求? (填“符合”或“不符合”)。
 B . 倾倒液体
B . 倾倒液体  C . 过滤杂质
C . 过滤杂质 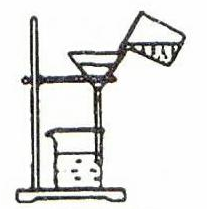 D . 获得食盐晶体
D . 获得食盐晶体 
实验一:如图是甲同学进行粗盐提纯实验的操作示意图。

-
(1) 粗盐提纯实验的正确操作顺序为(填操作示意图的序号);
实验二:乙同学用提纯得到的精盐配制100g溶质质量分数为15%的氯化钠溶液(所用天平称量时,1g以下用游码)。
-
(2) 称量氯化钠时如果发现指针偏向右侧,正确的操作是。如果称量时氯化钠和砝码位置颠倒了,其它操作步骤均正确,则所配制溶液的溶质质量分数(选填“大于”“等于”或“小于”)15%;
-
(3) 【反思拓展】海水晒盐采用操作③的原理而不用冷却氯化钠热饱和溶液的方法,原因是



