空气的成分及探究 知识点题库
为了探究某脱氧剂的成分(由两种单质组成)及利用该脱氧剂测定空气中氧气含量,兴趣小组进行了如下实验:

-
(1) Ⅰ探究脱氧剂成分
【实验观察】脱氧剂为灰黑色粉末,若在空气中放置一段时间,有红棕色固体生成.
【实验猜想】根据颜色变化,猜想该脱氧剂中含有 (填化学式).
【验证猜想】方法为: .
【实验探究】新取一定量的脱氧剂,将已验证的成分分离.取剩余固体与少量CuO混合,置于图1所示装置中加热.一会儿观察到黑色固体变红色,同时澄清石灰水变浑浊.
【实验结论】该脱氧剂中还含有 (填化学式).写出澄清石灰水变浑浊的化学方程式: .
-
(2) Ⅱ测定空气中氧气含量
使用图2装置进行实验.实验前应先进行的操作是 .
【实验过程】
步骤1:在注射器中放入足量脱氧剂粉末(体积为2mL),封闭.
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹.
步骤3:不断轻轻晃动注射器,至活塞位置不再发生变化.
【数据处理】
(1)实验中需要记录的数据是 .
(2)上述实验测定过程至少需要重复两次,其目的是 . 计算得氧气约占空气体积的
 .
. 【实验对比】
实验室常通过燃烧红磷法测定空气中氧气的含量(装置如图3).步骤如下:
(1)用弹簧夹夹紧橡皮管;
(2)点燃燃烧匙内的红磷,立即伸入瓶中并塞紧瓶塞.
(3) .
(4)观察并记录水面的变化情况.
多次实验发现,集气瓶内上升的水面始终小于瓶内原有空气体积的
 .
. 【拓展研究】查阅资料得知,当空气中氧气的体积分数降至约为7%以下时,红磷不再燃烧.由此可知,燃烧红磷法测定结果不够准确的原因的是 .
【实验评价】与燃烧红磷法相比,脱氧剂法测定空气中氧气含量的优点是 .
(1)实验时用来吸取和滴加少量液体的仪器是 .
(2)倾倒液体时,试剂瓶标签没有朝向手心 .
(3)在用红磷测定空气里氧气含量的实验中,如果红磷的量不足,其他操作均正确,则测得空气中氧气的含量  (填“大于”、“小于”或“等于”).
(填“大于”、“小于”或“等于”).
在由两个注射器组成的密闭系统内共有50 mL空气,如右图。然后给装有红磷的玻璃管加热。同时交替推动两个注射器的活塞,至玻璃管内的红磷变成白烟,且较长时间内无进一步变化时停止。停止加热后,待冷却至室温将气体全部推至一个注射器内。

请根据你对上述实验的理解,回答下列问题:
-
(1) 实验结束后,注射器内的气体体积理论上应该减少约mL。
-
(2) 在实验的加热过程中,交替缓慢推动两个注射器的目的是。
-
(3) 通过上面的实验,你学到的测量混合物中某成分含量的方法是
某学习小组为探究空气中氧气的含量,设计了如图所示的装置,根据装置回答下列问题:

-
(1) 用放大镜聚焦使燃烧匙中过量的白磷燃烧,当装置冷却到室温时,可观察到U形管右侧水面的变化情况是;
-
(2) 反应完毕后,U形管右侧剩余的气体主要是;
-
(3) 为什么不能用木炭取代白磷做这个实验:。

-
(1) 图A中产生气体的化学符号表达式;
-
(2) 实验B是测定空气中的氧气含量
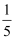 ,该实验成功的关键是(填序号).
,该实验成功的关键是(填序号). ①装置气密性好;②实验前夹紧止水夹;③红磷过量或足量;④冷却后再打开止水夹;⑤要选用教室内的空气.
-
(3) 如果实验室用高锰酸钾制氧气,装置C中还缺少,反应的化学符号表达式为.

 检查装置的气密性
B .
检查装置的气密性
B .  排水法收集氧气
C .
排水法收集氧气
C .  检测空气中氧气的含量
D .
检测空气中氧气的含量
D .  可以控制制取氧气的快慢
可以控制制取氧气的快慢

-
(1) 测定空气成分的方法很多,如图装置C不能测定空气中氧气含量的原因是。
-
(2) 你认为B与A相比装置的优点是。
-
(3) 装置D中实验开始时活塞前沿在5mL刻度处,足量白磷燃烧熄灭后,待温度降低至室温后,活塞沿应停在mL刻度处。
①连接仪器,检查装置气密性,发现装置气密性良好。
②在集气瓶里装进适量a体积的水,燃烧匙里放足量的白磷,并用酒精灯把玻璃棒下端加热,按图示把集气瓶中的空气密封起来,集气瓶内的长导管已伸到了瓶底,长导管的另一端放入盛有足量水的A容器中。
③按下玻璃棒,让玻璃棒与白磷接触,观察到白磷立即燃烧产生大量白烟,同时放热。
④待白磷燃烧熄灭后,稍加振荡,白烟消失。
⑤待集气瓶完全冷却至室温,测出集气瓶中水的体积是b,整个集气瓶的体积是c。
⑥根据a、b、c三个数据,计算出空气中氧气的体积分数(燃烧匙、白磷、玻璃棒、玻璃管体积忽略不计)。

根据以上信息,回答下列问题:
-
(1) 图中A仪器的名称是。
-
(2) 若实验成功,测得空气中氧气的体积分数为
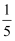 ,则a、b、c三个数据应满足=
,则a、b、c三个数据应满足= 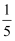 。
。
-
(3) 在白磷开始燃烧到最后熄灭的过程中,小明观察到集气瓶内水位会先下降一段,然后才会上升。水位会下降的原因是。

①连接装置并检查气密性;
②在量筒内加入100mL的水;
③在广口瓶中加入少量水,使瓶内空气体积为250mL;
④在燃烧匙内放入过量的红磷,塞紧瓶塞,关闭止水夹,接通电源使电烙铁发热,点燃红磷后,断开电源;
⑤燃烧结束并充分冷却后,打开止水夹,待量筒内水面不再下降时,记录量筒内水的体积为65mL。
-
(1) 小明按图甲装置进行实验时,该如何检查装置的气密性?。
-
(2) 与图甲装置相比,图乙装置中使用电烙铁可以减小实验误差,其原因是。
-
(3) 根据本实验数据,计算出空气中氧气的体积分数为。
小明发现,测量结果与真实值仍有较大差距,查阅资料发现,引起本实验的误差除装置外,还与可燃物的性质有关。

请回答:
-
(1) 数显设备显示,开始一段时间集气瓶内气体压强上升,这是因为温度升高导致的气压变化量(选填“大于”“等于”或“小于”)氧气减少导致的气压变化量。
-
(2) 基于数显设备显示的气压变化,“过一段时间打开活塞”中的“一段时间”指的是火焰熄灭后到所经历的时间。
-
(3) 在整个实验过程中,集气瓶中减少的氧气体积为(选填“V1-V2”“V1-V3”或“V2-V3”)。
①先将一个底部开孔的玻璃瓶放在水槽中央位置,然后向水槽加入一定量的水;
②在燃烧匙里加入白磷粉末;
③将带有电热棒、燃烧匙和传感器探头的橡胶塞紧紧塞在瓶口上;
④接通电热棒电源一段时间后,发现白磷燃烧起来。

-
(1) 在接通电源前,秀秀用热毛巾捂住玻璃瓶来检查装置的气密性,若气密性良好,则会出现的现象是。
-
(2) 反应结束后,发现玻璃瓶内液面未达空气总体积的20%,其可能的原因有 (可多选)。A . 未完全冷却到室温 B . 燃烧时有气体通过底部小孔逸出 C . 燃烧匙中白磷不足 D . 氧气体积分数低于3.2%时白磷会自动熄灭
-
(3) 图乙、丙是通过气压温度传感器测得的两幅图像,请分析t3时瓶内压强p2会小于初始气压p0的原因。
实验操作步骤如下:

步骤1:检查装置气密性,且装置气密性良好。
步骤2:将盛有足量白磷的燃烧匙放入空集气瓶中,塞紧塞子,白磷不燃烧。
步骤3:打开集气瓶塞子,往瓶中倒满80℃的热水,并塞紧塞子,白磷仍然不能燃烧。
步骤4:打开K1和K2 , 通过注射器从b管抽水,当瓶中液面刚低于燃烧匙底部时,立即同时关闭K1、K2 , 发现瓶中白磷燃烧,此时读出注射器中水量为V1毫升,导管b中水的体积忽略不计。
步骤5:待整个装置冷却至室温时,只打开K2 , 发现注射器中的水剩余V2毫升。
-
(1) 白磷和红磷在空气中燃烧的现象相似。步骤4中,白磷燃烧的现象是。
-
(2) 结合步骤2、4,说明白磷燃烧需要的条件是。
-
(3) 该实验测得空气中氧气的含量为(用V1、V2来表示)。
-
(4) 小明多次重复上述实验,测得空气中氧气的体积分数远大于21%,原因是。

-
(1) 用如图甲所示的实验装置来测定空气中的氧气含量。红磷点燃后迅速塞紧瓶塞,红磷燃烧的现象是:。数显设备显示,红磷刚开始燃烧时集气瓶内气体压强上升,这是因为温度升高导致的气压变化量(填“大于”“小于”或“等于”)氧气量减少导致的气压变化量。
-
(2) “暖宝宝贴”(主要成分为铁粉)的热是来源于铁粉的锈蚀反应(铁生锈消耗空气中的氧气和水并放出热量)。用如图乙所示的实验装置来测定空气中的氧气含量。实验后水从量筒进入广口瓶(广口瓶容积为250 mL),量筒中液面降至60 mL处(铁粉锈蚀消耗的水忽略不计)。下列说法错误的是 (填字母序号)。A . 实验前必须检查装置的气密性 B . 若测得空气中氧气含量偏低,可能是铁粉不足 C . 本次实验测得空气中氧气的体积分数为16% D . 必须等温度计的读数恢复至实验前的温度后,才能记录量筒内剩余水的体积
在老师的指导下,小明进行如图所示实验:用注射器获取V1毫升教室内的空气,通过导管缓缓地全部推入量筒,与量筒内足量的V2毫升一氧化氮气体混合,待充分反应后,读出量筒中剩余气体体积为V3毫升。

说明:①V1、V2、V3都是在与教室气温、气压相同的状态下测得。
②一氧化氮难溶于水,也不与水反应。
③同温同压下,在氢氧化钠溶液参与下,4体积一氧化氮与3体积氧气恰好完全反应,且产物能完全被溶液吸收。
-
(1) 小明用气密性良好的注射器,获取V1毫升教室内空气的具体操作是。
-
(2) 实验测得教室内空气中氧气的体积分数为。(用V1、V2、V3表示)
-
(3) 小明提出,注射器内空气中的二氧化碳也会被氢氧化钠溶液吸收,从而影响实验结果。但老师指出,相比空气中的氧气含量,二氧化碳对实验结果的影响属于“次要因素”,不是“主要因素”,可忽略不计。还有许多科学实验中存在“主要因素”和“次要因素”,请再举一例并指明次要因素。



