浓硫酸的稀释 知识点题库
下列实验操作中,错误的是( )
A . 滴加液体
B . 加热液体
B . 加热液体
C . 稀释浓硫酸
C . 稀释浓硫酸
D . 检查气密性
D . 检查气密性

B . 加热液体
B . 加热液体
C . 稀释浓硫酸
C . 稀释浓硫酸
D . 检查气密性
D . 检查气密性
下列图示实验操作中,正确的是( )
A . 读液体体积
B . 称量固体质量
B . 称量固体质量
C . 过滤
C . 过滤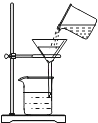
D . 稀释浓硫酸
D . 稀释浓硫酸

B . 称量固体质量
B . 称量固体质量
C . 过滤
C . 过滤
D . 稀释浓硫酸
D . 稀释浓硫酸
下列实验基本操作正确的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
下列有关物质的性质与应用叙述不正确的是( )
A . 氧气能支持燃烧,可用作火箭燃料的助燃剂
B . 氢氧化钠固体能吸水,可用来干燥SO2气体
C . 葡萄糖氧化时放出能量,可用来为人体供能
D . 碳酸氢钠能与酸反应,可用来治疗胃酸过多
下列所用试剂能达到实验目的是( )
实验目的 | 试剂 | |
A | 鉴别浓硫酸与稀硫酸 | 木条 |
B | 鉴别氯化钡溶液与氯化钙溶液 | 碳酸钾溶液 |
C | 除去氮气中的氧气 | 水 |
D | 除去二氧化碳中的一氧化碳 | 氢氧化钠溶液 |
A . A
B . B
C . C
D . D
下列实验操作正确的是( )
A . 
B .
B . 
C .
C . 
D .
D . 

B .
B . 
C .
C . 
D .
D . 
回答下列与常见的酸有关的问题.
(1)胃液中有助于消化的酸是 .
(2)浓硫酸常用作某些气体的干燥剂,主要是利用了浓硫酸具有 性.
(3)分析下列酸与金属氧化物反应方程式,这类反应的规律一般都生成 .
①CuO+H2SO4═CuSO4+H2O
②K2O+2HNO3═2KNO3+H2O
③Fe2O3+6HCl═2FeCl2+3H2O.
下列物质的性质与用途的对应关系错误的是( )
选项 | 性质 | 用途 |
A | 氢氧化钙呈碱性 | 改良酸性土壤 |
B | 浓硫酸具有脱水性 | 干燥氧气 |
C | 稀盐酸能与某些金属氧化物反应 | 除铁锈 |
D | 氢氧化钠能与某些非金属氧化物反应 | 吸收二氧化硫 |
A . A
B . B
C . C
D . D
如图所示,向试管中依次加入约3毫升饱和CuSO4溶液和约2毫升浓H2SO4 , 静止片刻后,可观察到的现象是( )

A . 玻璃管中左液面下降,右液面上升
B . 试管中的液体明显分为两层,上层呈蓝色,下层无色
C . 有蓝色晶体析出
D . 有白色固体沉降到试管底部
稀释浓硫酸的正确操作是 ( )
A . 将水缓缓倒入盛有浓硫酸的烧杯中,边倒边搅拌
B . 将浓硫酸缓缓倒入盛有水的量筒中,边倒边搅拌
C . 将浓硫酸和水同时倒入一试剂瓶中,充分振荡
D . 将浓硫酸缓缓倒入盛有水的烧杯中,边倒边搅拌
由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题。某科学研究小组的同学欲对某种塑料的组成分析探究(资料显示该塑料识含有 C、H 两种元素),他们设计了如图所示的实验装置。目的是通过测量有关数据,推算塑料组成元素的含量。图中字母 A 至 G 均表示装置编号。请根据实验装置,回答下列问题:
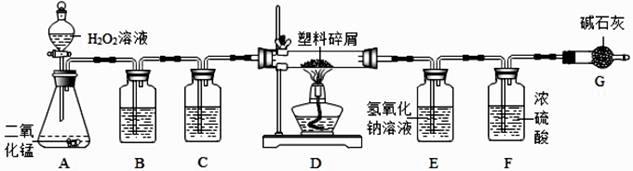
-
(1) 由于发生装置 A 制取的氧气中混有 CO2 和水蒸气,为使 D 装置中塑料试样在纯氧中燃烧,装置 C 中盛放的试剂应该是。
-
(2) E、F 装置是气体的吸收装置,该处的设计有不正确的地方,写出如何改进并说明理由。
-
(3) 碱石灰的成分是氢氧化钠和氧化钙,则装置连接正确时,G 装置的作用是。
实验室里几种物质在向同学们做“自我介绍”,请把内容补充完整。
-
(1) 浓硫酸:因为我有性,看,我滴在纸上把纸弄“黑”了。
-
(2) 烧碱固体:暴露在空气中,我容易,变湿了。
-
(3) 浓盐酸:因为我有挥发性,在空气中放置一段时间我的质量分数会。
下列实验操作正确的是( )
A . 向试管中加入液体  B . 测定溶液的pH值
B . 测定溶液的pH值  C . 收集CO2
C . 收集CO2 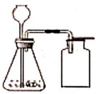 D . 稀释浓硫酸
D . 稀释浓硫酸 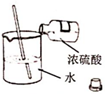
 C . 收集CO2
C . 收集CO2  D . 稀释浓硫酸
D . 稀释浓硫酸 
下列实验操作正确的是( )
A . 加热液体 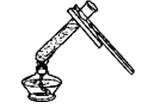 B . 稀释浓硫酸
B . 稀释浓硫酸  C . 过滤
C . 过滤 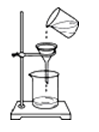 D . 测定溶液pH
D . 测定溶液pH 
 B . 稀释浓硫酸
B . 稀释浓硫酸  C . 过滤
C . 过滤  D . 测定溶液pH
D . 测定溶液pH 
小科发现暖水瓶中有一层淡黄色的水垢。据悉,该地区的水垢中除碳酸钙外,无其它盐类。他想探究还有没有其它物质,于是他收集水垢后经低温烘干进行下列实验:
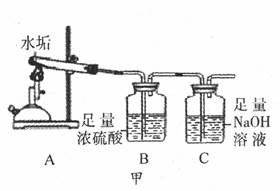
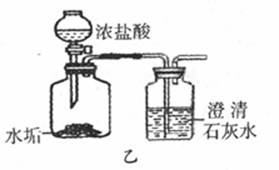
-
(1) 取2.5g水垢按图甲中的A装置高温加热充分反应(已知CaCO3
 CaO+CO2↑),产生的气体依次通过B、C装置,实验后发现C装置中氢氧化钠溶液增加了0.88g。
CaO+CO2↑),产生的气体依次通过B、C装置,实验后发现C装置中氢氧化钠溶液增加了0.88g。 ①写出C装置中发生的化学反应方程式。
②B装置中的浓硫酸是用来吸收反应中产生的水蒸气,这是利用了浓硫酸的性。
③该水垢所含碳酸钙的质量分数为。
-
(2) 按图乙所示的方法来实验,结果发现澄清石灰水没有变浑浊,原因是。
实验室中常需要使用硫酸。
-
(1) 在小纸片上涂上少量浓硫酸,放置一会后,可观察到。
-
(2) 用温度计的液泡蘸取少量浓硫酸,放置在空气中一会儿,可观察到温度计显示温度升高,其原因是。
-
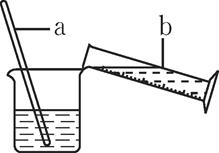
(3) 浓硫酸稀释过程如图所示,b中盛放的物质是。
浓H2SO4稀释时,要将慢慢沿杯壁倒入 中,不能将倒入中,否则将会使,造成危险。衣服、纸张沾到浓硫酸会变焦.是由于浓硫酸有性;浓硫酸可以干燥H2或O2 , 是由于它有性。
实验操作是学习化学的基本方法之一。以下实验操作中正确的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
实验操作或方法正确的是 ( )
A . 称量NaOH固体  B . 稀释浓硫酸
B . 稀释浓硫酸  C . 测溶液pH
C . 测溶液pH  D . 除去H2中的HCl
D . 除去H2中的HCl 
 B . 稀释浓硫酸
B . 稀释浓硫酸  C . 测溶液pH
C . 测溶液pH  D . 除去H2中的HCl
D . 除去H2中的HCl 
硫酸、盐酸是重要的化工原料。
-
(1) 浓硫酸在实验室常用作干燥剂,是因为浓硫酸有性。
-
(2) 98%的浓硫酸稀释为稀硫酸时,一定要将沿烧杯壁缓慢地注入盛有水的烧杯里,并用不断搅拌。
-
(3) 盐酸在下列用途中,不能用硫酸代替盐酸的是(填编号)。
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
最近更新



