物质的量及相关计算 知识点
物质的量及相关计算 知识点题库
-
(1) 生成氧气mol。
-
(2) 反应后剩余固体的成分及相应的质量。
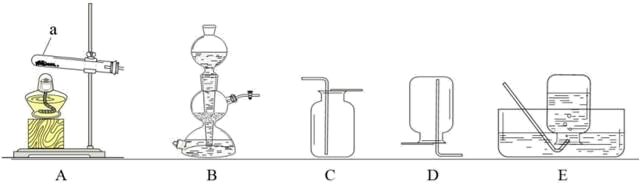
①仪器a的名称:。
②用氯酸钾和二氧化锰制取较干燥的氧气,可选用的装置组合是,反应的化学方程式为。
③实验室制取二氧化碳选用B 装置的优点是,反应的化学方程式为,若要证明该反应后的废液中含有盐酸,不可选用的试剂是。
A.锌粒 B.氧化铜 C.氢氧化铜 D.硝酸银溶液
④用以下仪器组装一套实验室制取CO2的发生装置,可选择B、C和(选填字母)。
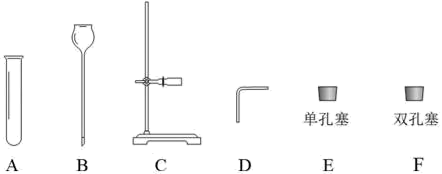
⑤含0.2mol过氧化氢的溶液与二氧化锰混合,充分反应后得到氧气g.(根据化学方程式列式计算)
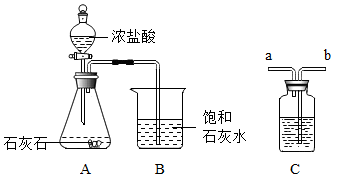
查阅资料:Na2CO3与CO2、H2O反应生成可溶于水的NaHCO3;NaHCO3与HCl反应,与CO2不反应。
①写出装置A中的一种仪器名称。
②反应中装置B内没有变浑浊,用化学方程式解释原因。
③为证明CO2确实能与石灰水反应,在A、B装置之间增加C装置,装置的连接顺序是A→B(填“a”b”);其中盛放的试剂合理的是(填选项序号)。
Ⅰ.浓硫酸;Ⅱ.NaOH溶液;Ⅲ.饱和Na2CO3溶液;Ⅳ.饱和NaHCO3溶液
④改进实验装置后,装置B中饱和石灰水变浑浊了,写出装置B中发生的化学方程式。
⑤石灰石与稀盐酸反应(杂质不与稀盐酸反应),固体质量减少12.5g,则生成二氧化碳气体mol(通过化学方程式计算)。
 甲
甲 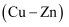 、乙
、乙 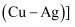 中铜的质量分数,但实验室只提供一瓶标签模糊的稀盐酸和必要的仪器
中铜的质量分数,但实验室只提供一瓶标签模糊的稀盐酸和必要的仪器  根据学过的知识。
根据学过的知识。
-
(1) 你认为他能测出铜的质量分数是哪一块合金?是
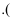 填甲或乙
填甲或乙  理由是:.
理由是:.
-
(2) 现小王取该合金粉末
 与足量该盐酸充分反应,生成
与足量该盐酸充分反应,生成  氢气,则该合金中铜的质量为g,该合金中铜的质量分数为.
氢气,则该合金中铜的质量为g,该合金中铜的质量分数为.
-
(1) 请选择合适物质的编号填空:A 一氧化碳;B 活性炭;C 氢气;D 氦气;E 二氧化硫。
与酸雨形成有关的是;可用于防毒面具的是;可充入霓虹灯内且通电时会发出有色光的是;
-
(2) 1mol氢气中约含有个氢原子。
-
(3) 固定和利用二氧化碳能有效减少空气中的温室气体。例如工业上利用CO2和NH3生产尿素,反应的化学方程式为CO2+2NH3
 CO(NH2)2+X,则X的化学式为。
CO(NH2)2+X,则X的化学式为。
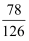 ,其中混合物中只有O22-(过氧离子)和O2-(超氧离子)两种.此晶体中,O22-和O2-的个数比为( )
,其中混合物中只有O22-(过氧离子)和O2-(超氧离子)两种.此晶体中,O22-和O2-的个数比为( )
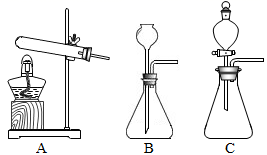
①实验室选用气体发生装置的依据是和。写出用氯酸钾和二氧化锰制取氧气的化学反应方程式,其基本反应类型是。和装置B相比,装置C的优点是。
②过氧化钠(Na2O2)可在潜水艇中作为制取氧气的来源,它能和二氧化碳反应生成氧气和碳酸钠,配平该反应方程式:Na2O2+CO2=Na2CO3+O2。
③实验室用含0.1mol过氧化氢的双氧水与二氧化锰混合制取氧气时,完全分解能产生氧气mol(根据化学方程式列式计算)实验结束后,经过、洗涤、烘干等操作可回收二氧化锰。



