氢气的制取和检验 知识点题库
请结合图示实验装置,回答下列问题.

-
(1) 写出有标号的仪器名称:① , ② .
-
(2) 用高锰酸钾制氧气选用的发生装置是 (选填序号),反应的化学方程式为 .
-
(3) 若B装置中固体为锌粒,试剂可制H2 . 要获得干燥的H2 , 应先将气体通过盛有的D装置,再用E装置收集,气体应从 端通入(选填“a”或“b”).
-
(4) 实验室可用B或C装置制CO2 , 反应的化学方程式为 ,C相对于B装置的优点有 .
-
(5) 若用F装置收集NH3 , 油层的作用是 .
根据下图回答问题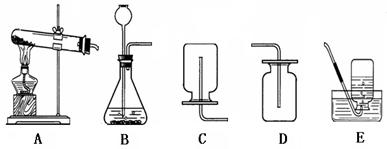
(1)实验室常用稀盐酸和石灰石制取二氧化碳,该反应的化学方程式为 。应选用的发生装置是(填字母,下同) 。 检验二氧化碳是否收集满的方法是 。
(2)实验室常用加热氯酸钾和二氧化锰混合物的方法制取氧气,该反应的化学方程式为 ;实验室常用金属锌和稀硫酸反应制取氢气,该反应的化学方程式为 ; 收集H2的装置是 。
如图为实验室中常见的气体制备、干燥、净化和收集实验的部分仪器,试根据题目要求,回答下列问题: 
-
(1) 若用Zn和稀硫酸反应制取并收集干燥的氢气.
①所选仪器的连接顺序为:(从左至右填写仪器序号字母).
②生成氢气时,发生的化学反应方程式为.
③经测定,装置A中锌粒和稀硫酸反应后溶液的pH了(填“变大”“变小”“不变”之一)
-
(2) 若以H2O2溶液为原料(MnO2为催化剂)在实验室中制备干燥的氧气,并用来测定,CuO和Cu的混合物样品中CuO的质量分数,仪器的连接顺序为A→B1→C→B2 , (B1、B2为浓硫酸洗气瓶),并检验装置的气密性,所设计的实验装置中气体流向是从左向右,小明同学取了氧化铜的混合物样品ag,进行实验:
①根据完全反应后的C装置的质量变化测定CuO的质量分数,若测得C处大玻璃管内的物质总质量增加b克,则该混合物样品中CuO的质量分数(计算结构可为用a和b表示的代数式)
②若C处大玻璃管中红色的固体还没有完全消失就测定,则样品中CuO的质量分数的测算结果将(填“偏大”“偏小”“不影响”之一)
③二氧化锰是H2O2溶液制氧气反应的,反应后的二氧化锰可以进行回收重复利用,可采用的操作方法是、洗涤、干燥.

-
(1) 写出图中标号仪器名称:①;②.
-
(2) 用A装置制取气体前,要先检查装置的,往A装置的试管中加入图中这两种药品时,要先加入.
-
(3) 用B装置收集气体的方法是法,已知氨气的相对分子质量为17,极易溶于水,则收集氨气应选用上述装置中的(填写字母)装置.

-
(1) 写出下列仪器名称:b.
-
(2) 实验室若用A装置制取氧气,反应的化学方程式为;若用装置E收集,则气体应从端通入(填c或d).
-
(3) 实验室制取氢气时,用C装置代替B装置在操作方面的优点是;实验室制取氢气的化学方程式是.
-
(4) 若要分离CO2和CO的混合气体,可将气体通过图2装置(液体药品均足量),操作步骤如下:
①关闭活塞,打开活塞(填a或b,),通入混合气体,可收集到气体.
②然后(填操作),又可收集到另一种气体.

-
(1) 装置A中仪器①的名称为;装置D中仪器②的名称为.
-
(2) 用稀硫酸和锌粒制氢气的发生装置可选用上述或 (填序号)装置;收集氢气可用或(填序号)装置.
-
(3) 除去粗盐中不溶性杂质的实验步骤是、过滤和蒸发结晶,用到的蒸发装置是.(填序号),还必须用下列玻璃仪器组合中的(填序号)才能完成实验.
①漏斗、烧杯、玻璃棒 ②滴管、量筒、试管 ③集气瓶、表面皿、广口瓶
-
(4) 用氯化钠固体和水配制5%的氯化钠溶液,需要用到上图装置中的(填序号).
若配制过程中,在已经有少量水的烧杯中加入5g氯化钠和95mL水,其他操作均规范,则所得溶液中氯化钠的质量分数(填“>”或“<”,或“=”)5%.

-
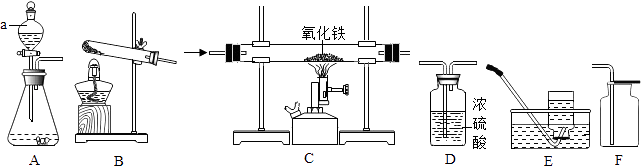
(1) 写出仪器a的名称.
-
(2) 氢气是最理想的燃料.通常状况下,氢气密度比空气小,难溶于水.欣悦同学用锌粒与盐酸反应制取氢气,选择的装置组合是(填字母),该发生装置的优点是,若用F装置排空气法收集氢气,气体应从端进入(填b或c).
-
(3) 【提出问题】①导出的气体除H2外,还有哪些气体?
②氢气具有可燃性外,还具有什么化学性质?
【设计实验方案】欣悦同学按如图2装置进行实验(假设每个装置中气体都完全反应或吸收).
【实验现象和结论】
实验现象
实验结论
甲装置中的白色固体变成蓝色
气体中有H2O
乙装置中产生
气体中有HCl
丁装置中玻璃管内红色粉末变成黑色、戊装置中白色固体变成蓝色
H2能与Fe2O3反应
丁装置中玻璃管内反应的化学方程式为
-
(4) 【交流总结】
①根据丁装置中实验现象,说明氢气具有性.
②丁装置加热前通入H2的目的是.
-
(1) Ⅰ、氯酸钾固体和二氧化锰混合加热,能较快的产生氧气.小刚同学欲在实验室中以此方法制备并收集干燥的氧气.
①所选装置的连接顺序为(填写仪器序号字母).
②用氯酸钾制备氧气的化学方程式为.
-
(2) Ⅱ、小强同学欲用锌和稀硫酸反应制取氢气,然后利用氢气测定某氧化铁样品中含Fe2O3的质量分数(假设杂质不发生反应).选择制取氢气的发生装置是,接下来连接装置的顺序为:D1→C→D2→D3 . (已知:Fe2O3+3H2
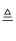 2Fe+3H2O;其中D1、D2、D3为三个盛浓硫酸的洗气瓶)
2Fe+3H2O;其中D1、D2、D3为三个盛浓硫酸的洗气瓶) ①写出仪器a的名称.在装药品之前,检查装置A气密性的具体操作是.
②小强欲通过测量反应前后D2浓硫酸洗气瓶的质量变化,测算氧化铁样品中含有Fe2O3的质量分数.实验中,在其他操作正常的条件下,若装置中不连接D1 , 则测算结果将(填写“偏小”、“偏大”或“不受影响”).
阅读了上述新闻之后,好奇的唐唐猜测:金属钠能与水发生反应。她通过查找资料获得了以下信息:
常温下在空气中易氧化成氧化钠(Na2O),氧化钠可与水化合生成相应的碱;
钠能与水剧烈反应,放出大量的热,生成一种碱和氢气。
她在老师的指导下设计并进行了实验,并做了如下实验记录:

①取一空矿泉水瓶,加入纯净水,仅留一小段空隙,如上图一所示;
②用手挤压矿泉水瓶,除去里面的空气,如上图二所示;
③在胶塞上固定一根大头针,用针扎起一块金属钠,如上图三所示;
④迅速用胶塞塞住挤瘪的瓶口,倒置,如上图四所示;
⑤待完全反应后,打开瓶塞,检验产生的气体;
⑥在矿泉水瓶中滴入数滴A试剂,溶液呈红色。
请根据唐唐的实验过程与实验记录,回答以下问题:
-
(1) 写出试剂A的名称:;
-
(2) 写出钠与水反应的化学方程式:;
-
(3) 写出氧化钠与水反应的化学方程式
-
(4) 为什么在实验步骤②中要除去矿泉水瓶中的空气? ;
-
(5) 本实验中,对取用的金属钠的大小是否有要求,为什么?

-
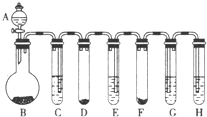
(1) 甲装置:
①仪器a 的名称为
②向a 中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性。
-
(2) 乙装置:
①若生成O2 使气球胀大,则锥形瓶中所装的固体物质可以是
②若生成H2 使气球胀大,则反应的化学方程式为。
③若锥形瓶中装有CaO 固体,分液漏斗中加入少量水,则气球胀大的主要原因是,反应的化学方程式是。
-
(3) 丙装置:
若锥形瓶中盛满CO2 , 欲使气球胀大, 则分液漏斗中的液体可以是。锥形瓶中发生的化学方程式是。
-
(1) 实验开始前必须进行的操作是.
-
(2) 反应开始后,若G中出现红色,H中有白色沉淀生成,判断E、F中的物质可能是;.(填名称)
-
(3) 按基本反应类型写出该实验中有关反应的化学方程式:(装置用字母表示)
化合反应,发生在装置中;
分解反应,发生在装置中;
置换反应,发生在装置中.
-
(1) 氢燃料电池是将能转化为电能。
-
(2) 氢气被称为“绿色能源”的主要原因是。
-
(3) 如图是实验中的常用装置,请回答下列问题:
图一
 图二
图二 
图三

①写出仪器a的名称。
②实验室常用图一装置来制取氢气,反应的化学方程式为,该装置的优点是。
③若用稀盐酸制取氢气,会含有少量杂质,用图二装置可得到干燥、纯净的氢气,导管气流方向接接顺序正确的是(填字母)。
-
(4) 用上述干燥,纯净的氢气进行如图三所示的实验,测定混合固体中CuO的质量分数。已知:反应前A装置中CuO样品的质量为m1g,(样品中的其它物质不与H2反应),反应结束后装置B增重m2g,试用m1、m2表示样品中CuO的质量分数为。

-
(1) 装置图中仪器a的名称为。
-
(2) 实验室用加热高锰酸钾的方法制取氧气,可选用的发生装置是,指出该装置存在的不足,该反应的化学方程式是。收集纯净的氧气所选用的收集装置 ,看到的现象则收集满。
-
(3) 小丽同学做实验需要两瓶氧气,她采用过氧化氢溶液和二氧化锰制取氧气,可选用的最佳发生装置是。
-
(4) 若用G装置采用排空法收集氢气,氢气应从进。(选“b”或“c”)
-
(5) 常温下,用锌粒和稀硫酸(液态)反应制取氢气,可选用B装置,该装置虽操作简便,但无法控制产生氢气的速率。可选择如图中(填序号)装置来取代装置中的双孔塞,以达到控制产生氢气速率的目的。


-
(1) 请写出图中标有字母的仪器名称:a,b。
-
(2) 小蕊想节省药品的同时慢慢地制取二氧化碳,她应该选择发生装置,并且装置还需做改动的是,请写出该反应的化学方程式:。
-
(3) 实验室用氯酸钾制取氧气,可用的发生装置是,请写出反应的化学方程式:,
-
(4) 实验室制取氢气的化学方程式为:,常用的发生和收集装置是,若要收集到干燥的氢气,应将发生装置与F装置的(填“m”或“n”)相连。
-
(1) 如图四种途径都可以得到氧气:

化学实验的绿色化就是以绿色化学的理念和原则来指导实验工作。从实现原料和反应过程的绿色化考虑,你认为在中学化学实验室中,甲、乙、丙三种制取氧气的途径中,(填“甲”“乙”或“丙”)途径更体现化学实验的绿色化追求。请你分别写出乙、丙二种制取氧气的途径反应的化学方程式:乙:;丙:。
-
(2) 实验室用锌粒与稀硫酸反应制取氢气,发生装置如下图所示。打开止水夹,若发现稀硫酸未能与有孔塑料板上的锌粒接触,但此时已无稀硫酸可加,则下列溶液中,最适宜从长颈漏斗中添加的是(选填字母)

A 硫酸钠稀溶液 B 碳酸钠溶液
C 氢氧化钠溶液 D 澄清石灰水
请你写出碳酸钠溶液与澄清石灰水发生化学反应的方程式是。

-
(1) 若制备的气体是氢气,且产生的气体中不含有酸性杂质气体,则试剂X常用,用图示的乙装置收集氢气,A端应与(填“B”或“C”)端相连。
-
(2) 若制备的气体是氧气,且Y是黑色粉末,则甲中发生反应的化学方程式为。
-
(1) 可燃性气体在点燃之前要。发生爆炸的氢气来自反应堆燃料棒用作包壳的金属锆(zr)与水的反应,该反应在高温下生成+4价锆的氧化物和氢气,反应的化学方程式是。
-
(2) 核事故释放出的人工放射性核素碘131是原子序数为53号碘元素的一种原子,下列说法正确的是_____。A . 碘131是一种金属元素 B . 碘131的放射性会对人体产生危害 C . 碘131原子核外的电子数是78 D . 碘131的放射性是化学性质
-
(3) 我国于3月中旬出现了抢购碘盐的现象,用于防护核辐射。碘盐是在食盐中添加了一定量的碘酸钾,由于碘盐中碘含量相对较低,根本起不到预防辐射的作用。碘盐中的“碘”指的是(选“分子”“原子”或“元素”),如果人体内缺碘,会引起甲状腺肿大。因此,在日常生活中,要适量摄入含碘的产品。

-
(1) 写出图中标号仪器①的名称:。
-
(2) 检查装置A气密性的方法是:夹紧止水夹,若,则气密性良好。
-
(3) 用锌粒和稀硫酸制取氢气,选择的发生装置为(填字母),反应的化学方程式为。用装置C而不用装置D收集氢气,原因是。
-
(4) 用装置F和量筒收集并测量氢气的体积,在F中气体应从导管(填“b”或“c”)端通入。

资料:Ⅰ、水煤浆是由煤(主要含碳)与水混合而成,经过气化器后转化为CO和H2。
Ⅱ、在气化器中发生了两个反应:
① ②
②
-
(1) 煤在进入气化器之前,将其粉碎与水混合制成水煤浆的目的是。
-
(2) 气化器中两个反应中含碳物质的化合价皆在(填“不变”、“升高”或“降低”),属于置换反应的是(填序号)。
-
(3) 重整器内发生两步化学反应,写出有CaO参与的化学方程式。
-
(4) 该生产流程中CaO循环再利用的目的是。



