摩尔质量 知识点题库
关于1molCO2(相对分子质量:44)的叙述正确的是( )
A . 质量为44g/mol
B . 摩尔质量为44g
C . 标准状况下的体积约为22.4L
D . 分子数为1
下列叙述正确的是( )
A . 1molH2O的质量为18g/mol
B . 标准状况下,1mol任何物质体积均为22.4L
C . CH4的摩尔质量为16g
D . 3.01×1023个SO2分子的质量为32g
下列数量的物质中含原子个数最多的是( )
A . 0.4mol氧气
B . 4℃时,5.4 mL H2O
C . 标准状况下5.6 L二氧化碳
D . 10g氖
假定把  C的相对原子质量改为24,那么下列叙述错误的是( )
C的相对原子质量改为24,那么下列叙述错误的是( )
 C的相对原子质量改为24,那么下列叙述错误的是( )
C的相对原子质量改为24,那么下列叙述错误的是( )
A . 此时16O的相对原子质量为32
B . NA个O2与NA个H2的质量比为16:1
C . N2的摩尔质量为56g/mol
D . 标准状况下,16g O2的体积约为5.6L
按要求做答
-
(1) 甲烷(CH4)的摩尔质量为。
-
(2) 0.5mol H2的质量为,标准状况下该气体的体积为。
-
(3) 5molCO2所含氧原子的数目为个。
-
(4) 100mL0.25mol/L Na2SO4溶液中Na+的物质的量浓度是mol/L。
-
(5) 有200mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.2mol/L,c(Cl﹣)为1.6mol/L,则Al3+的物质的量浓度为mol/L。
已知3.01×1023个X气体分子的质量为8 g,则X气体的摩尔质量是( )
A . 16g
B . 32g
C . 64g/mol
D . 16g/mol
下列各组物质中物质的量相同的是( )
A . 2 L CO 和 2 L CO2
B . 9 g H2O 和标准状况下 11.2 L CO2
C . 标准状况下 1 mol O2 和 22.4 L H2O
D . 0.2 mol H2 和 4.48 L HCl 气体
用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A . 标准状况下,22.4LH2O含有的分子数为 NA
B . 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C . 通常状况下,NA 个CO2分子占有的体积为22.4L
D . 物质的量为0.5 mol的MgCl2中,含有Mg2+个数为 NA
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A . 物质的量浓度为0.5mol的MgCl2溶液中,含Cl-个数为NA
B . 0.1 mol Na2O2固体与足量的H2O充分反应,转移0.2NA个电子
C . 3g3He含有的中子数为1NA
D . 标准状况下,4.48L的水中含有H2O分子的数目为0.2NA
下列说法正确的是( )
A . 22g CO2含有0.5mol CO2分子,体积为11.2L
B . 3.2g O2和3.2g O3含氧原子的数目不相同
C . 3.01×1023个水分子的质量为9g
D . 1L 0.2mol/L CaCl2溶液中,Cl-数目为0.2×6.02×1023个
NA是阿伏加德罗常数的值。下列说法正确的是( )
A . pH=13的NaOH溶液中含有OH-的数目为0.1NA
B . Na2O2与足量H2O反应生成0.1mol O2时转移电子的数目为0.4NA
C . 常温常压下,23g NO2与N2O4的混合气体中共含有NA个氧原子
D . 常温常压下,22.4L CO2中含有NA个CO2分子
设NA为阿伏加德罗常数的值( )
A . 标准状况下,将22.4LCl2通入水中发生反应,转移的电子数为NA
B . 常温常压下,48gO2与O3混合物含有的氧原子数为3NA
C . 将78gNa2O2与过量CO2反应转移的电子数为2NA
D . 标准状况下,18gD2O中所含电子数为10NA
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 5.6g铁与稀硝酸反应,转移电子数一定为0.3NA
B . 密闭容器中,1molN2和3molH2催化反应后分子总数大于2NA
C . 3.2gN2H4中含有共用电子对的总数为0.6NA
D . 室温下,pH=1的H3PO4溶液中,含有0.1NA个H+
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确是( )

A . 分子中N、O间形成的共价键是非极性键
B . 分子中四个氮原子共平面
C . 该物质既有氧化性又有还原性
D . 15.2g该物资含有6.02×  个原子
个原子
 个原子
个原子
若某氖原子质量是a g,12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法正确的是( )
A . 氖元素的相对原子质量一定是  B . 该氖原子的摩尔质量是aNAg
C . Wg该氖原子的物质的量一定是
B . 该氖原子的摩尔质量是aNAg
C . Wg该氖原子的物质的量一定是  mol
D . Wg该氖原子所含质子数是
mol
D . Wg该氖原子所含质子数是 
 B . 该氖原子的摩尔质量是aNAg
C . Wg该氖原子的物质的量一定是
B . 该氖原子的摩尔质量是aNAg
C . Wg该氖原子的物质的量一定是  mol
D . Wg该氖原子所含质子数是
mol
D . Wg该氖原子所含质子数是 
将宏观和微观联系起来研究物质及其变化是化学的魅力所在。回答下列问题:
-
(1) 0.5molH2O中氢原子的数目为个。
-
(2) 22g某气体中含有3.01×1023个分子,此气体的摩尔质量为g·mol-1
-
(3) 相同质量的O2 , O3 , 氧原子个数之比为。
-
(4) 某同学用Na2CO3固体配制500mL0.10mol·L-1Na2CO3溶液的过程如图所示。指出该同学的不正确操作:(填字母)。

-
(5) 标准状况下,22.4LCO、CO2的混合气体的质量为36g,则CO的质量为g,CO与CO2的体积比为。
-
(6) VLFe2(SO4)3溶液中含mgFe3+ , 则溶液中SO
 的物质的量浓度为mol·L-1
的物质的量浓度为mol·L-1
下列说法正确的是( )
A . NaOH的摩尔质量为40g
B . 钠露置在空气中会发生一系列的变化,最终生成NaHCO3
C . 称取25g胆矾溶于1L水中,即可制得0.1mol·L-1的CuSO4溶液
D . 84消毒液不能与洁厕灵等酸性产品混用是为防止产生有毒的氯气
下列说法中,正确的是( )
A . 物质的量就是物质的质量
B . 摩尔既是物质的数量单位又是物质的质量单位
C . 摩尔质量等于物质的相对分子质量
D . “物质的量”表示含有一定数目粒子的集合体,是七个基本物理量之一
200℃时11.6g CO2 和H2O的混合气体与足量Na2O2充分反应后,固体质量增加了3.6g,则原混合气体的平均相对分子质量为( )
A . 5.8
B . 11.6
C . 23.2
D . 46.4
按要求填空
-
(1) 现有下列物质:①
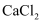 固体;②
固体;② ;③Cu;④
;③Cu;④ 固体;⑤石墨;⑥蔗糖;⑦熔融NaOH;⑧
固体;⑤石墨;⑥蔗糖;⑦熔融NaOH;⑧ 固体;⑨氨水;⑩四氯化碳
固体;⑨氨水;⑩四氯化碳 。
。属于电解质的是(填序号,下同);属于非电解质的是;其中
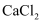 溶于水时的电离方程式是:。
溶于水时的电离方程式是:。 -
(2) 据报道,某些花岗岩会产生氡
 , 对人体产生伤害。请根据Rn的原子结构示意图,预测氡气的化学性质____。
, 对人体产生伤害。请根据Rn的原子结构示意图,预测氡气的化学性质____。 A . 非常活泼,容易与氧气等非金属单质反应 B . 比较活泼,能与钠等活泼金属反应 C . 不太活泼,与氮气性质相似 D . 很难与其他物质发生反应
A . 非常活泼,容易与氧气等非金属单质反应 B . 比较活泼,能与钠等活泼金属反应 C . 不太活泼,与氮气性质相似 D . 很难与其他物质发生反应 -
(3) 81g某金属氯化物
 含有1.2mol氯离子,则金属R的摩尔质量为。
含有1.2mol氯离子,则金属R的摩尔质量为。
-
(4) 某同学在做萃取和分液实验时,将分液漏斗放在铁架台上静置分层,漏斗中的液体分为清晰的两层,但打开分液漏斗下面的旋塞后,并没有液体流下,请分析其可能的原因。
-
(5) 铝是一种活泼的金属,常温下它不仅能和一定浓度的盐酸反应,还能和一定浓度的NaOH溶液反应,请写出铝与NaOH溶液反应的化学方程式。
-
(6) 科学家为什么要引入物质的量?请简要的说说你的理解。
最近更新



