氯气的物理性质 知识点题库
生活中可以用氯气灌洞的方法来消灭田鼠,这是利用了氯气的哪些性质:①密度比空气大②易液化③能溶于水④有毒( )
A . ①⑦
B . ③④
C . ①③④
D . ①④
氯元素有多种盐类,其中亚氯酸钠(NaClO2)亚氯酸钠受热易分解.以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:

请回答下列问题:
-
(1) “反应1”中氧化剂与还原剂物质的比为 ;“反应2”的氧化剂是 (化学式),该反应的化学方程式为
-
(2) 采取“减压蒸发”而不用“常压蒸发”,原因是
-
(3) 从“母液”中可回收的主要物质是 (化学式).
-
(4) “冷却结晶”后经 (填操作名称)即可获得粗产品.
化学史上很多重要物质的发现背后都有科学家们的兴趣、坚持、创新与传承.例如氨的发现史,阅读下文并填空.
1727年,英国牧师、化学家哈尔斯用氯化铵与熟石灰的混合物在以水封闭的曲颈瓶中加热,只见水被吸入瓶中而不见气体放出;
-
(1) 哈尔斯制氨气发生的反应方程式为 ,水吸入曲颈瓶的原理与 实验相同.氨的电子式为
-
(2) 1774年英国化学家普利斯特里重作这个实验,采用汞代替水来密闭曲颈瓶,即排汞取气法,制得了碱空气(氨).他还研究了氨 的性质,他发现
氨可以在纯氧中燃烧,已知该反应为一个置换反应,反应方程式为 ,预期该反应在生产上 (填有或无)实际用途.
-
(3) 在氨气中通以电火花时,气体体积在相同条件下增加很多,该反应的化学方程式是 ,据此证实了氨是氮和氢的化合物.其后戴维等化学家继续研究,进一步证实了氨的组成.
标准状态下,在四个干躁的烧瓶中分别充入:①纯净的氨气,②混有 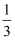 体积空气的氯化氢气体,③纯净的NO2气体,④混有少量O2的NO2气体.然后各做喷泉实验.实验后,三烧瓶中溶液的物质的量浓度大小关系是( )
体积空气的氯化氢气体,③纯净的NO2气体,④混有少量O2的NO2气体.然后各做喷泉实验.实验后,三烧瓶中溶液的物质的量浓度大小关系是( )
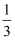 体积空气的氯化氢气体,③纯净的NO2气体,④混有少量O2的NO2气体.然后各做喷泉实验.实验后,三烧瓶中溶液的物质的量浓度大小关系是( )
体积空气的氯化氢气体,③纯净的NO2气体,④混有少量O2的NO2气体.然后各做喷泉实验.实验后,三烧瓶中溶液的物质的量浓度大小关系是( )
A . ①=②=③=④
B . ①=②=③>④
C . ①=②=③<④
D . ④>①=②>③
丰富多彩的颜色变化增添了化学实验的魅力,下列有关反应颜色变化的叙述中正确的是( )
①新制氯水久置后→浅黄绿色消失 ②Cl2通入石蕊试液中→先变红后褪色 ③SO2通入石蕊试液中→先变红后褪色 ④SO2通入品红溶液中→红色褪去 ⑤氨气通入酚酞溶液中→红色 ⑥N2和O2放电条件下→直接生成红棕色气体.
A . ①②③⑥
B . ②③④⑤
C . ①②④⑤
D . 全部
下列各操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①向石灰水中通入过量的CO2
②向Ca(ClO)2溶液中通入过量SO2
③向氢氧化铝胶体中逐滴滴入过量稀NaOH溶液
④向氯化钡溶液中逐渐通入过量二氧化碳
⑤向AgNO3溶液中逐滴滴入过量稀氨水
⑥向饱和碳酸钠溶液中逐渐通入过量二氧化碳.
A . ①②⑥
B . ①③⑤
C . ②④⑥
D . ③④⑤
下列有关氯气的叙述,其说法正确的是( )
A . 在通常情况下氯气比空气重
B . 点燃是使氯气和氢气化合的唯一条件
C . 氯气跟铁反应生成FeCl2
D . 将红热的铜放入氯气中生成蓝色氯化铜
用自来水养金鱼,在将水注入鱼缸之前,常需把水在阳光下晒一段时间,主要目的是( )
A . 增加水中氧气的含量
B . 起杀菌作用
C . 使水中的次氯酸分解
D . 使水的温度升高
CuCl广泛应用于化工和印染等行业。在实验室中模拟热分解CuCl2·xH2O制备CuCl的原理和实验装置如下:

完成下列填空:
-
(1) 在实验(Ⅰ)过程中,观察到B中固体由白色变为蓝色,C中产生的现象是,导致该现象的物质是。
-
(2) 装置D的作用是,其中发生氧化还原反应的化学方程式是。
-
(3) 反应结束后,CuCl产品中可能存在少量的CuCl2或CuO杂质。
①若杂质是CuCl2 , 则原因是。
②若杂质是CuO,则原因是。
-
(4) 根据实验(Ⅱ),测定CuCl2·xH2O中结晶水的含量。取CuCl2·xH2O样品1.692g,经过3次灼烧、冷却、称量,得到黑色固体的质量数据如下:
称 量
第1次
第2次
第3次
质量(g)
0.820g
0.800g
0.800g
则x=(保留2位小数)。
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
|
选项 |
陈述I |
陈述Ⅱ |
|
A |
MnO2有较强的氧化性 |
MnO2可作H2O2分解的催化剂 |
|
B |
SO2具有氧化性 |
SO2通入紫色石蕊试液中先变红后褪色 |
|
C |
液氨汽化时吸热 |
NH3可用作制冷剂 |
|
D |
氯化铁溶于水产生氢氧化铁胶体 |
氯化铁可用于硬水的软化 |
A . A
B . B
C . C
D . D
氨气、氯化氢和水是重要的几种非金属氢化物。请回答下列问题
-
(1) 氨气通入紫色石蕊溶液中,溶液变(填“蓝色”或“红色”)。
-
(2) 氯化氢的水溶液与金属铁反应,生成(填“FeCl2“或“FeCl3”).
-
(3) 水中投入过氧化钠,写出反应的化学方程式:。
如下图,利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是( )
![]()

| 选项 | 实验现象 | 解释 |
| A | 干燥红色石蕊试纸不变色,湿润红色石蕊试纸变蓝 | NH3是一种可溶性碱 |
| B | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
| C | 氯化物溶液变浑浊 | 该溶液一定是MgCl2溶液 |
| D | 浓盐酸附近产生白烟 | NH3与浓盐酸挥发出的HCl反应产生了NH4Cl固体 |
A . A
B . B
C . C
D . D
下列对氯气的叙述中,正确的是( )
A . 工业上用Cl2和石灰水为原料制造漂白粉
B . 红热的铁丝在Cl2中剧烈燃烧生成FeCl2
C . 闻氯气时要小心将集气瓶放在鼻孔下直接闻
D . 氯气没有漂白性,但通入紫色石蕊试液中,溶液先变红后褪色
下列关于氯气的说法正确的是( )
A . 氯气是无色无味气体
B . 铁在氯气中燃烧生成氯化亚铁
C . 氢气在氯气中燃烧,火焰呈淡蓝色
D . 氯气与水反应生成盐酸和次氯酸
下列关于氯气性质的描述中,错误的是( )
A . 无色气体
B . 有刺激性气味
C . 相同条件下密度比空气的大
D . 能与水反应
某同学用下列装置进行有关Cl2的实验。下列说法错误的是( )
A .  证明氯气无漂白作用,氯水有漂白作用
B .
证明氯气无漂白作用,氯水有漂白作用
B .  闻Cl2的气味
C .
闻Cl2的气味
C .  生成棕黄色的烟
D .
生成棕黄色的烟
D .  若气球干瘪,证明Cl2可与NaOH反应
若气球干瘪,证明Cl2可与NaOH反应
 证明氯气无漂白作用,氯水有漂白作用
B .
证明氯气无漂白作用,氯水有漂白作用
B .  闻Cl2的气味
C .
闻Cl2的气味
C .  生成棕黄色的烟
D .
生成棕黄色的烟
D .  若气球干瘪,证明Cl2可与NaOH反应
若气球干瘪,证明Cl2可与NaOH反应
下列物质中,既含有氯分子,又含有氯离子的是( )
A . 氯化钠溶液
B . 新制氯水
C . 漂白粉
D . 液氯
下列有关实验说法,错误的是( )
A . 碱液不慎溅到手上,先用大量水冲洗,再用饱和硼酸溶液洗,最后用水冲洗
B . KCl和MnO2的混合物经溶解、过滤、洗涤、干燥,可分离出MnO2
C . 用容量瓶配制溶液,定容时若加水超过刻度线,应重新配制
D . 用同一针筒先后抽取80mL氯气、20mL水,振荡,气体完全溶解,溶液变为无色
下列气体既有颜色又有毒性的是( )
A .  B .
B .  C . HCl
D .
C . HCl
D . 
 B .
B .  C . HCl
D .
C . HCl
D . 
氯是一种重要的非金属元素。下列有关氯气及其化合物的性质与用途具有对应关系的是( )
A . 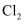 是黄绿色气体,可用于制氯仿
B .
是黄绿色气体,可用于制氯仿
B . 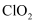 具有强氧化性,可用于环境消毒
C . HClO具有弱酸性,可用于漂白纸张
D . NaCl溶液呈中性,可用于工业制氯气
具有强氧化性,可用于环境消毒
C . HClO具有弱酸性,可用于漂白纸张
D . NaCl溶液呈中性,可用于工业制氯气
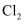 是黄绿色气体,可用于制氯仿
B .
是黄绿色气体,可用于制氯仿
B . 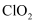 具有强氧化性,可用于环境消毒
C . HClO具有弱酸性,可用于漂白纸张
D . NaCl溶液呈中性,可用于工业制氯气
具有强氧化性,可用于环境消毒
C . HClO具有弱酸性,可用于漂白纸张
D . NaCl溶液呈中性,可用于工业制氯气
最近更新



