常见的生活环境的污染及治理 知识点题库
节日期间因燃放鞭炮会引起空气中SO2含量增高,造成大气污染.实验小组同学欲测定空气中SO2的含量,并探究SO2的性质.

-
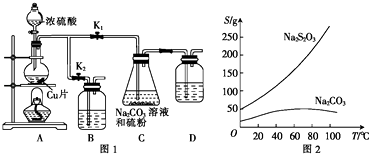
(1) 某实验小组同学拟用如图1所示简易装置测定空气中SO2的含量.
实验操作如下:按图连接好仪器,检查装置气密性后,在广口瓶中盛放足量的H2O2水溶液,用规格为20mL的针筒抽气100次,使空气中的SO2被H2O2水溶液充分吸收(SO2+H2O2=H2SO4).在吸收后的水溶液中加入足量的BaCl2溶液,生成白色沉淀,经过滤、洗涤、干燥等步骤后进行称量,得白色固体0.233mg.
(1)计算所测空气中SO2含量为 mg•L﹣1 .
(2)已知常温下BaSO3的Ksp为5.48x10﹣7 , 饱和亚硫酸溶液中c(SO32﹣)=6.3x10﹣8mol•L﹣1 .
有同学认为以上实验不必用H2O2吸收SO2 , 直接用0.1mol•L﹣1BaCl2溶液来吸收SO2即可产生沉淀.请用以上数据分析这样做是否可行
-
(2) 另一实验小组同学依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2 .
用如图2所示装置收集满Cl2 , 再通入SO2 , 集气瓶中立即产生无色液体,充分反应后,将液体和剩余气体分离,进行如下研究.
(3)写出二氧化锰和浓盐酸反应制取氯气的离子方程式
(4)研究反应的产物.向所得液体中加水,出现白雾,振荡、静置得到无色溶液.经检验该溶液中的阴离子(除OH﹣外)只有SO42﹣、Cl﹣ , 证明无色液体是SO2Cl2 .
写出SO2Cl2与H2O反应的化学方程式 .
(5)研究反应进行的程度.用NaOH溶液吸收分离出的气体,用盐酸酸化后,再滴加BaCl2溶液.产生白色沉淀.
①该白色沉淀的成分是 .
②SO2和Cl2生成SO2Cl2的反应 可逆反应(填“是”或“不是”),阐述理由
热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl﹣KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( )

选项 | 环境问题 | 造成环境问题的主要物质 |
A | 酸雨 | O3 |
B | 温室效应 | CO2 |
C | 南极臭氧层空洞 | SO3 |
D | 光化学烟雾 | N2 |
-
(1) 下列做法有助于能源“开源节流”的是 (填字母).
a.大力开采煤、石油和天然气以满足人们日益增长的能源需求
b.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
c.开发太阳能、水能、风能、地热等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
-
(2) 氢能是理想的清洁能源.下列制氢的方法中,最节能的是 (填字母).
a.电解水制氢:2H2O
 2H2↑+O2↑
2H2↑+O2↑b.高温使水分解制氢:2H2O
 2H2↑+O2↑
2H2↑+O2↑c.太阳光催化分解水制氢:2H2O
 2H2↑+O2↑
2H2↑+O2↑d.天然气制氢:CH4+H2O
 CO+3H2
CO+3H2 -
(3) 利用MnFe2O4通过两步反应使水分解制氢气,第一步反反应为:
MnFe2O4
 MnFe2O4﹣X+
MnFe2O4﹣X+ 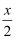 O2
O2则第二步反应的化学方程式为 (不写条件).
-
(4) 图是以SO2、I2、H2O为原料,利用核能使水分解制氢气的一种流程.

反应X的化学方程式为,该流程中循环使用的原料有.从理论上讲,该流程中,1mol原料水制得molH2 .
①直接排放电镀废水入海 ②使用无磷洗衣粉 ③实施沙漠绿化工程④大量使用含硫量高的燃煤 ⑤建立垃圾发电厂 ⑥大力发展清洁能源



