金属冶炼的一般原理 知识点题库
铜的冶炼过程大致可分为:
①富集,将硫化物矿进行浮选;
②焙烧,主要反应为2CuFeS2+4O2═Cu2S+3SO2+2FeO(炉渣);
③制粗铜,在1200℃发生的主要反应为2Cu2S+3O2═2Cu2O+2SO2;2Cu2O+Cu2S═6Cu+SO2↑;
④电解精炼铜.
下列说法正确的是( )
A . 冶炼过程中的尾气可用来制硫酸
B . 上述过程中,由1molCuFeS2制取1molCu时共消耗2molO2
C . 在反应2Cu2O+Cu2S═6Cu+SO2↑中,只有Cu2O作氧化剂
D . 电解精炼铜的过程中,每转移1mol电子时,阳极溶解铜的质量为32g
下列叙述不正确的是( )
A . 根据金属活动性顺序表,可以推断冶炼金属时可能的方法
B . CaCl2、MgCl2晶体都容易潮解,它们潮解的实质是晶体表面吸水形成溶液
C . 根据某元素原子的质子数和中子数,可以确定该元素的相对原子质量
D . 根据酸、碱、盐的溶解性表,可以判断某些溶液中的复分解反应能否进行
完成下列反应化学方程式:
-
(1) 用氯乙烯制聚氯乙烯;
-
(2) 湿法炼铜;
-
(3) 用CO还原赤铁矿(Fe2O3)冶炼铁;
-
(4) 用铝矾土(Al2O3)冶炼铝;
-
(5) 丁烷裂解获得乙烯.
下列叙述正确的是( )
A . SO2具有还原性,故可作漂白剂
B . Na的金属活性比Mg强,故可用Na与MgCl2溶液反应制Mg
C . 浓硝酸中的HNO3见光易分解,故有时在实验室看到的浓硝酸呈黄色
D . Fe在Cl2中燃烧生成FeCl3 , 故在与其他非金属反应的产物中的Fe也显+3价
化学与生活、社会发展息息相关,下列记载或叙述错误的是( )
A . “丹砂烧之成水银,积变又成丹砂”,是因为加热丹砂(HgS)熔融成液态,冷却时重新结晶成HgS晶体
B . “霾尘积聚难见路人”,雾霾所形成的气溶胶能产生丁达尔效应
C . “曾青涂铁,铁赤色如铜”(“曾青”是指硫酸铜),记载中的反应属于置换反应
D . “用浓酒和糟入甑(蒸锅),蒸令气上,用器承滴露”,涉及的操作是蒸馏
下列金属冶炼的反应原理,不合理的是
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
下列冶炼金属的方法错误的是( )
A . 加热分解  制金属Hg
B . 高温下用CO还原赤铁矿炼铁
C . 电解
制金属Hg
B . 高温下用CO还原赤铁矿炼铁
C . 电解 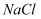 溶液制金属Na
D . Fe和
溶液制金属Na
D . Fe和  溶液湿法炼铜
溶液湿法炼铜
 制金属Hg
B . 高温下用CO还原赤铁矿炼铁
C . 电解
制金属Hg
B . 高温下用CO还原赤铁矿炼铁
C . 电解 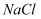 溶液制金属Na
D . Fe和
溶液制金属Na
D . Fe和  溶液湿法炼铜
溶液湿法炼铜
下列化学反应不宜作为工业冶炼金属的原理的是( )
A . 2NaCl(熔融)  2Na+Cl2↑
B . Al2O3+3C
2Na+Cl2↑
B . Al2O3+3C  2Al+3CO↑
C . Fe2O3+3CO
2Al+3CO↑
C . Fe2O3+3CO  2Fe+3CO2
D . HgS+O2
2Fe+3CO2
D . HgS+O2  Hg+SO2
Hg+SO2
 2Na+Cl2↑
B . Al2O3+3C
2Na+Cl2↑
B . Al2O3+3C  2Al+3CO↑
C . Fe2O3+3CO
2Al+3CO↑
C . Fe2O3+3CO  2Fe+3CO2
D . HgS+O2
2Fe+3CO2
D . HgS+O2  Hg+SO2
Hg+SO2
下列叙述正确的是( )
A . 活泼金属钠用电解法冶炼
B . 铜只能用电解法冶炼得到
C . 汞的冶炼只能用热还原法
D . 用铝热法冶炼铝
金属冶炼的实质是( )
A . 金属元素失去电子
B . 金属元素获得电子
C . 金属元素被氧化了
D . 金属元素可能被氧化,也可能被还原
甲、乙为两种常见的单质,丙、丁为氧化物,它们存在如下转化关系,则不满足条件的甲和乙为()

A . 铝和铁
B . 镁和碳
C . 铁和氢气
D . 铜和氢气
某卤块样品的主要成分为MgCl2、FeCl3、FeCl2 , 一实验小组以该样品为原料。按如下流程制取铁单质和氧化镁(假设杂质不参加反应)。
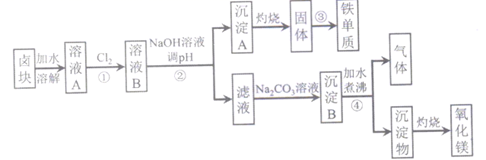
已知部分金属离子沉淀的pH如下表:
| 金属离子 | Fe3+ | Fe2+ | Mg2+ |
| 开始沉淀的pH | 2.7 | 7.6 | 9.6 |
| 沉淀完全的pH | 3.7 | 9.6 | 11.1 |
回答以下问题:
-
(1) 流程①通入Cl2反应的离子方程式为;流程②NaOH溶液调pH的适宜范围< pH<。
-
(2) 沉淀A是;分离沉淀A和滤液的操作名称是,该滤液中的主要溶质为和 (填化学式)。
-
(3) 工业上用流程③冶炼铁的方法属于_______(填正确答案的字母)。A . 物理分离法 B . 电解法. C . 热还原法 D . 热分解法
-
(4) 流程④产生的气体是CO2 , 其反应的化学方程式为。
下列说法错误的是( )
A . 铅蓄电池的工作原理为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,铅蓄电池在放电过程中,负极质量增加,正极质量也增加
B . 金属铝的冶炼流程为:铝土矿 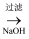 NaAlO2
NaAlO2  Al(OH)3
Al(OH)3 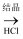 无水AlCl3
无水AlCl3  Al
C . 铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀,但加热反应剧烈
D . 一定条件下,使用催化剂能加快反应速率但不提高反应物的平衡转化率
Al
C . 铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀,但加热反应剧烈
D . 一定条件下,使用催化剂能加快反应速率但不提高反应物的平衡转化率
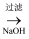 NaAlO2
NaAlO2  Al(OH)3
Al(OH)3 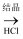 无水AlCl3
无水AlCl3  Al
C . 铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀,但加热反应剧烈
D . 一定条件下,使用催化剂能加快反应速率但不提高反应物的平衡转化率
Al
C . 铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀,但加热反应剧烈
D . 一定条件下,使用催化剂能加快反应速率但不提高反应物的平衡转化率
地球上的金属矿物资源是有限的,应合理开发利用。
-
(1) 金属冶炼的实质是金属离子被(填“氧化”或“还原”)生成金属单质。
-
(2) 铜在自然界存在于多种矿石中,如:
矿石名称
黄铜矿
辉铜矿
孔雀石
主要成分
CuFeS2
Cu2S
Cu2(OH)2 CO3
请回答下列问题:
① 上表所列铜化合物中,推断铜的质量百分含量最高的是。
② CuFeS2其中 Cu 为+1 价、Fe 为+3 价,高温焙烧时发生的反应是CuFeS2 + O2
 SO2 +FeS +Cu,焙烧过程中被还原的元素有。
SO2 +FeS +Cu,焙烧过程中被还原的元素有。③ 工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:Cu2S+O2
 2Cu+SO2 , 该反应中氧化剂是。
2Cu+SO2 , 该反应中氧化剂是。④ Cu2(OH)2 CO3 与稀硫酸反应的离子方程式为。
海水是人类宝贵的自然资源,从海水中可以提取多种化工原料。部分流程如图:
 请回答下列问题:
请回答下列问题:
-
(1) 请写出海水淡化的两种方法:、。
-
(2) 通入热空气吹出Br2 , 利用了Br2的(填序号)。
a.氧化性 b.还原性c.挥发性
-
(3) 操作Ⅰ用SO2水溶液吸收Br2有关反应的离子方程式为。
-
(4) 写出操作Ⅱ通氯气后发生的离子方程式。
-
(5) 为使母液中的MgCl2转化为Mg(OH)2 , 从原料来源及经济效益角度考虑,试剂①最好选用。
a.氨水 b.氢氧化钙c.氢氧化钠
-
(6) 操作Ⅲ的化学方程式为。
下列有关无机材料的叙述正确的是( )
A . 工业上常用电解法来生产铝、钠、铁等金属
B . 工业生产玻璃和水泥均要用到石灰石
C . 硅是生产计算机芯片的原料,二氧化硅是制造太阳能电池的原料
D . 耐高温的碳化硅陶瓷是新型无机非金属材料,属于高分子化合物
中华文化对人类文明和进步有着巨大贡献,对下列描述所作的解释或说明正确的是( )
| 选项 | 描述 | 解释或说明 |
| A | 有硇水者,剪银塊投之,则旋而为水 | 能溶解银的“硇水”可能为硝酸 |
| B | 暮春之初,北海之民即煮海为盐 | “煮海为盐”涉及蒸发结晶 |
| C | 曾青得铁则化为铜 | 曾青的蓝色来自 |
| D | 丹砂烧之成水银 | 金属均可用热分解法冶炼 |
A . A
B . B
C . C
D . D
下列金属的冶炼原理中,属于热分解法的是( )
A . 2HgO  2Hg+O2
B . Fe3O4+4CO
2Hg+O2
B . Fe3O4+4CO  3Fe+4CO2
C . Fe+CuSO4 =Cu+FeSO4
D . 2NaCl(熔融)
3Fe+4CO2
C . Fe+CuSO4 =Cu+FeSO4
D . 2NaCl(熔融)  2Na+Cl2↑
2Na+Cl2↑
 2Hg+O2
B . Fe3O4+4CO
2Hg+O2
B . Fe3O4+4CO  3Fe+4CO2
C . Fe+CuSO4 =Cu+FeSO4
D . 2NaCl(熔融)
3Fe+4CO2
C . Fe+CuSO4 =Cu+FeSO4
D . 2NaCl(熔融)  2Na+Cl2↑
2Na+Cl2↑
化学与人类生产、生活、社会可持续发展密切相关。下列说法正确的是( )
A . 煤、石油、天然气都是可再生能源
B . 气象环境报告中的”PM2.5”是对一种新分子的描述
C . 由于 Al 的活泼性强,故工业上采用电解熔融 AlCl3的方法生产 Al
D . “一带一路”是“丝绸之路经济带”和“21世纪海上丝绸之路”的简称。丝绸的主要成分是蛋白质,属于高分子化合物
下列关于物质制备的说法正确的是( )
A . 可用电解饱和食盐水的方法制取金属钠
B . 工业上主要用Na2O和H2O反应制取NaOH
C . 工业上用氯气与澄清石灰水反应制取漂白粉
D . 侯氏制碱法的原料有食盐、氨、二氧化碳,最终制得碳酸钠
最近更新




