化学电源新型电池 知识点题库
则下列推断中,正确的是( )

 ﹣e﹣═N2O5
D . 石墨II极上发生氧化反应
﹣e﹣═N2O5
D . 石墨II极上发生氧化反应
-
(1) 将锌片和银片用导线相连浸入稀硫酸中组成原电池.若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,试计算产生氢气的体积(标准状况).
-
(2) 利用下列反应:Fe+2Fe3+=3Fe2+ , 设计一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选):负极电极反应;正极材料,正极电极反应.
磷酸铁锂电池具有高效率输出、可快速充电、对环境无污染等优点,其工作原理如图。M电极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种
能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式
为LixC6+Li1-xFePO4 ![]() LiFePO4+6C。下列说法正确的是( )
LiFePO4+6C。下列说法正确的是( )

-
(1) 燃料电池具有广阔的发展前途,请说出其优点(任答一点).以甲醇燃料电池为例,在KOH为电解质溶液的碱性电池中,负极反应式为:.总反应式为:.
-
(2) 工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+2H2(g)⇌CH3OH(1)△H1=﹣116kJ•mol﹣1
又知:CO(g)+
 O2(g)=CO2(g)△H2=﹣283kJ•mol﹣1
O2(g)=CO2(g)△H2=﹣283kJ•mol﹣1H2(g)+
 O2(g)=H2O(g)△H3=﹣242kJ•mol﹣1
O2(g)=H2O(g)△H3=﹣242kJ•mol﹣1H2(g)+
 O2(g)=H2O(1)△H4=﹣286kJ•mol﹣1
O2(g)=H2O(1)△H4=﹣286kJ•mol﹣1则表示甲醇的燃烧热△H=.
 2CO32﹣+6H2O,则下列说法错误的是( )
2CO32﹣+6H2O,则下列说法错误的是( )


 B .
B .  C .
C .  D .
D . 
 VO2+(黄色)+V2+(绿色)+2H+。下列说法正确的是( )
VO2+(黄色)+V2+(绿色)+2H+。下列说法正确的是( ) 


-
(1) 2SO2(g)+O2(g)
 2SO3(g)ΔH=kJ·mol-1(
2SO3(g)ΔH=kJ·mol-1(  含E1、E2的计算式表示)
含E1、E2的计算式表示)
-
(2) ①下列措施不能使该反应速率加快的是。
A.升高温度 B.降低压强 C.使用催化剂
②若上述反应在恒容的密闭容器中进行,下列叙述中能说明该反应已达平衡状态的是。
A.SO3的浓度不再变化
B.SO2与SO3的物质的量相等
C.容器内气体的压强不再变化
D.单位时间内消耗1molO2 , 同时消耗2molSO2
-
(3) 运用电化学原理可生产硫酸,总反应为2SO2+O2+2H2O=2H2SO4 , 装置如图所示。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。

①该电池的负极是。(填“电极a”或“电极b”)
②H+通过质子交换膜时的移动方向是。
A.从左向右 B.从右向左
③通入O2的电极反应式是。
I.研究发现,一定温度和压强下,在催化剂表面,反应N2(g)+3H2(g) 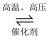 2NH3(g)的相关能量(E)变化如图所示:
2NH3(g)的相关能量(E)变化如图所示:

-
(1) 每生成2molNH3时 (填放出”或“吸收”) kJ的能量。
-
(2) 在恒容密闭容器中发生上述反应,能说明该反应达到平衡状态的是。
a.容器内混合气体的质量不再变化
b.c(N2):c(H2):c(NH3)=1:3:2
c.容器内NH3的浓度不再变化
d.容器内混合气体的物质的量不再变化
-
(3) 一定温度下,在体积为2L的密团容器中,充入1molN2和3molH2模拟工业合成氨的反应。10min时,测得容器中气体的总物质的量是起始时的0.8倍,用NH3的浓度变化表示的化学反应速率为。
-
(4) II.某氨-空气燃料电池的工作原理是氨气与氧生成一种常见的无毒气体和水,其装置如图所示:

溶液c最好选择(填“酸性”、“碱性”或“中性”)溶液。
-
(5) 正极的电极反应式为。

-
(1) 一种脱硫工艺为:真空K2CO3-克劳斯法。
①K2CO3溶液吸收H2S的反应为K2CO3+H2S=KHS+KHCO3 , 该反应的平衡常数的对数值为lgK=。(已知:H2CO3 lgK1= -6.4,lgK2=-10.3; H2S lgK1ˊ= -7,lgK2ˊ= -19)
②已知下列热化学方程式:
2H2S(g) +3O2(g)=2SO2(g)+2H2O(l) ΔH1= -1172kJ·mol-1
2H2S(g) +O2(g)=2S (s) +2H2O(l) △H2 = -632 kJ·mol-1
克劳斯法回收硫的反应为SO2气体和H2S气体反应生成S(s),则该反应的热化学方程式为。
-
(2) 工业采用高温分解H2S制取氢气,2H2S(g)
 2H2(g) +S2(g),在膜反应器中分离出H2。在容积为2L的恒容密闭容器中,控制不同温度进行此反应。H2S的起始物质的量均为1mol,实验过程中测得H2S的转化率如图所示。曲线a表示H2S的平衡转化率与温度的关系,曲线b表示不同温度下反应经过相同时间时H2S的转化率。
2H2(g) +S2(g),在膜反应器中分离出H2。在容积为2L的恒容密闭容器中,控制不同温度进行此反应。H2S的起始物质的量均为1mol,实验过程中测得H2S的转化率如图所示。曲线a表示H2S的平衡转化率与温度的关系,曲线b表示不同温度下反应经过相同时间时H2S的转化率。

①反应2H2S(g)⇌2H2(g) + S2(g) 的ΔH(填“>”“<”或“=”) 0。
②985℃ 时,反应经过5 s达到平衡状态,此时H2S的转化率为40%,则用H2表示的反应速率为v(H2) =,下列各项不能作为该反应达到平衡状态的标志的是。
A.压强不再变化
B.气体密度不再变化
C.气体的平均相对分子质量不再变化
D.H2的消耗速率与S2的消耗速率之比为2:1
E. S2 的在体系中质量分数保持不变
③随着H2S分解温度的升高,曲线b向曲线a逐渐靠近,其原因是。
-
(3) 科学家设计出质子膜H2S燃料电池,实现了利用H2S废气资源回收能量并得到单质硫。质子膜H2S燃料电池的结构示意图如图所示。

①装置中微电池负极的电极反应式:
②当有16gS2析出时,有mol H+ 经质子膜进入正极区。
I.我们可以二氧化钛表面覆盖Cu2Al2O4为催化剂,将CO2和CH4转化成乙酸,CO2(g)+CH4(g)  CH3COOH(g)。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。
CH3COOH(g)。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。

-
(1) 250~300℃时,乙酸的生成速率降低的主要原因是,300~400℃时,乙酸的生成速率升高的主要原因是,在此工业生产中,我们应选择的最佳条件为。
-
(2) 在300℃时判断该反应在固定容积的容器中反应达到平衡的标志为___。A . 容器内的气体分子总个数不再发生变化 B . 生成CO2的反应速率与消耗CH3COOH的反应速率相等 C . 容器内气体平均摩尔质量不再发生变化 D . 容器内气体密度不再变化
-
(3) II.已知CH4+2O2→CO2+2H2O,为了提高甲烷的能量利用率,可以把CH4设计成燃料电池使用,如图所示,c为一种质子交换膜,它只允许H+通过,回答下列问题。

该燃料电池的正极为:(填“a”或“b”)。a电极反应方程式:。b电极反应方程式:。
-
(4) H+在电池内部电解质溶液中向(填“左”或“右”)移动。
-
(5) 在标准状况下,若每分钟通过质子交换膜的H+为0.01mol,那么消耗甲烷的体积为L。
-
(1) 如图是依据氧化还原反应
 设计的原电池装置。
设计的原电池装置。 
①电极Y的材料是(填化学名称)。
②X上发生的电极反应式为。
-
(2) 如图是使用固体电解质的燃料电池,装置中以稀土金属材料作惰性电极,在两极上分别通入
 和空气,其中固体电解质是掺杂了
和空气,其中固体电解质是掺杂了  的
的  固体,它在高温下能传导正极生成的
固体,它在高温下能传导正极生成的  离子(
离子(  )。
)。 
①c电极为(填“正”或“负”)极。
②d上的电极反应式为。
③如果消耗甲烷
 ,假设化学能完全转化为电能,则转移电子的数目为(用
,假设化学能完全转化为电能,则转移电子的数目为(用  表示),需消耗标准状况下氧气的体积为
表示),需消耗标准状况下氧气的体积为  。
。



