溶液pH的定义 知识点题库
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( )

A . a、c两点溶液的导电能力相同
B . b点溶液中c(H+)+c(NH3•H2O)=c(OH﹣)
C . 用等浓度NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液体积Vb=Vc
D . a、b、c三点溶液水的电离程度a>b>c
实验测得某些食物的近似pH如表,下列说法正确的是( )
食物 | 泡菜 | 葡萄 | 番茄 | 苹果 | 牛奶 | 玉米粥 |
pH | 3.4 | 4.2 | 4.4 | 3.1 | 6.5 | 7.8 |
A . 牛奶和玉米粥均属于碱性食物
B . 胃酸过多的人应少食泡菜
C . 番茄的酸性比苹果强
D . 用湿润的pH试纸蘸取葡萄汁测其pH
pH的大小,可用来表示溶液的 的强弱.溶液的 性越强,pH越大;溶液的 性越强,pH越小.溶液中H+或OH﹣离子浓度 1mol/L时,一般不用pH表示溶液的酸碱性,而直接用 表示.测定溶液pH通常可用pH试纸,它是用 混合溶液浸制而成.若精确测定溶液pH,则应用 .
为了研究土壤的酸碱性,某学生做了如下实验:将一定体积的蒸馏水加入一定质量的土壤中,充分搅拌后,过滤并留取滤液,测滤液的pH后向滤液中滴加氨水,每加入2mL氨水就搅拌均匀并测量溶液的pH,所得实验记录如下:
加氨水体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 |
溶液的pH | 4 | 4 | 4 | 4 | 6 | 8 | 10 | 10 | 10 |
利用上述记录的数据,以加入的氨水体积为横坐标、pH为纵坐标绘制曲线图,并根据曲线图回答下列问题:
-
(1) 所测土壤的酸碱性如何?
-
(2) 所用氨水的pH和c(OH﹣)分别为多少?
-
(3) 为使该滤液呈中性,所加入氨水的恰当体积是多少?
在农业生产中,各种作物生长都对土壤的pH范围有一定的要求(见下表)
作物 | 水稻 | 小麦 | 玉米 | 大豆 | 油菜 | 棉花 | 马铃薯 | 洋葱 |
pH | 6~7 | 6.3~7.5 | 6~7 | 6~7 | 6~7 | 6~8 | 4.8~5.5 | 6~7 |
某课外小组同学研究土壤的酸碱性,操作如下:将一定体积的蒸馏水加入一定质量的土壤中,充分搅拌后,过滤并留取滤液,测滤液的pH后向滤液中滴加氨水,每加入2mL氨水就搅拌均匀并测量溶液的pH,绘制出下图.
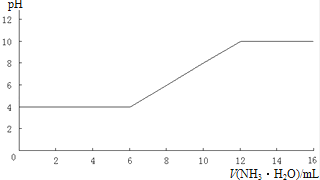
根据上图回答:
(1)在没有对土壤改良前,该土壤最可能种植的作物名称是 .
(2)该土壤滤液中c(H+)= .
(3)从上图还能得到的信息有 (答出一条即可).
下列溶液一定呈中性的是( )
A . pH=7的溶液
B . c(H+)=c(OH﹣)=10﹣6mol/L溶液
C . 使石蕊试液呈紫色的溶液
D . 酸与碱恰好完全反应生成正盐的溶液
下列各物质的溶液物质的量浓度均为0.1mol/L:①HCl;②NaOH;③Na2CO3;④NH4Cl;⑤CH3COONa;⑥Ba(OH)2;⑦KCl.它们pH按由小到大的排列顺序为( )
A . ⑥②③⑤⑦④①
B . ①④⑦③⑤②⑥
C . ①④⑤③⑦②⑥
D . ①④⑦⑤③②⑥
下列说法正确的是( )
A . pH越小,溶液的酸性越强
B . pH小于5.6的雨水是酸雨
C . 胃酸过多的病人在空腹时最好多喝一些柠檬汁
D . 用pH试纸伸入某溶液中测定其pH
牙齿中含珐琅质,它本身是一种坚硬物质,不容易受损.但口腔内酸性过强,酸性物质就会与珐琅质发生反应,从而损害珐琅质的表面而形成蛀牙.如图为没有护理牙齿与有护理牙齿人的口腔在饭后pH的变化情况.下列说法正确的是( )

A . 饭后六十分钟时牙齿最易被腐蚀
B . 饭后十分钟时口腔内的酸性最弱
C . 经护理后口腔内的酸性增强
D . 经护理后口腔内的酸性减弱
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )
A . pH=4的醋酸中:c(H+)=4.0mol•L﹣1
B . 饱和小苏打溶液中:c(Na+)=c(HCO3﹣)
C . 饱和食盐水中:c(Na+)+c(H+)=c(Cl﹣)+c(OH﹣)
D . pH=12的纯碱溶液中:c(OH﹣)=1.0×10﹣2mol•L﹣1
下列实验过程中,溶液的pH增大的是( )
A . 向NaOH溶液中加水
B . 向NaCl溶液中滴加稀盐酸
C . 向NaOH溶液中滴加稀盐酸
D . 向稀盐酸中滴加NaOH溶液
相同物质的量浓度的下列物质的稀溶液中,pH最小的是( )
A . 乙醇
B . 乙酸
C . 碳酸钠
D . 碳酸
酸与碱完全中和时( )
A . 溶液一定呈中性
B . 溶液的pH一定为7
C . 酸与碱的物质的量一定相等
D . 酸所能提供的H+与碱所能提供的OH-的物质的量一定相等
关于浓度均为0.1mol·L-1的三种溶液:①氨水 ②盐酸③氯化铵溶液,下列说法错误的是( )
A . 溶液的pH:①>③>②
B . 水电离出的(H+):③>②>①
C . ①和②等体积混合后的溶液:c(NH4+)+c(H+)=c(Cl-)+c(OH-)
D . ①和③等体积混合后的溶液呈碱性:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
常温下,下列说法正确的是( )
A . pH = 4 的醋酸中c(H+)= 4.0 mol/L
B . pH = 2的盐酸与pH = l的盐酸中c(H+)之比为1:10
C . pH= 1的盐酸与pH= 1的硫酸中c(H+)之比为l∶2
D . 0.1 mol/L的醋酸与0.2 mol/L的醋酸中c(H+)之比为l∶2
常温下,将甲酸和氢氧化钠溶液混合,所得溶液pH=7,则此溶液中( )
A . c(HCOO-)>c(Na+)
B . c(HCOO-)<c(Na+)
C . c(HCOO-)=c(Na+)
D . 无法确定c(HCOO-)与c(Na+)的关系
用0.1000mol/L的NaOH溶液分别滴定体积均为10.00mL、浓度均为0.1000mol/L的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液的电导率(电导率越大表示溶液导电性越强)变化如图所示.下列说法正确的是( )

A . 曲线①代表向盐酸中滴加 B . A点溶液的
B . A点溶液的 小于C点溶液的
小于C点溶液的 C . D点溶液中:
C . D点溶液中: D . 随着
D . 随着 溶液的加入,曲线①逐渐向②靠拢,说明电解质溶液的电导率只与离子浓度大小相关
溶液的加入,曲线①逐渐向②靠拢,说明电解质溶液的电导率只与离子浓度大小相关
 B . A点溶液的
B . A点溶液的 小于C点溶液的
小于C点溶液的 C . D点溶液中:
C . D点溶液中: D . 随着
D . 随着 溶液的加入,曲线①逐渐向②靠拢,说明电解质溶液的电导率只与离子浓度大小相关
溶液的加入,曲线①逐渐向②靠拢,说明电解质溶液的电导率只与离子浓度大小相关
下列说法正确的是( )
A . 用广泛pH试纸测得新制氯水的pH为2]
B . 取一根洁净的铂丝,放在酒精灯外焰上灼烧至与原来的火焰颜色相同时为止,再蘸取少量试液,在外焰上灼烧,若火焰呈黄色,则试液中一定含有Na+
C . 配制100mL0.1mol/LNaCl溶液时,若未将洗涤液注入容量瓶,则所配溶液浓度偏大
D . 取少量某溶液于试管中,加入少量NaOH溶液,若未产生能使湿润的红色石蕊试纸变蓝的气体,则该溶液一定不含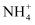
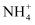
常温下,稀释0.1 mol/LCH3COONa溶液,如图的横坐标表示加水的量,则纵坐标可以表示( )
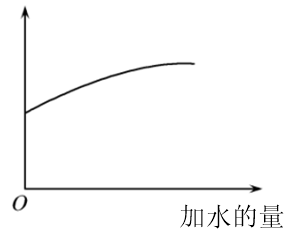
A . Kb(CH3COO-)
B . c(CH3COO-)
C . n(CH3COOH)
D . 溶液pH
25℃时,向
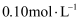 氨水(
氨水( )中逐滴加入
)中逐滴加入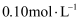 的盐酸,溶液pH随所加盐酸体积变化如图。下列说法错误的是( )
的盐酸,溶液pH随所加盐酸体积变化如图。下列说法错误的是( )

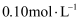 氨水(
氨水( )中逐滴加入
)中逐滴加入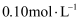 的盐酸,溶液pH随所加盐酸体积变化如图。下列说法错误的是( )
的盐酸,溶液pH随所加盐酸体积变化如图。下列说法错误的是( )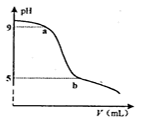
A . a点处存在 B . b点处存在
B . b点处存在 C . 由a→b,溶液中
C . 由a→b,溶液中 持续增大
D .
持续增大
D . 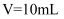 时,存在
时,存在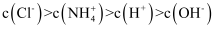
 B . b点处存在
B . b点处存在 C . 由a→b,溶液中
C . 由a→b,溶液中 持续增大
D .
持续增大
D . 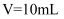 时,存在
时,存在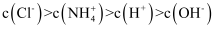
最近更新



