酯化实验 知识点题库

①新制Cu(OH)2与乙醛反应; ②银镜反应; ③溴乙烷的水解;
④由乙醇制乙烯; ⑤乙酸和乙醇反应制乙酸乙酯;⑥乙酸乙酯的水解
(2)配制银氨溶液时,把氨水滴入硝酸银溶液的操作关键是 ,丙醛与银氨溶液反应的化学方程式是: .在澄清的苯酚钠溶液中通入CO2气体,溶液浑浊,其反应方程式是:
 2CH3CHO+2H2O;取代反应
D . CH3COOH+CH3CH2OH
2CH3CHO+2H2O;取代反应
D . CH3COOH+CH3CH2OH 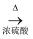 CH3COOCH2CH3+H2O;酯化反应也属于取代反应
CH3COOCH2CH3+H2O;酯化反应也属于取代反应
 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
回答下列问题:
-
(1) 写出A的电子式,A的结构简式。
-
(2) B、D分子内含有的官能团分别是、(填名称)。
-
(3) 写出下列反应的反应类型:①,②,④。
-
(4) 写出下列反应的化学方程式:
①;
②;
④。

-
(1) 反应开始前试管B中加入的试剂是,反应结束后试管B中上层液体的主要成分是。
-
(2) 向试管A中加入试剂时,浓硫酸应在加入乙醇之后再加入,目的是。
-
(3) 制取乙酸乙酯的化学方程式为。
-
(4) 插入试管B中的干燥管的作用是。
-
(5) 从试管B中分离出粗产品乙酸乙酯(含乙酸,乙醇和水),采用的分离方法是,使用CaO可以除去粗产品中的杂质,最后采用的方法可得到较纯净的乙酸乙酯。
 制备乙酸乙酯
B .
制备乙酸乙酯
B .  构成原电池
C .
构成原电池
C .  检验有无二氧化碳生成
D .
检验有无二氧化碳生成
D .  检查装置气密性
检查装置气密性

-
(1) 向试管中加入2mL10%氢氧化钠溶液,滴加4-5滴5%硫酸铜溶液,振荡后加入2mL10%的E的溶液,加热,可观察到的现象是。
-
(2) 写出C和F在浓H2SO4作用下生成G的化学方程式,该反应的类型是。
-
(3) 已知D和F在催化剂作用下反应也能生成G,写出该反应的化学方程式。
-
(4) 下列说法错误的是。
a.要确定A已发生部分水解,先将水解液中和成碱性,再用银氨溶液和碘水分别检验
b.有机物B,C,D和G均能使酸性KMnO4溶液褪色
c.将足量的D通入溴水中,可以观察到溴水褪色,溶液分层
d.某烃X的相对分子质量是D,H之和,则X能与溴水发生加成反应
-
(5) 写出比G少一个碳原子的同系物的可能结构简式。
主反应:CH3COOH+C2H5OH  CH3COOC2H5+H2O
CH3COOC2H5+H2O
副反应:2CH3CH2OH  CH3CH2OCH2CH3(乙醚)+H2O
CH3CH2OCH2CH3(乙醚)+H2O
CH3CH2OH  CH2=CH2↑+H2O
CH2=CH2↑+H2O
根据查得的资料设计了下图所示的装置(夹持装置忽略)制取纯净的乙酸乙酯。

步骤如下:
①在图1的三口烧瓶中加入3mL乙醇,边摇动边慢慢加入3mL浓硫酸,在分液漏斗中装入3:2的乙醇和乙酸混合液。
②油浴加热三口烧瓶至一定温度,然后把分液漏斗中的混合液慢慢地滴入三口烧瓶里并保持反应混合物在一定温度。
③反应一段时间后,向锥形瓶中缓慢加入饱和Na2CO3溶液,并不断摇动,分层后进行分液。
④用饱和食盐水和氯化钙溶液洗涤酯层,再分液,在酯层加入干燥剂干燥得粗乙酸乙酯。
⑤将粗乙酸乙酯转入图2的仪器A中,在水浴中加热,收集74~80℃的馏分即得纯净的水果香味无色透明液体。
根掲题目要求回答:
-
(1) 在实验中浓硫酸的作用;混合液加热前都要加入碎瓷片,作用是。
-
(2) 歩驟②中油浴加热保持的一定温度范围,原因是。
-
(3) 图2中仪器A的名称是,冷凝管中冷水从(填a或b)口进入。
-
(4) 步骤③和④中都用到了分液操作,该操作用到的主要玻璃仪器是,在分液操作时,上下两层液体移出的方法是。
-
(5) 步骤④中干燥乙酸乙酯,可选用的干燥剂为(填字母)。
a.五氧化二磷
b.无水Na2SO4
c.碱石灰


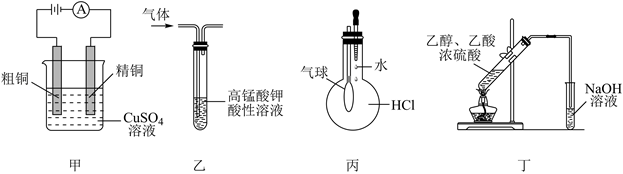
 ),是常用的解热镇痛药。合成原理:
),是常用的解热镇痛药。合成原理:

查阅资料:
阿司匹林:相对分子质量为180,分解温度为128~135℃,溶于乙醇、难溶于水;
水杨酸:相对分子质量为138,溶于乙醇、微溶于水;
乙酸酐:相对分子质量为102,无色透明液体,遇水形成乙酸。

制备过程:
①如图1向三颈烧瓶中加入3.45g水杨酸、新蒸出的乙酸酐20mL(ρ=1.08g·mL-1),再加10滴浓硫酸反复振荡后,连接回流装置,搅拌,70℃加热半小时。
②冷却至室温后,将反应混合液倒入100mL冷水中,并用冰水浴冷却15min,用图2装置减压抽滤,将所有晶体收集到布氏漏斗中。抽滤过程中用少量冷水多次洗涤晶体,继续抽滤,尽量将溶剂抽干,得到乙酰水杨酸粗品。
提纯过程(重结晶法):
③将粗产品转至烧瓶中,装好回流装置,向烧瓶内加入100mL乙酸乙酯和2粒沸石,加热回流,进行热溶解。然后趁热过滤,冷却至室温,抽滤,洗涤,干燥,得无色晶体状乙酰水杨酸。
-
(1) 图1装置中仪器A的名称是。
-
(2) 步骤①中加热宜采用,冷凝回流过程中外界的水可能进入三颈烧瓶,导致发生副反应(用化学方程式作答),降低了水杨酸的转化率。
-
(3) 步骤②用冷水洗涤晶体的目的是,用图2装置减压抽滤后的操作是。
-
(4) 步骤③中肯定用不到的装置是(填序号)。

重结晶时为了获得较大颗粒的晶体产品,查阅资料得到如下信息:

a.不稳定区出现大量微小晶核,产生较多小颗粒的晶体
b.亚稳过饱和区,加入晶种,晶体生长
c.稳定区晶体不可能生长
由信息和已有的知识分析,从温度较高浓溶液中获得较大晶体颗粒的操作为。
-
(5) 最终称量产品质量为2.61g,则所得乙酰水杨酸的产率为%(精确到0.01)。
-
(1) 检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2 , 加热,其现象是。
-
(2) 葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式。
C6H12O6(葡萄糖)
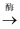 2+2C2H5OH
2+2C2H5OH -
(3) 葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用右图所示装置制备乙酸乙酯:
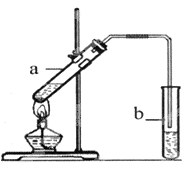
①试管a中生成乙酸乙酯的化学方程式是 。
②实验开始时,试管b中的导管不伸入液面下的原因是。
③若分离出试管b中生成的乙酸乙酯,需要用到的仪器是(填序号)。
a. 漏斗 b. 分液漏斗 c. 长颈漏斗
-
(4) 某有机物的结构简式为HOOC—CH=CHOH。验证该有机物中含有-COOH官能团常采用的方法是,产生的现象为。

回答下列问题:
-
(1) 反应①的反应类型为,G的名称是,F中含氧官能团的名称是。
-
(2) 下列关于物质B的说法正确的是____(填正确答案标号)A . B为苯的同系物 B . 物质B可用于萃取碘水中的碘 C . 一定条件下,1molB最多能与4mol
 发生加成
D . B分子中最多有3个碳原子共直线
发生加成
D . B分子中最多有3个碳原子共直线
-
(3) 检验H在稀硫酸作用下是否完全反应,所需要的试剂是,检验H在稀硫酸作用下的反应产物F的实验操作是。
-
(4) 某化学课外小组设计了如下图所示的制取E的装置(加热及夹持仪器已略去)。

①上述装置的锥形瓶中加入的试剂是,其作用是(填正确答案标号);
A.中和G
B.和D反应并溶解G
C.E在所加试剂中的溶解度比在水中更小,有利于分层析出
D.加速E的生成,提高其产率
②实验过程中需要小火均匀加热三颈烧瓶,其主要理由是。
-
(5) 符合下列条件的E的同分异构体有种。
①苯环上有两个取代基
②能与碳酸氢钠溶液发生反应
③分子结构中只含有一个甲基



