蒸馏的原理、方法、操作及其应用 知识点题库
提纯下列物质主要采用了哪种操作.
A.溶解、过滤 B.过滤 C.蒸发、结晶 D.结晶
1)从食盐水中分离出食盐;选 .
2)从碳酸钠和碳酸钙的混合物中提取碳酸钙;选 .
3)从KCl和MnO2 混合物中分离出KCl;选 .
4)从硝酸钾和氯化钠的混合物中分离出硝酸钾;选 .
规范的操作是实验成功的前提,下列实验操作正确的是( )
A . 实验完毕后,实验过程中剩余的试剂都应该放回原试剂瓶
B . 蒸发饱和食盐水,蒸发皿必须放在石棉网上,用酒精灯的外焰加热
C . 没有腐蚀性的药品可直接放在电子秤上称量,有腐蚀性的应放在烧杯中称量
D . 玻璃管与胶皮管连接时,将玻璃管一端用水润湿,稍用力转动插入胶皮管中
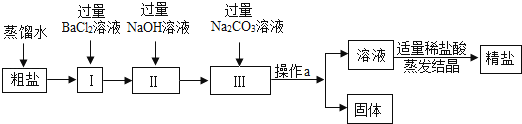
粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(Na2SO4、CaCl2、MgCl2).现以粗盐为原料制取精盐,生产过程如图所示
-
(1) 写出I中发生反应的化学方程式 .加入过量BaCl2溶液的目的是.
-
(2) 操作a的名称是 ,该操作需要用到的玻璃仪器主要有:烧杯、、玻璃棒.
-
(3) 加入适量稀盐酸的作用是除去溶液中的 、 (填化学式).
-
(4) 在加热蒸发过程中,要用玻璃棒不断地搅拌,其目的是.
下列实验操作基本正确的是( )
A . 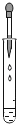 B .
B . 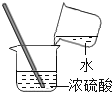 C .
C . 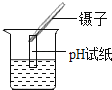 D .
D . 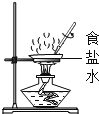
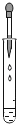 B .
B .  C .
C .  D .
D . 
下列实验操作正确的是( )
A.制取蒸馏水时,将湿度计水银球插入水中
B.过滤时,将玻璃棒靠在三层滤纸的一边
C.实验室制取并用排水法收集氧气,停止加热时,先熄灭酒精灯,再移出导气管
D.在“粗盐中难溶性杂质的去除”实验中,将蒸发皿中的溶液直接蒸干
A . 制取蒸馏水时,将湿度计水银球插入水中
B . 过滤时,将玻璃棒靠在三层滤纸的一边
C . 实验室制取并用排水法收集氧气,停止加热时,先熄灭酒精灯,再移出导气管
D . 在“粗盐中难溶性杂质的去除”实验中,将蒸发皿中的溶液直接蒸干
通过晾晒海水或煮井盐水、盐湖水等,可以蒸发除去水分,得到粗盐,粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等).通过如图所示过程,使粗盐得到初步提纯:

-
(1) 操作a的名称是 , 该操作中要用到的玻璃仪器有烧杯、玻璃棒、 .
-
(2) 通过蒸发M溶液中的水分使之浓缩结晶,想一想,能否采用降低溶液温度的方法来达到同一目的? (填“能”或“否”).理由是 .
-
(3) 在蒸发操作时,当蒸发皿中出现较多量固体时,应 ,利用蒸发皿的余热使滤液蒸干.
-
(4) 某同学欲通过实验探究所得精盐是否是纯净物,进行了如下实验.
实验步骤
实验现象
实验结论
取一定量精盐样品于试管中,加水使之完全溶解,并向其中加入
①
②
写出一个相应的化学方程式:③
结论:该精盐样品为混合物
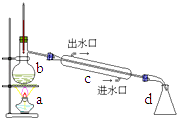
在实验室可用如图装置制取蒸馏水.回答下列问题:
-
(1) 写出装置图中仪器的名称:
B;c;d
-
(2) 仪器C的作用是;冷水由端流入,由端流出;
-
(3) 水在中由液态变气态,在中由气态变为液态.
水是人类生活不可缺少的物质。日常生活中不少人喜欢喝纯净水,市售的纯净水有些就是蒸馏水。有关这类纯净水的下列说法正确的是( )
A . 它是纯天然饮品,不含任何化学物质
B . 它清洁、纯净,长期饮用对健康有益而无害
C . 它含有人体所需的矿物质和多种微量元素
D . 它可以通过自来水加热产生的水蒸气冷却而获得
海水淡化可采用分离技术。如下图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的氯化钠不能通过淡化膜,从而得到淡水。对加压后右侧海水成分进行分析,正确的是( )
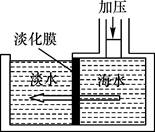
A . 溶质质量增加
B . 溶剂质量减少
C . 溶液质量不变
D . 溶质质量分数减少
净化水的以下操作,其中净化程度最高的是( )
A . 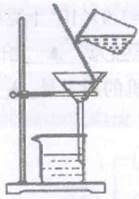 B .
B .  C .
C .  D .
D . 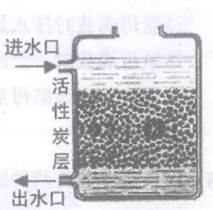
 B .
B .  C .
C .  D .
D . 
将物质从水中分离出来的方法通常有:①沉淀②过滤③结晶④蒸馏。要完成下列物质的分离,请你选择合适的方法
-
(1) 除去食盐水的溶质得到纯净水 ;
-
(2) 彻底除去黄河水中的泥浆 ;
-
(3) 获得配置生理盐水所需的纯净水。
分离和提纯的方法很多,常用的方法有过滤、蒸发结晶、蒸馏等,请用以上分离方法填空。除去河水的泥沙可用的方法,从食盐水中得到食盐晶体可用的方法,从自来水中得到蒸馏水可用的方法。
下列实验中,实验原理和主要操作方法都符合实验目的是( )
| 选项 | 实验目的 | 实验原理 | 主要操作方法 |
| A | 除去粗盐中的泥沙 | 各成分的溶解性差异 | 蒸发 |
| B | 分离水与酒精的混合物 | 各成分的密度差异 | 蒸馏 |
| C | 鉴别稀盐酸和稀硫酸 | 酸根离子的化学性质差异 | 加碳酸钠溶液,观察产生气泡快慢 |
| D | 除去FeSO4、CuSO4混合溶液中的CuSO4 | 金属活动性差异 | 加过量铁粉,充分反应后过滤 |
A . A
B . B
C . C
D . D
在实验室中,常用到以下方法:①蒸发溶剂、②冷却热饱和溶液、③溶解过滤、④蒸馏。将食盐水中的食盐分离出来可以用,将酒精溶液中的酒精和水分离出来可以用。 (用序号填空)
实验室通常用蒸馏的方法制取蒸馏水。如图是制取蒸馏水的实验装置,请回答下列问题:

-
(1) 在实验中,加热前在烧瓶中加几粒沸石(或碎瓷片), 目的是;
-
(2) 实验时,冷凝水应从(填“A“或“B")通入;
-
(3) 图2是简易装置,烧杯内冷水的作用.
在进行蒸馏实验时,常在蒸馏烧瓶中加入少量的小石粒,其目的是( )。
A . 增加装置的稳定性
B . 便于观察实验现象
C . 有利于液体的汽化
D . 防止液体的暴沸
①某一食盐饱和溶液的质量是12克,把它蒸干后,得食盐3.2克。该实验溶液的质量分数是(保留一位小数);②将物质从水中分离出来的方法有和等(任选两种)
石墨烯之父海姆带领的科研团队研制出氧化石墨烯薄膜制成“筛子”,能够很好地筛掉海水中的盐类物质。当海水流过该膜时,钠离子和氯离子被水分子包裹而不能通过,独立的水分子却能通过(如下图)。下列关于氧化石墨烯膜“筛掉”氯化钠的说法错误的是( )
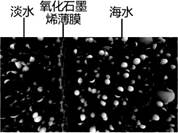
A . “筛掉”氯化钠过程类似于过滤操作
B . 该过程可应用于海水蒸馏
C . 该过程属于物理变化
D . 右侧海水的溶质的质量分数增大
海水中蕴含丰富的资源。
-
(1) 海水淡化是解决淡水资源不足的重要方法。下列方法中, 可以使海水变为淡水的是 (填字母序号)A . 滤纸过滤 B . 吸附 C . 沉降 D . 蒸馏
-
(2) 从海水中提炼出来的重水(D2O)可作原子能反应堆的中子减速剂和热传热介质。重水中重氢原子(D)的相对原子质量是2,则重水中氢元素的质量分数为 。
-
(3) 从海水中制备纯碱和金属镁的流程如图所示:
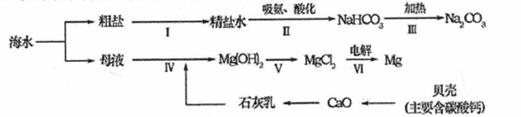
回答下列问题:
①步骤V中所加试剂是
②写出由贝壳得到CaO的化学方程式
如图所示为实验室常用的蒸馏装置。下列说法中错误的是( )
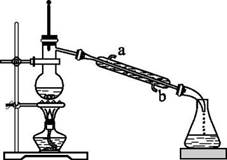
A . 蒸馏时蒸馏烧瓶中放几粒沸石,是为了防止加热时液体暴沸
B . 温度计的水银球要位于蒸馏烧瓶的支管口处
C . 冷凝水要从a口进入,b口流出
D . 实验开始时,先接通冷凝水,再点燃酒精灯加热蒸馏烧瓶
最近更新



