分解反应及其应用 知识点题库
在下列变化中,属于分解反应的是( )
A . 硫在氧气中燃烧
B . 石蜡在空气中燃烧
C . 高锰酸钾受热分解
D . 镁带在空气中燃烧
下列反应既不属于分解反应,也不属于化合反应的是( )
A . 镁+氧气  氧化镁
B . 过氧化氢
氧化镁
B . 过氧化氢 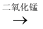 水+氧气
C . 水
水+氧气
C . 水 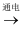 氢气+氧气
D . 蜡烛+氧气
氢气+氧气
D . 蜡烛+氧气  二氧化碳+水
二氧化碳+水
 氧化镁
B . 过氧化氢
氧化镁
B . 过氧化氢 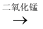 水+氧气
C . 水
水+氧气
C . 水 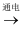 氢气+氧气
D . 蜡烛+氧气
氢气+氧气
D . 蜡烛+氧气  二氧化碳+水
二氧化碳+水
下列反应属于分解反应的是( )
A . 过氧化氢 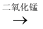 水+氧气
B . 铁+氧气
水+氧气
B . 铁+氧气  四氧化三铁
C . 铝+氧气水
四氧化三铁
C . 铝+氧气水  三氧化二铝(氧化铝)
D . 石蜡+氧气
三氧化二铝(氧化铝)
D . 石蜡+氧气  水+二氧化碳
水+二氧化碳
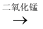 水+氧气
B . 铁+氧气
水+氧气
B . 铁+氧气  四氧化三铁
C . 铝+氧气水
四氧化三铁
C . 铝+氧气水  三氧化二铝(氧化铝)
D . 石蜡+氧气
三氧化二铝(氧化铝)
D . 石蜡+氧气  水+二氧化碳
水+二氧化碳
下列变化中,既不属于化合反应又不属于分解反应的是( )
A . 蜡烛+氧气  水+二氧化碳
B . 氯酸钾
水+二氧化碳
B . 氯酸钾 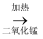 氯化钾+氧气
C . 碳+氧气
氯化钾+氧气
C . 碳+氧气  二氧化碳
D . 硫+氧气
二氧化碳
D . 硫+氧气  二氧化硫
二氧化硫
 水+二氧化碳
B . 氯酸钾
水+二氧化碳
B . 氯酸钾 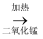 氯化钾+氧气
C . 碳+氧气
氯化钾+氧气
C . 碳+氧气  二氧化碳
D . 硫+氧气
二氧化碳
D . 硫+氧气  二氧化硫
二氧化硫
下列关于化学反应类型的叙述中,正确的是( )
A . 凡是生成盐和水的反应都是中和反应
B . 复分解反应一定没有单质参加
C . 生成一种单质和一种化合物的反应一定是置换反应
D . 分解反应的生成物不一定是单质
下列化学反应中属于是分解反应的是( )
A . 铝+氧气  氧化铝
B . 氢气+氯气
氧化铝
B . 氢气+氯气  氯化氢
C . 碳酸氢铵
氯化氢
C . 碳酸氢铵  氨气+二氧化碳+水
D . 锌+硫酸→硫酸锌+氢气
氨气+二氧化碳+水
D . 锌+硫酸→硫酸锌+氢气
 氧化铝
B . 氢气+氯气
氧化铝
B . 氢气+氯气  氯化氢
C . 碳酸氢铵
氯化氢
C . 碳酸氢铵  氨气+二氧化碳+水
D . 锌+硫酸→硫酸锌+氢气
氨气+二氧化碳+水
D . 锌+硫酸→硫酸锌+氢气
实验室常用下列装置来制取氧气:

-
(1) 写出图中有标号仪器的名称:①②
-
(2) 装置B可用于实验室制取氧气,写出该反应的化学方程式 ,该反应属于(填基本反应类型)若要收集一瓶较纯净的氧气可选用(填收集装置的字母)。
-
(3) 小明同学用“碎冰冰”包装软塑料管做了如图F的发生装置制氧气,该装置中的液体药品是(填药品名称),无纺布包中的固体药品是,起作用,写出该反应的化学方程式,F装置的优点是可以随时开始和停止反应,装好药品后如何操作使反应开始?。
将一种无色液体A和一种黑色固体B混合能得到另一种无色液体C和无色气体D,E在D中燃烧中剧烈燃烧,火星四射,放出大量的热,生成黑色固体F。则:
-
(1) A的俗名 , F的化学式, D的用途 (写一点即可)。
-
(2) 写出A与B混合得到C与D的符号表达式: 其中B起 作用,此反应属于 反应(填“化合”或“分解”)。
下列获得氧气的方法中不含有分解反应的是:( )
A . 用氯酸钾制氧气
B . 分离液态空气制氧气
C . 用双氧水制氧气
D . 用高锰酸钾制氧气
下列描述的变化不属于分解反应的是( )
A . 用高锰酸钾加热制取氧气
B . 分离液态空气法制取氧气
C . 双氧水和二氧化锰制取氧气
D . 加热铜绿
完成下列反应的文字表达式,并在括号里注明反应是属于化合反应还是分解反应.
电解水:,反应.
写出下列反应的文字表达式,并指明反应类型:
①镁带在空气中燃烧:;反应类型是:;
②电解水:;反应类型是:。
下列关于“物质——在氧气中燃烧的主要现象——所属基本反应类型”的描述正确的是( )
A . 硫——微弱的淡蓝色火焰——化合反应
B . 木炭——发出白光——化合反应
C . 铁——剧烈燃烧,火星四射——氧化反应
D . 蜡烛—发出白光,有水雾出现—化合反应
下列对化学反应类型的判断中,错误的是( )
A . 碳酸→水+二氧化碳(分解反应)
B . 过氧化氢→水+氧气(分解反应)
C . 铁+氧气→四氧化三铁(化合反应)
D . 石蜡+氧气→二氧化碳+水(化合反应)
用“>”、“<”“=”或“≧”填空。
-
(1) 纯净物所含物质的种类混合物所含物质的种类。
-
(2) 分解反应的生成物两种。
-
(3) 盛完全相同氯酸钾固体的A,B,C三支试管,A中加入适量的高锰酸钾,B中加入等量的二氧化锰后加热,则产生O2的速率AC,产生O2质量BC。
下列反应中,属于分解反应的是( )
A . 铁丝+氧气  四氧化三铁.
B . 氢氧化钠+硫酸铜→硫酸钠+氢氧化铜
C . 蜡烛+氧气
四氧化三铁.
B . 氢氧化钠+硫酸铜→硫酸钠+氢氧化铜
C . 蜡烛+氧气  二氧化碳+水
D . 碱式碳酸铜
二氧化碳+水
D . 碱式碳酸铜  氧化铜+水+二氧化碳
氧化铜+水+二氧化碳
 四氧化三铁.
B . 氢氧化钠+硫酸铜→硫酸钠+氢氧化铜
C . 蜡烛+氧气
四氧化三铁.
B . 氢氧化钠+硫酸铜→硫酸钠+氢氧化铜
C . 蜡烛+氧气  二氧化碳+水
D . 碱式碳酸铜
二氧化碳+水
D . 碱式碳酸铜  氧化铜+水+二氧化碳
氧化铜+水+二氧化碳
提升“中国芯”的性能是我国信息产业的当务之急。“中国芯”的核心材料是高纯度的单质硅,工业上制取粗硅的化学方程式为:SiO2+2C  Si+2CO↑,下列说法正确的是( )
Si+2CO↑,下列说法正确的是( )
 Si+2CO↑,下列说法正确的是( )
Si+2CO↑,下列说法正确的是( )
A . 单质硅结构和金刚石类似,由分子构成
B . 该反应的基本类型为分解反应
C . 在此反应中硅元素的化合价降低
D . 硅元素在地壳中的含量最多
阅读下面科普短文。
酒精,又名乙醇,化学式为C2H5OH,在常温常压下是一种易燃、易挥发的无色液体,有特殊香味,能与水以任意比互溶。乙醇用途广泛,可用于制造饮料、香精、染料、燃料等。工业上常用淀粉发酵法制酒精,其主要流程如下: 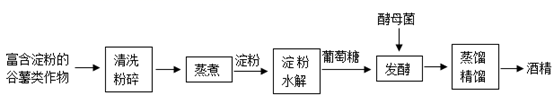
医用酒精主要用于消毒、杀菌。酒精浓度过高时,会在细菌表面形成一层保护膜,阻止其进入细菌体内,不能彻底杀死细菌;浓度过低时,不能将细菌体内的蛋白质凝固,同样无法将细菌杀死。因此,浓度适当的酒精溶液,才能达到良好的杀菌效果。经实验测定,酒精杀菌效果较好的浓度范围是50%-80%,常用的医用浓度为75%。下表是不同浓度酒精杀灭细菌所需的时间。
| 酒精浓度 | 金黄色葡萄球菌 | 溶血性链球菌 | 大肠杆菌 |
| 40% | 4小时 | 2分钟 | 2分钟 |
| 50% | 2小时 | 20秒 | 20秒 |
| 60% | 30分钟 | 10秒 | 20秒 |
| 70% | 5分钟 | 10秒 | 30秒 |
| 80% | 2分钟 | 10秒 | 1小时 |
| 90% | 30分钟 | 5分钟 | 15小时 |
| 100% | 7天 | 15分钟 | 24小时 |
乙醇还可以通过各种植物纤维发酵制得,将其按一定比例与汽油混合,即成为一种新型替代能源——乙醇汽油。乙醇汽油作为汽车燃料,可节省石油资源,减少汽车尾气对空气的污染,还可以促进农业生产。
依据文章内容回答下列问题。
-
(1) 乙醇属于(填“有机物”或“无机物”)。
-
(2) 淀粉发酵法制酒精时,发生的主要反应为:C6H12O6
 2C2H5OH+2CO2↑,此反应属于基本反应类型中的反应。
2C2H5OH+2CO2↑,此反应属于基本反应类型中的反应。
-
(3) 酒精浓度为时,杀灭金黄色葡萄球菌速度最快。
-
(4) 酒精杀灭溶血性链球菌所需时间与其浓度的关系是。
-
(5) 下列说法正确的是(填序号)。
A淀粉发酵法制酒精的过程,只发生化学变化
B使用酒精做消毒剂时,其浓度越大杀菌速度越快
C乙醇汽油的使用,对空气质量的改善有一定作用
D酒精用途广泛,发展前景广阔
已知下列四个反应在一定条件下都能发生,其中属于分解反应的是( )
A . 氧化汞  汞+氧气
B . 碳酸钙+盐酸→氯化钙+二氧化碳+水
C . 蜡烛+氧气
汞+氧气
B . 碳酸钙+盐酸→氯化钙+二氧化碳+水
C . 蜡烛+氧气 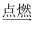 二氧化碳+水
D . 木炭+氧气
二氧化碳+水
D . 木炭+氧气 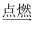 二氧化碳
二氧化碳
 汞+氧气
B . 碳酸钙+盐酸→氯化钙+二氧化碳+水
C . 蜡烛+氧气
汞+氧气
B . 碳酸钙+盐酸→氯化钙+二氧化碳+水
C . 蜡烛+氧气 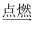 二氧化碳+水
D . 木炭+氧气
二氧化碳+水
D . 木炭+氧气 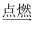 二氧化碳
二氧化碳
甲、乙、丙、丁四种物质在一定的条件下反应,测得反应前后各物质的质量分数如图所示,则有关说法中正确的是( )

A . 该反应为分解反应
B . 甲可能是单质
C . 乙一定是这个反应的催化剂
D . 丙、丁两物质变化的质量比为11:4
最近更新



