合理利用金属资源 知识点
(2)防止金属锈蚀
(3)回收利用废弃金属材料
(4)寻找替代产品
合理利用金属资源 知识点题库
某回收站回收的废金属粉末中含锰(Mn)、金(Au)、铜三种金属。为了回收贵重金属,回收站将有关三种金属随意编号为:A、B、C,并设计了如下回收流程:
(1)A、B、C三种金属的活动性顺序为:>>
(2)C是;B的氧化物的化学式是:。
(3)已知A的硫酸盐中A元素显+2价,请写出步骤①的反应的化学方程式:。
(4)你认为步骤③中所加入的X溶液是。
(5)欲直接从蓝色溶液中制得金属B,可选用的试剂是(填标号)。
a.氢氧化钠溶液 b.氯化钠溶液 c.稀盐酸 d.铁
A、能量变化 | B、环境保护 |
①电解水是将电能转化为化学能 ②化学反应中只有燃烧放热 | ①合理施用农药和化肥 ②不得随意乱扔塑料垃圾 |
C、数字含义 | D、资源节约 |
①Fe2+一个亚铁离子带2个单位正电荷 ②SO3 三氧化硫中含有3个原子 | ①废旧金属回收利用 ②pH试纸用水润湿后然后进行测定其酸碱度 |

回答下列问题:
-
(1) Ⅰ、Ⅱ、Ⅲ都需要进行过滤的操作,过滤用到的玻璃仪器是烧杯、玻璃棒和。溶液A所含的溶质有(填化学式)
-
(2) 写出下列反应的化学方程式:步骤Ⅲ,步骤Ⅴ。
-
(3) 同一久置铜片分别通过途径甲和途径乙最终得到的铜的质量是:途径甲(选填“大于”、“等于”或“小于”)途径乙。
-
(4) 途径甲比途径乙更好的理由是(答一点)。
选项 | 现象或做法 | 解释 |
A | 蚊虫叮咬后可涂抹肥皂水消肿 | 肥皂水呈碱性 |
B | 食品包装袋中充氮气以防腐 | 氮气的化学性质不活泼 |
C | 用洗洁精洗去餐具上的油渍 | 洗洁精能溶解油渍 |
D | 废旧电池不随意丢弃而要回收利用 | 减少环境污染同时节约金属资源 |
-
(1) 衡阳被誉为“有色金属之乡”,金属材料使用极为广泛。保护金属资源的有效途径有(请列举出任意两点):、。
-
(2) 2019年5月河南某市的“水氢动力汽车”成为新闻的热点,再度吸引人们对新能源开发应用的关注。氢气作为新能源,越来越受到人们的重视。
①氢气作为燃料与正在广泛使用的化石燃料相比,有什么优点?(任写一条)。
②你还能举出另一种新能源的例子吗?。
-
(1) 做饭时,有时燃气灶的火焰呈黄色或橙色,锅底出现黑色,这是为什么?
-
(2) 酸雨产生的原因是什么?
-
(3) 回收利用废旧金属的一种作用是什么?

-
(1) 图中标识的物质,属于金属材料是,属于有机合成材料的是。
-
(2) 确定垃圾的成分,是对垃圾进行分类的的前提。纯净水塑料瓶应投入(填“可回收”或“干垃圾”)筒中。
-
(3) 垃圾分类,从我做起。如何做到科学分类处理生活垃圾?。
-
(1) I 化学兴趣小组的同学对“影响铁钉锈蚀快慢的因素”展开了如下探究:
(提出问题)溶液的酸碱性对铁钉生锈的快慢是否有影响?溶液中的阴离子种类对铁钉锈蚀的快慢是否有影响?
(设计实验)按图1装置进行实验,测得装置中氯化铵、硫酸铵溶液上方氧气浓度变化曲线如图2。


上述实验中,氧气浓度下降先陡后缓的原因为。
-
(2) 将规格、材质相同的打磨过的铁钉放入下列不同溶液中,测得有关数据如下表:
溶液中的溶质
氯化铵
硫酸铵
氯化钠
硫酸钠
氢氧化钠
0 min时氧气浓度/%
20.8
20.8
20.8
20.8
20.8
500 min时氧气浓度/%
15.8
17.0
18.6
19.0
19.8
实验前溶液pH
5.31
5.53
7.0
7.0
13.6
实验后溶液pH
7.37
7.99
10.5
10.4
13.8
铁钉锈蚀情况
大量
铁锈
大量
铁锈
少量
铁锈
少量
铁锈
几乎
无锈
(结论与拓展)①实验中溶液上方氧气浓度变化越大,证明铁钉锈蚀速率。
②根据表中数据可知,铁钉在(填“酸”、“碱”或“中”)性溶液中更易锈蚀,其中铁钉在含有(填“氯离子”或“硫酸根离子”)的溶液中锈蚀更快。
-
(3) (拓展应用)化学是把双刃剑,铁制品在使用过程中常常会出现不同程度的锈蚀,会造成资源浪费,但将铁生锈的原理用于食品脱氧时,要求铁能快速生锈从而达到脱氧的目的,因此食品脱氧剂中除了加入铁粉、炭粉外,还可加入。
-
(4) II某实验小组同学欲通过实验探究金属的性质。
(实验目的)证明金属活动性强弱:Al > Cu
(设计并实施实验)小组内的3位同学分别做了下述实验:
实验
现象
甲
将铝片直接放入到稀CuCl2溶液中
一段时间后才出现了预期的实验现象
乙
将用砂纸打磨过的铝片放入稀CuCl2溶液(与甲实验浓度相同)中
十几秒内即观察到明显现象。
丙
将用砂纸打磨过的铝片放入稀CuSO4溶液中
在与乙相同的时间内没有观察到明显现象
对比甲、乙同学的实验,推测甲同学开始时没有观察到明显实验现象的原因是。
-
(5) (提出问题)为什么打磨过的铝片放入到CuCl2溶液和CuSO4溶液中观察到的现象不同呢?
(微观探析)查阅资料可知两个反应的微观示意图如下。
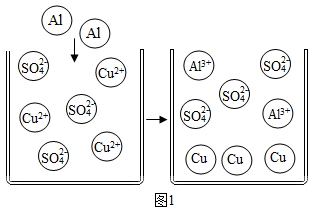

图1反应的化学方程式为;Al和CuCl2溶液、CuSO4溶液反应的微观本质是Al和Cu2+反应生成 Al3+和。
-
(6) (提出猜想)根据上述图示,小组同学提出了如下猜想。
猜想1:产生现象不同的原因是CuCl2溶液比CuSO4溶液中含有的Cu2+浓度大。
猜想2:溶液中Cl-对Al和Cu2+反应有促进作用。
猜想3:溶液中
 对Al和Cu2+反应有阻碍作用。
对Al和Cu2+反应有阻碍作用。(设计并实施实验)
序号
实验方案及操作
现象
结论
①
乙、丙两位同学取Cu2+浓度相同的CuCl2溶液和CuSO4溶液重复实验。
与上述乙、丙同学实验现象相同
猜想1(填“成立”或“不成立”)
②

在同一时间内,③最快产生现象,②次之,①无明显现象
猜想2成立
-
(7) 甲同学认为通过实验2得到的结论证据不充足,理由是溶液中的微粒对实验可能有干扰。
-
(8) 丙同学通过查阅资料排除了上述干扰,并模仿实验2又设计了一组3支试管的实验,证明了猜想3也成立。请在下列方框中画出实验设计图示。

-
(1) 项目一:调查山西金属矿物的种类
(查阅资料)山西省已发现的矿种达120多种,其中探明资源储量的矿产有63种。铝土矿、镁矿的储量居全国第一位,铁矿储量居全国第四位,此外还有铜矿、银矿、金矿等。金在自然界中以单质形式存在,原因是。
-
(2) 项目二:测定某赤铁矿中铁元素的含量
赤铁矿的主要成分是Fe2O3 , 不同地区的赤铁矿中含铁量不同。同学们在调查过程中获得了当地的一块赤铁矿样品,该赤铁矿中铁元素的含量是多少?
(设计方案)
方案一:还原法。将赤铁矿样品粉碎、称量,在高温条件下用将赤铁矿还原得到金属铁,称量、计算。
方案二:沉淀法。
①将赤铁矿样品粉碎、称量,向其中加入足量,充分反应(样品中的杂质不参加反应),过滤。
②向滤液中加入一定量的NaOH溶液,至不再产生沉淀。
③根据所加NaOH溶液中溶质的质量,计算出赤铁矿样品中铁元素的质量。
-
(3) (交流评价)
①方案二与方案一相比,优点是。
②方案二中加入NaOH溶液后,一定发生反应的化学方程式是。
-
(4) (质疑反思)有同学认为,方案二中利用所加NaOH的质量进行计算,结果不一定准确,原因是,因此应利用沉淀的质量进行计算。
-
(5) (进行实验)同学们根据修改后的方案二进行了实验,测得了该赤铁矿样品中铁元素的含量。
项目三:了解日常生活中金属的利用
金属铝、铁的制品在生活中应用广泛,例如:(举一例)。但每年因为锈蚀,也会造成很多金属的浪费。为减少经济损失、保护金属资源,可采取的措施是防止金属腐蚀、(写一种)。
 B . 广口瓶
B . 广口瓶 C . 坩埚钳
C . 坩埚钳 D . 滴瓶
D . 滴瓶
-
(1) 生活中常见的医疗器材、厨房用具和餐具等,很多都是用不锈钢制造的。这是利用了不锈钢具有很强的抗能力。
-
(2) 铁矿石有多种,写出用磁铁矿(主要成分Fe3O4)炼铁的化学方程式。
-
(3) 某工厂排放的废液中含有Zn(NO3)2和AgNO3 , 为回收金属Ag,设计如下方案:

①B中含有,②气体C是。
-
(4) 保护金属资源的有效途径之一是废旧金属的回收和利用,其意义在于(答出一点即可)。



