稀释浓硫酸 知识点
稀释浓硫酸时要将浓硫酸沿器壁缓缓倒入盛水的烧杯中,并用玻璃棒不断搅拌散热
稀释浓硫酸 知识点题库
关于反应C+2H2SO4(浓)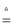 CO2↑+2X↑+2H2O,下列分析错误的是( )
CO2↑+2X↑+2H2O,下列分析错误的是( )
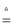 CO2↑+2X↑+2H2O,下列分析错误的是( )
CO2↑+2X↑+2H2O,下列分析错误的是( )
A . X气体排放到空气中,会造成空气污染
B . 该反应说明了碳具有还原性,浓硫酸具有氧化性
C . 硫酸中硫元素与氧元素的质量比为1:2
D . 硫元素的化合价在化学反应前后没有发生改变
现有五种物质:A.氮气 B.浓硫酸 C.熟石灰 D.盐酸 E.尿素,请用合适物质的序号填空.
(1)可用于改良酸性土壤的是 ;(2)可用作保护气的是 ;
(3)可用作化学肥料的是 ;(4)可用作某些气体干燥剂的是 .
下列实验操作中,正确的是( )
A .  稀释浓硫酸
B .
稀释浓硫酸
B .  蒸发食盐水
C .
蒸发食盐水
C .  量取35mL液体
D .
量取35mL液体
D .  测定空气里氧气的含量
测定空气里氧气的含量
 稀释浓硫酸
B .
稀释浓硫酸
B .  蒸发食盐水
C .
蒸发食盐水
C .  量取35mL液体
D .
量取35mL液体
D .  测定空气里氧气的含量
测定空气里氧气的含量
如图是两种稀释浓硫酸的操作:回答下列问题:

(1)B图中锥形瓶内产生的现象是 .产生这一现象的原因是 .
(2)A图中玻璃棒的作用是 .B图中玻璃导管的作用是 .
(3)A中浓硫酸倾倒后要立即盖上瓶塞的原因是什么 .
下列实验操作中,不正确的是( )
A . 倾倒液体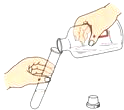 B . 称量NaCl
B . 称量NaCl 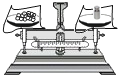 C . 稀释浓硫酸
C . 稀释浓硫酸 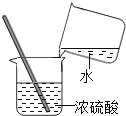 D . 取用固体
D . 取用固体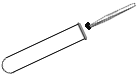
 B . 称量NaCl
B . 称量NaCl  C . 稀释浓硫酸
C . 稀释浓硫酸  D . 取用固体
D . 取用固体
下列叙述正确的是( )
A . 稀释浓硫酸时应将水沿烧杯内壁倒入浓硫酸中,并用玻璃棒不断搅拌
B . 将100g溶质质量分数为98%的浓硫酸稀释为49%,需加水50g
C . 玻璃棒在过滤操作和蒸发操作中所起的作用是一样的
D . 点燃可燃性气体之前检验气体的纯度
合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.


【提出问题】难道NaOH溶液也能与某些金属发生化学反应吗?
【查阅资料】
①铝能与氢氧化钠溶液反应,铁、铜不能与氢氧化钠溶液反应.
②铝与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑(NaAlO  溶于水,溶液现无色)
溶于水,溶液现无色)
-
(1) 【进行猜想】猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有.
猜想3:该合金粉末中除铝外,还含有铁、铜.
-
(2) 【实验探究】下列实验(见表1)仅供选用的试剂:20%的硫酸溶液、30%的NaOH溶液.
表1实验记录
实验步骤
实验现象
结论
①取一定量的合金粉末,加过量的,充分反应后过滤,滤渣备用
粉末部分溶解,并有无色气体放出
合金中一定含有
②取步骤①所得滤渣,加过量,充分反应
滤渣部分溶解,并有无色气体放出,溶液呈浅绿色
合金中一定含有
-
(3) 【得出结论】猜想3成立.
【反思】
①一般来说,活泼金属能与稀硫酸等算反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.铝与稀硫酸发生化学反应的基本类型是反应.
②上述实验中用到的稀硫酸由浓硫酸稀释得到,稀释浓硫酸的方法是:把,并不断搅拌.
③若小明向合金粉末中加入的是足量的稀硫酸,则最终剩余的固体成分是.
【拓展与分析】请你设计一个实验方案,比较铝、铁、铜的金属活动性强弱.
实验室中常需要使用硫酸.
-
(1) 用小木棍蘸少量浓硫酸,放置一会儿后,可观察到;
-
(2) 98%的浓硫酸稀释为稀硫酸时,一定要将沿烧杯壁缓慢地注入盛有的烧杯里,并用搅拌,此时若用手轻轻触碰烧杯外壁,有的感觉;
-
(3) 49g质量分数为20%的稀硫酸与足量锌反应,最多生成氢气的质量是多少?(写出计算过程)
请仔细观察下面溶液的变化并回答问题.

-
(1) 浓硫酸的颜色是.
-
(2) B中溶液变浑浊的原因.
-
(3) 把浓硫酸换成氢氧化钠固体(填“是”或“否”)出现图B中相同现象.
-
(4) 稀硫酸与氯化钡反应的方程式为.
下列是化学实验基本操作的图示.其中正确的是( )
A .  浓硫酸的稀释
B .
浓硫酸的稀释
B .  收集CO2时验满
C .
收集CO2时验满
C . 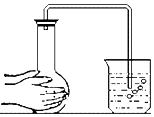 检查装置的气密性
D .
检查装置的气密性
D .  过滤操作
过滤操作
 浓硫酸的稀释
B .
浓硫酸的稀释
B .  检查装置的气密性
D .
检查装置的气密性
D .  过滤操作
过滤操作
用玻璃棒蘸取浓硫酸在白纸上写字,如图.


-
(1) 现象:放置一会儿发现用(填“浓”或“稀”)硫酸在白纸上写的字变黑.
-
(2) 结论:同种酸由于不同,它们的性质不完全相同.
如图图示的实验操作中正确是( )
A .  测溶液pH
B .
测溶液pH
B .  闻气体气味
C .
闻气体气味
C .  除去CO2中的HCl
D .
除去CO2中的HCl
D . 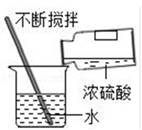 稀释浓硫酸
稀释浓硫酸
 测溶液pH
B .
测溶液pH
B .  闻气体气味
C .
闻气体气味
C .  除去CO2中的HCl
D .
除去CO2中的HCl
D .  稀释浓硫酸
稀释浓硫酸
观察实验图象,得到结论正确的是( )
A . 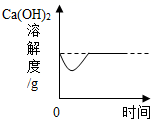 向饱和石灰水中加入少量的CaO
B .
向饱和石灰水中加入少量的CaO
B . 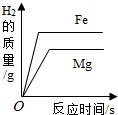 将等质量的镁片和铁片投入到足量稀硫酸中
C .
将等质量的镁片和铁片投入到足量稀硫酸中
C .  向硝酸和硫酸铜的混合溶液中滴加氢氧化钡溶液
D .
向硝酸和硫酸铜的混合溶液中滴加氢氧化钡溶液
D . 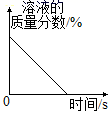 将浓硫酸露置在空气中
将浓硫酸露置在空气中
 向饱和石灰水中加入少量的CaO
B .
向饱和石灰水中加入少量的CaO
B .  将等质量的镁片和铁片投入到足量稀硫酸中
C .
将等质量的镁片和铁片投入到足量稀硫酸中
C .  向硝酸和硫酸铜的混合溶液中滴加氢氧化钡溶液
D .
向硝酸和硫酸铜的混合溶液中滴加氢氧化钡溶液
D .  将浓硫酸露置在空气中
将浓硫酸露置在空气中
下列实验操作中正确的是( )
A . 过滤  B . 稀释浓硫酸
B . 稀释浓硫酸 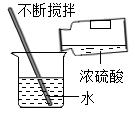 C . 测溶液的pH
C . 测溶液的pH  D . 加热液体
D . 加热液体 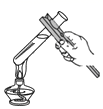
 B . 稀释浓硫酸
B . 稀释浓硫酸  C . 测溶液的pH
C . 测溶液的pH  D . 加热液体
D . 加热液体 
下列实验操作或数据中,正确的是( )
A . 称量10.05g固体  B . 稀释浓硫酸
B . 稀释浓硫酸 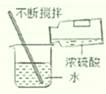 C . 测溶液Ph
C . 测溶液Ph  D . 量取9.5mL液体
D . 量取9.5mL液体 
 B . 稀释浓硫酸
B . 稀释浓硫酸  C . 测溶液Ph
C . 测溶液Ph  D . 量取9.5mL液体
D . 量取9.5mL液体 
下列实验操作正确的是( )
A . 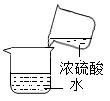 浓硫酸稀释
B .
浓硫酸稀释
B .  液体读数
C .
液体读数
C . 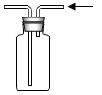 收集氢气
D .
收集氢气
D .  熄灭酒精灯
熄灭酒精灯
 浓硫酸稀释
B .
浓硫酸稀释
B .  液体读数
C .
液体读数
C .  收集氢气
D .
收集氢气
D .  熄灭酒精灯
熄灭酒精灯
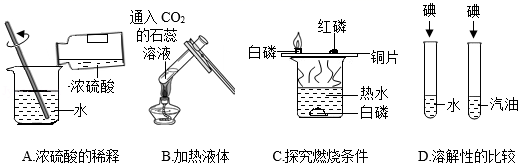
根据如图所示实验回答问题。
-
(1) A实验中沿器壁慢慢注入,并用玻璃棒搅拌的目的是,如果错误的将水注入浓硫酸,会非常危险,原因是。
-
(2) B实验中加热通入CO2后的石蕊溶液,观察到的现象是。
-
(3) C实验中铜片上的白磷燃烧而红磷不燃烧,可以说明燃烧的条件之一是,发生化学反应的方程式是,热水中的白磷也不燃烧,说明燃烧的另一个条件是,该实验主要利用了铜片良好的性,燃着的白磷熄灭后,去掉铜片上的白色固体,可看到铜片表面变黑,该黑色物质是(填化学式)。
-
(4) D实验中碘几乎不溶于水却能溶解在汽油中,说明物质的溶解性与有关。
下列仪器操作不正确的是( )
A . 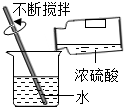 浓硫酸的稀释
B .
浓硫酸的稀释
B .  加热液体
C .
加热液体
C .  滴加液体
D .
滴加液体
D . 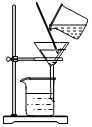 过滤
过滤
 浓硫酸的稀释
B .
浓硫酸的稀释
B .  加热液体
C .
加热液体
C .  滴加液体
D .
滴加液体
D .  过滤
过滤
下列实验操作正确的是( )
A . 滴加液体 B . 稀释浓硫酸
B . 稀释浓硫酸 C . 硫在氧气中烧烧
C . 硫在氧气中烧烧 D . 称量NaOH固体
D . 称量NaOH固体
 B . 稀释浓硫酸
B . 稀释浓硫酸 C . 硫在氧气中烧烧
C . 硫在氧气中烧烧 D . 称量NaOH固体
D . 称量NaOH固体
从安全的角度考虑、下列做法正确的是( )
A . 稀释浓硫酸时,将一定量的水缓慢倒入量取好的浓硫酸中
B . 若不慎将氢氧化钠溶液进入眼中,要先用大量水冲洗、再滴上稀盐酸缓解疼痛
C . 炒菜时油锅着火,应立即向锅中加入凉水灭火
D . 点燃氢气、甲烷气体前要检验气体的纯度
最近更新



