酸雨的产生、危害及防治 知识点题库
化学是人类用以认识和改造物质世界的主要方法和手段之一.
-
(1) 人类生存离不开空气.空气中含量最多的气体是 ,其体积分数是 ;引起温室效应的气体是 ;引起酸雨的主要气体是 .
-
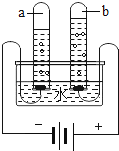
(2) 如图所示的装置可以帮助我们认识水的组成.a试管中的气体是 ,发生反应的化学方程式是 ;检验b试管中气体的方法是 .
-
(3) 化学与医学密切相关,为人类健康做贡献.中国科学家屠呦呦因从中草药中分离出青蒿素(C15H22O5)应用于疟疾治疗,挽救了数百万人的生命而获得了2015年诺贝尔生理学或医学奖.C15H22O5由 种元素组成,碳、氢元素的原子个数比是 ;0.4mol C15H22O5中约含有 个氧原子(用科学记数法表示).
测定时刻 | 6:05 | 6:10 | 6:15 | 6:20 | 6:25 | 6:30 |
p H | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 |
已知:正常雨水的pH约为5.6,酸雨的pH小于5.6.
(1)所取的雨水是否为酸雨?(填“是”或“否”);在测定的期间,雨水水样的酸性随着时间的变化逐渐(填“增强”或“减弱”).
(2)经调查,这一地区有一座燃煤发电厂(生产过程中产生SO2),某同学设计用火碱来吸收生产过程中产生的SO2 , 将其转化成亚硫酸钠(Na2SO3).请你帮他写出该反应的化学方程式: .
(3)若用pH试纸测定雨水的酸碱度,测定方法是: .
工业烟气脱硫就是将烟气中含有的二氧化硫除去.一种采用“双碱法”脱硫的工业流程示意图如图: 
-
(1) 吸收塔中,用NaOH溶液吸收SO2 , 生成和H2O.NaOH溶液喷成雾状能充分吸收SO2的原因是.
-
(2) 沉淀室中,发生反应的化学方程式为.
-
(3) 氧化室中,化学反应的基本类型是反应.
-
(4) 上述流程中,可以循环利用的物质是,有利于节约成本.
-
(1) 溶于雨水会形成酸雨的气体有哪些?酸雨对环境会造成哪些危害?(各答一种即可)
-
(2) 现有一瓶蒸馏水和一瓶稀氯化钾溶液,可用什么简单的办法把它们鉴别开?(注意:在实验室里,任何鉴别都不能尝溶液的味道)
-
(1) 人类目前使用的化石燃料有煤、天然气和.化石燃料的燃烧会排放污染气体,其中就有会引起“酸雨”的主要气体,其化学式为.
-
(2) 天然气是常见的燃料,其燃烧的化学方程式为.
【提出假设】酸雨易对造成危害.
【调查收集资料】通过查阅资料搜集到以下资料.

【交流讨论】造成酸雨的物质主要
来自于:(任写两点)、.
【设计实验方案】以“模拟酸雨的危害”为题进行对比实验.(如下图所示)

实验环境:①天然雨水;②向充满SO2的集气瓶中加少量的水,模拟“酸雨”.
【实验现象】观察一段时间后,各装置里的物质分别发生了变化,就A、B、C三组装置中任选一组描述其对比现象.
【交流反思】
①用pH试纸测定酸雨pH的具体操作方法是.
②同学甲认为:酸雨的腐蚀作用来自于SO2的酸性;同学乙认为:酸雨的腐蚀作用是由于SO2与水等反应生成相应的酸的缘故.你认为的结论正确.为了说明正确的结论,你认为还需要补充的对比实验所用的样品是.
A.蒸馏水B.干燥的SO2气体C.稀硫酸D.其他稀酸溶液
【实际运用】下列控制酸雨的措施合理的是
A.使用脱硫煤B.加高工业烟囱C.开发新能源.

①水银 ②生石灰 ③氢气 ④二氧化硫 ⑤碳酸钙
-
(1) 能够形成酸雨的是
-
(2) 温度计中含有的物质是
-
(3) 未来最清洁的燃料是
-
(4) 石灰石的主要成分是
-
(5) 溶于水放热的是;发生的化学反应方程式为。
-
(1) 造成酸雨的气体是;
-
(2) 实验室中常用的燃料是;
-
(3) 可用于人工降雨的是;
-
(4) 可做净水吸附剂的是;
-
(5) 发酵粉的主要成分之一是;
-
(6) 改良酸性土壤的碱是.
(查阅资料)
①实验室常用亚硫酸钠(Na2SO3)固体与硫酸在常温下反应制SO2气体.SO2是无色有刺激性气味的气体,密度比空气大,溶于水生成亚硫酸(H2SO3);
②SO2能使品红溶液褪色;③海水呈弱碱性;④BaSO3不溶于水,能与盐酸反应;BaSO4不溶于水,也不溶于盐酸.
-
(1) (实验1)制取二氧化硫
实验时先组装好仪器,在加入药品前,还必须进行的实验操作是;
-
(2) 实验室制取SO2可选择的发生装置为;最佳收集装置是(填序号).

-
(3) (实验2)模拟酸雨的形成
实验小组将SO2通入一定量的水后,每隔一定时间,用pH计测定其pH,结果如下表:

(分析讨论)
SO2的水溶液呈性(填“酸”、“碱”);
-
(4) 将新鲜菜叶、铝合金制品、大理石颗粒分别置于上述溶液中,观察到的现象分别是菜叶变黄、铝合金制品表面有气泡、,说明酸雨有腐蚀性;
-
(5) 模拟酸雨样品在空气中放置一段时间后pH减小,原因是SO2与水反应生成的H2SO3被氧气氧化为H2SO4 . 写出H2SO3转化为H2SO4的化学方程式.
-
(6) (提出猜想)同学们对模拟酸雨样品中的溶质进行猜想:
猜想Ⅰ:溶质只含有H2SO3;猜想Ⅱ:溶质只含有H2SO4;猜想Ⅲ:溶质.
-
(7) (实验探究)
向模拟酸雨样品中滴加过量Ba(OH)2溶液,有白色沉淀生成,过滤.
①在滤液中滴加酚酞溶液,溶液呈色.证明滴加的Ba(OH)2溶液已过量.
②向沉淀中加入足量盐酸,沉淀部分溶解.由实验可知猜想符合题意.
-
(8) (拓展延伸)
利用海水脱硫是减少SO2排放的方法之一,海水吸收含硫烟气后,酸性显著增强.
①设计一种检验净化后的烟气中是否含SO2的简单实验方案:.
②吸收含硫烟气后的海水需与大量天然海水混合后才能排放,主要目的是.
-
(1) 多步行,骑单车出行,能有效减少CO2、SO2、CO等气体的排放,这些气体中能引起温室效应的是,会造成酸雨的是。
-
(2) 氢气在空气中燃烧时,产生色火焰,该反应的化学方程式是。混有一定量空气或氧气的氢气遇明火可能会发生爆炸,因此点燃氢气前一定要进行。
-
(3) 奥司他韦(化学式为:C16H28N2O4)是一种治疗流行性感冒的药物,它的一个分子中共含有个原子,其中氢、氧元素的个数比为。
-
(4) 某些工厂用稀硫酸清洗铁制品表面的铁锈(主要成分氧化铁):(填写化学方程式),溶液由无色变为色。
-
(5) 在做铁丝在氧气中燃烧实验时,要预先在集气瓶中装少量或铺一层细砂,是为了.
-
(1) 煤中含有硫元素,燃烧时会产生形成酸雨的主要物质(填化学式),用煤炉取暖时易发生中毒,主要是由于室内(填化学式)不足引起的。
-
(2) 生活中的下列做法,不利于人体健康的是(填字母序号)。
A 食用霉变的花生
B 倡导大家不吸烟
C 食用甲醛溶液浸泡的海产品
-
(3) 某人的早餐有①米饭;②凉拌黄瓜;③茶叶蛋;其中富含蛋白质的是(填序号)。
-
(4) 硬水给生活和生产带来很多麻烦,生活中可用的方法来软化硬水。
-
(5) 我国钢铁年产量很高,但因锈蚀造成的损失也很惊人。工业上常用稀盐酸除去铁锈,该反应的化学方程式为。

回答下列问题:
-
(1) 生铁属于材料(填“金属”或“合成”或”天然")。“高炉气体”中的(填化学式)会导致酸雨,在农村改良酸性土壤最常用(填物质名称)。
-
(2) “煅烧”时:SiO2固体和CaCO3在高温条件下发生反应,生成CO2气体和CaSiO3 , 该反应的化学方程式为 。
-
(3) 生活中铁制品锈蚀的过程,实际上是Fe与空气中氧气、水分等发生化学反应的过程。下列措施不能防止铁制品锈蚀的是 (填标号)。A . 用盐水清洗 B . 涂油、喷漆 C . 久置于酸性环境 D . 镀耐腐蚀的铬层
-
(4) 在工业上用稀盐酸清除铁锈,该反应的化学方程式为。
-
(1) 在“鸡蛋,西红柿、菜子油”中,富含蛋白质的是。
-
(2) 生活中,要处处注意安全,下列灭火方法不合理的。
A图书馆内图书着火—用高压水枪灭火
B电线老化而短路引起火灾—先切断电源,再用干粉灭火器灭火
C炒菜时油锅着火—盖上锅盖
-
(3) 酒精在空气中燃烧时放出大量的热,可用作酒精灯、内燃机等的燃料。写出酒精在空气中燃烧的化学方程式。
-
(4) 工业燃煤会产生大气污染物二氧化硫,二氧化硫在空气中发生反应的生成物溶于雨水,会形成,为减少空气污染,工业上将产生的二氧化硫与氧化钙、氧气共同反应生成硫酸钙,写出其反应的化学方程式。
-
(1) 煤燃烧产生的二氧化碳会导致温室效应,同时二氧化氮、(填化学式)等污染物的产生还会形成酸雨。
-
(2) 为了让煤充分燃烧,可以采用的方法有。
-
(3) 炼铁也是产生二氧化碳的主要原因之一。工业上常用赤铁矿石(主要成分为三氧化二铁)炼铁,请标出三氧化二铁中铁的化合价。
-
(4) 为实现“碳达峰、碳中和”,工业上利用天然气“捕获”二氧化碳,以减少碳排放。该反应的微观示意图如图:在图中横线处相应微粒的图示为____ (填序号)。
 A .
A . B .
B .  C .
C .  D .
D . 
-
(5) 新能源替代化石燃料是实现碳中和的根本措施。氢气被喻为未来最清洁能源:以水为原料,在太阳光照射和催化剂条件下分解产生氢气和氧气,该反应的化学方程式为:。



