离子或物质的共存问题 知识点
共存问题即为各物质是否能发生反应,能发生反应则不能共存,不能发生反应则能共存。解题的关键是复分解反应条件的掌握,若各物质或离子交换成分后生成物中有气体或沉淀或水生成,则能反应,即不能共存。
离子或物质的共存问题 知识点题库
图表资料可以为我们提供许多信息。下列对图表资料的使用能达到目的是( )
A . 根据某元素的原子结构示意图推断该元素原子核内的中子数
B . 根据酸、碱、盐的溶解性表可推知离子间能否在溶液中共存
C . 根据元素的相对原子质量表查出某元素的质量
D . 根据元素周期表查出某元素在地壳中的含量
下列物质在水溶液中能大量共存的是( )
A . HCl、Ca(OH)2、NaNO3
B . NaCl、K2CO3、H2SO4
C . HCl、BaCl2、CuSO4
D . KNO3、NaOH、Na2CO3
在碱性溶液中,一定能大量共存的离子组是( )
A . Al3+、NH4+、SO42﹣、Cl﹣
B . Na+、SO42﹣、K+、CO32﹣
C . K+、Fe2+、Cl﹣、NO3﹣
D . Ba2+、Na+、Cu2+、NO3﹣
对某pH=2的溶液成分进行分析、检测,下列结果合理的是( )
A . KNO3 K2CO3 NaNO3 CaCl2
B . KCl NaHCO3 K2SO4 NaCl
C . NaCl ZnSO4 KNO3 KOH
D . HCl MgCl2 Na2SO4 NaCl
俗话说“不是一家人,不进一家门”,我是NaOH溶液,我的家人和谐共处,相互间不发生反应.以下溶液中能进我家门的一组是( )
A . KNO3、Na2SO4、HCl、KCl
B . KNO3、NaCl、NH4Cl、Na2SO4
C . KOH,BaCl2、KCl、NaNO3
D . K2CO3、K2SO4、CaCl2、NaNO3
下列溶液无色,在pH=1时能大量共存的是( )
A . CuSO4 NaCl KNO3
B . NaOH NaCl NaNO3
C . Na2SO4 NH4Cl ZnCl2
D . K2SO4 AgNO3 NaCl
下列可以共存且能形成无色溶液的是( )
A . HCl、NaOH、  B .
B .  、
、  、
、  C .
C .  、
、  、NaCl
D . NaOH、
、NaCl
D . NaOH、  、NaCl
、NaCl
 B .
B .  、
、  、
、  C .
C .  、
、  、NaCl
D . NaOH、
、NaCl
D . NaOH、  、NaCl
、NaCl
常温下,下列各组离子能在pH=13的无色透明溶液中大量共存的是( )
A . K+、Cu2+、Cl﹣、SO42﹣
B . Mg2+、Na+、Cl﹣、CO32﹣
C . Na+、Ba2+、Cl﹣、NO3﹣
D . H+、NH4+、NO3﹣、Cl﹣
下列各组离子在pH=1的水溶液中能大量共存的是( )
A . K+、Na+、Cl-、HCO3-
B . H+、K+、Cl-、OH-
C . Cu2+、Ba2+、Cl-、SO42-
D . K+、NH4+、Cl-、NO3-
据东北网报道:哈尔滨北方农业科技园无土栽培温室大棚(如图)喜获丰收,试回答:

-
(1) 建造大棚所用的外部塑料名称一般是薄膜,而内部没有铁做支架,因为铁易;
-
(2) 大棚内的绿色大叶蔬菜主要为人体提供的营养素是;
-
(3) 为防止植物倒伏,且叶色浓绿,应施加的一种化肥是(填化学式)
-
(4) 无土栽培,在配制右表中一份营养液时,表中备注不要用硬水配置营养液,推测原因是。
在“宏观﹣微观﹣符号”之间建立联系,是化学学科特有的思维方式,能帮助我们更好地认识物质变化的本质。请完成下列问题:
-
(1) 晋代葛洪所著《抱朴子》一书中记载有“丹砂烧之成水银”,丹砂指的是HgS.该反应的微观示意图可以表示为(如图1所示):
图1
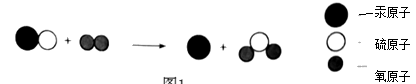
图2

请写出该反应的化学方程式,微粒“
 ”表示的物质属于(填“单质”或“化合物”)。
”表示的物质属于(填“单质”或“化合物”)。 -
(2) 由初中学习可知:中和反应的微观实质是氢离子和氢氧根离子结合生成了水分子,即:H++OH﹣=H2O.像这种用实际参加反应的离子符号来表示化学反应的式子叫离子方程式。离子方程式的书写一般按以下步骤(以氯化镁溶液与氢氧化钾溶液反应为例):
I.写出氯化镁溶液与氢氧化钾溶液反应的化学方程式:;
Ⅱ.把易溶于水、易电离的物质写成离子形式,难溶的物质、气体和水等仍用化学式表示。上述方程式可改写成:Mg2++2Cl﹣+2K++2OH﹣=Mg(OH)2↓+2Cl﹣+2K+;
Ⅲ.删去两边不参加反应的离子,即得离子方程式:Mg2++2OH﹣=Mg(OH)2↓。
请回答:
①如图2是碳酸钠溶液和稀盐酸反应的微观示意图,请写出该反应的离子方程式:;
②写出一个与Fe+Cu2+=Fe2++Cu相对应的化学方程式。
③下列各组离子,在pH=3的无色水溶液中能大量共存的是(填序号)。
A.K+、Fe2+、Cl﹣、SO42﹣
B.Na+、Ca2+、NO3﹣、OH﹣
C.Na+、Ca2+、Cl﹣、CO32﹣
D.NH4+、Ba2+、Cl﹣、NO3﹣
下列各组物质分别加入到足量的水中,能共存且得到无色透明溶液的是( )
A . KNO3、NaCl、HCl
B . FeCl3、Na2SO4、KCl
C . Na2CO3、H2SO4、NaCl
D . MgCl2、KCl、NaOH
许多物质在溶液中都以离子形式存在。我们熟悉的复分解反应就是溶液中离子间结合得到水、气体或沉淀 的一类化学反应。如:氢氧化钠与盐酸的反应就是溶液中的H+和OH-结合成水分子的过程(如图所示)。结合信息、图示,你认为下列各组离子间不能反应的是( )

A . H+、Na+、OH-、 NO3-
B . Na+、 K+、 Cl-、OH-
C . H+、K+ 、CO32-、HCO3-
D . K+、Ba2+、Cl-、SO42-
下列各组物质在水中能大量共存,且形成无色透明溶液的是( )
A . CuSO4、KCl、HCl
B . K2SO4、NaOH、NH4Cl
C . HNO3、NaCl、Ca(OH)2
D . KNO3、Na2SO4、NaCl
下列各组离子在溶液中能大量共存的是( )
A . K+、  、
、 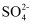 、OH-
B . H+、Ba2+、Cl-、OH-
C . Fe3+、Na+、
、OH-
B . H+、Ba2+、Cl-、OH-
C . Fe3+、Na+、  、
、  D . Ag+、Na+、Cl-、
D . Ag+、Na+、Cl-、 
 、
、 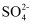 、OH-
B . H+、Ba2+、Cl-、OH-
C . Fe3+、Na+、
、OH-
B . H+、Ba2+、Cl-、OH-
C . Fe3+、Na+、  、
、  D . Ag+、Na+、Cl-、
D . Ag+、Na+、Cl-、 
能在水中大量共存的一组离子是( )
A . NH4+、Na+、Cl-、  B . K+、Ag+、
B . K+、Ag+、  、Cl-
C . K+、Ba2+、OH-、
、Cl-
C . K+、Ba2+、OH-、  D . H+、Na+、
D . H+、Na+、  、
、 
 B . K+、Ag+、
B . K+、Ag+、  、Cl-
C . K+、Ba2+、OH-、
、Cl-
C . K+、Ba2+、OH-、  D . H+、Na+、
D . H+、Na+、  、
、 
甲化工厂排放的酸性污水和乙化工厂排放的污水,共含有以下6种离子中的各3种:K+、OH﹣、 、Ba2+、H+、
、Ba2+、H+、 , 则乙化工厂排放的污水中所含有的3种离子是。
, 则乙化工厂排放的污水中所含有的3种离子是。
 、Ba2+、H+、
、Ba2+、H+、 , 则乙化工厂排放的污水中所含有的3种离子是。
, 则乙化工厂排放的污水中所含有的3种离子是。
下列各组物质能在pH为2的无色溶液中大量共存的是( )
A . FeCl3、CuSO4、NaCl
B . K2SO4、NaNO3、KCl
C . CaCl2、Na2CO3、NaNO3
D . NaOH、AgNO3、NaCl
某无色溶液中只有三种离子,这三种离子可能是( )
A . H+、Ca2+、Na+
B . Na+、OH-、 C . Fe2+、Cl-、
C . Fe2+、Cl-、 D . H+、
D . H+、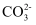 、OH-
、OH-
 C . Fe2+、Cl-、
C . Fe2+、Cl-、 D . H+、
D . H+、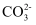 、OH-
、OH-
能在pH=1的溶液中大量共存,且溶液无色透明的一组离子是( )
A . Ba2+、Ag+、 、Cl-
B . K+、Na+、
、Cl-
B . K+、Na+、 、OH-
C . Zn2+、Na+、
、OH-
C . Zn2+、Na+、 、Cl-
D . Fe2+、Ca2+、NO3-、Cl-
、Cl-
D . Fe2+、Ca2+、NO3-、Cl-
 、Cl-
B . K+、Na+、
、Cl-
B . K+、Na+、 、OH-
C . Zn2+、Na+、
、OH-
C . Zn2+、Na+、 、Cl-
D . Fe2+、Ca2+、NO3-、Cl-
、Cl-
D . Fe2+、Ca2+、NO3-、Cl-
最近更新



