水的净化 知识点题库
(1)①现对水样进行如下处理:向水样中加入明矾溶解,搅拌,静置一段时间后,进行 (填操作名称),下列仪器在该操作中要用到的有 (填字母).
A.带铁圈的铁架台 B.酒精灯 C.漏斗 D.玻璃棒 E.量筒 F.烧杯
②再向滤液中加入活性炭,利用其 性除去水样中的颜色和异味.
③做好生活饮用水消毒工作,是预防肠道传染病的关键.适用于饮用水消毒的常用消毒剂是漂白粉.漂白粉的主要成分是氯化钙[CaCl2]和次氯酸钙[Ca(ClO)2],关于漂白粉的说法中,合理的是: .
A.氯化钙[CaCl2]和次氯酸钙[Ca(ClO)2]中氯元素的化合价相同
B.氯化钙[CaCl2]和次氯酸钙[Ca(ClO)2]中钙元素的质量分数相同
C.氯化钙[CaCl2]和次氯酸钙[Ca(ClO)2]都由离子构成
D.次氯酸钙[Ca(ClO)2]中含有的原子团是ClO﹣
(2)硬水给生产、生活带来许多不便.检验水样是硬水还是软水的方法是: .生活中降低水的硬度最常用的方法是: .
-
(1) 洪涝灾害期间,水源容易受到细菌、病毒、寄生虫卵、幼虫的污染.饮用水的消毒方法很多,简便实用的是;
-
(2) 灾民用下列几个步骤将河水转化为可饮用水:①化学沉降(用明矾),②消毒杀菌(用漂白粉),③自然沉降,④加热煮沸.以上处理过程顺序合理的是;A.③②①④B.③①②④C.③①④②D.①③④②
Ⅰ、向水样中加入明矾搅拌溶解,静置一段时间后,进行 (填操作名称),除去固体小颗粒,该实验用到的仪器和用品有(填序号).
①带铁圈的铁架台;②试管;③漏斗;④玻璃棒;⑤集气瓶;⑥烧杯;⑦滤纸
Ⅱ、再向滤液中加入活性炭,利用其性除去水样中的颜色和异味,该过程属于 变化(填“物理”或“化学”).
-
(3) 用肥皂在实验室的自来水中洗衣时,起浮渣,说明该自来水是含的水,属于硬水.
-
(1) 保持水的化学性质的最小微粒是(用化学用语答);
-
(2) 自来水生产过程中,除去水中不溶性杂质可采用的方法是,活性炭的作用是;
-
(3) 常见的几种净水方法中,净化程度最高的操作是.
-
(4) “水”在化学实验中的作用不可小视.

请回答:实验A中水的作用是;实验B中水的作用是,写出该反应的化学方程式;实验C中的水除提供热量外,还起到了作用.
-
(5) 下列关于生理盐水的说法中,不正确的是 (填字母).A . 生理盐水的溶剂是水 B . 各部分一样咸体现了溶液具有均一性的特征 C . 饮用生理盐水可以为人体补充无机盐 D . 氯化钠分子是保持氯化钠化学性质的最小微粒
-
(6) 在细菌作用下,可以用氨气处理含有甲醇(CH3OH)的工业废水,有关反应的化学方程式为
5CH3OH+12O2+6NH3
 3X+5CO2+19H2O,则X的化学式为.
3X+5CO2+19H2O,则X的化学式为.
-
(1) 某矿泉水的主要矿物质成分机及含量如表,这里Ca、K、Zn、F是指.(填“单质、元素、分子或原子”)
成分
Ca
K
Zn
F
含量(mg/L)
20
3
0.06
0.02
-
(2) 水污染日益严重,水资源的保护和合理利用已受到人们的普遍关注,请参与讨论下列有关问题:
(Ⅰ)自来水、冰水混合物、海水中属于纯净物的是.
(Ⅱ)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如图所示:

①对应的作用是(填字母序号,下同).
A.杀菌消毒 B.吸附杂质 C.沉淀过滤 D.蒸馏
(Ⅲ)下列做法会造成水体污染的有.
A、工业废水直接排放 B、工业废气处理后排放
C、禁止使用含磷洗衣粉 D、大量使用化肥、农药
(Ⅳ)能确认水是由氧元素和氢元素组成的实验是.
A、氢气在氧气中燃烧生成水 B、水的蒸发 C、水的电解 D、水的净化
-
(3) 长期饮用硬水可能会引起体内结石,鉴别硬水和软水最简单的方法是用鉴别.
-
(4) 水通电分解生成最理想的能源﹣﹣氢气,电解一定量的水,当其中负极产生5ml气体时,正极产生的气体体积是ml.
-
(1) 检验某地下水是硬水还中软水,可用的物质是。
-
(2) 为了降低水的硬度,要建议农民在饮用前要。
-
(3) 自来水生产过程中可用方法除去水中不溶性杂质。
-
(4) 自来水厂用活性炭的性去除水中的色素,该性质是性质(填“化学”或“物理”)。
-
(5) 目前湘江河水污染严重,河水污染的原因之一是 ,从保护水资源的角度向全市人民发出倡议:。
-
(1) 沉淀、过滤和吸附是工业中常用的净水方法。水中含有不溶性杂质,加入明矾沉降后,通过将其除去;常用吸附水中的色素和异味。
-
(2) 使用硬水会给生活和生产带来许多麻烦,可用 检验硬水和软水;生活中可以通过 降低水的硬度。
-
(3) 电解水实验证明水是由 组成的。

-
(1) 仪器名称:①;②。
-
(2) 用氯酸钾和二氧化锰制氧气,可选用装置(选填序号)和 E 组合,化学方程式为。
-
(3) 实验室制氧气时将0.8g二氧化锰与一定量氯酸钾共热到质量不减少为止,称得残渣质量为15.7g。求:原氯酸钾的质量是g
-
(4) 实验室可用装置B或C制 H2 , C 装置相对于B的优点有,用D装置收集 H2 , 气体应从(选填“a”或“b”)端通入。
-
(5) F为简易净水装置,相当于化学实验中的装置。向该装置处理过的水中,加入少量肥皂水振荡,产生较多浮渣,说明是(填“硬”或“软”)水,若要得到纯水,还需 要进行(填操作名称)。
-
(1) 从宏观角度:水是由 组成的。
-
(2) 从微观角度:下列图示可以表示构成水的微粒是 (填序号);

-
(3) 从生活角度:
a:某同学取自来水于试管中,加入适量,振荡,发现有较多浮渣产生,说明该自来水属于硬水。随着净水技术的发展,一种净水机可以将水厂原水直接净化为饮用水,其 中处理流程如图所示:

b:步骤①对应的作用是 ,步骤③对应的作用是 ,超滤膜可起到过滤不溶性杂质的作 用,实验室进行过滤操作所需要的仪器有带铁圈的铁架台、烧杯、漏斗(含滤纸)和
-
(4) 从变化角度:
水通电可发生分解反应,电解一定量的水,负极产生的气体是 (写化学式),当负 极产生的气体为 10mL 时,正极产生的气体体积为 mL;检验正极产生的气体用的木条放在尖嘴处,观察现象,可证明气体成分。
-
(1) 天然水多为硬水,生活中可通过使其转化为软水。
-
(2) 家用净水剂中常使用净水,可以吸附水中的异味和色素。
-
(3) 如图为实验室电解水的装置,通电一段时间后,a管和b管中产生气体的体积比是,反应的化学方程式为,该反应的基本类型是。

-
(4) 爱护水资源,一方面要节约用水,另一方面要防治水体污染。水体污染的来源主要有工业污染、农业污染和。
-
(1) 化石燃料是一种不可再生资源,包括天然气、石油、。天然气主要成分燃烧时反应的化学方程式为。
-
(2) “生命吸管”可直接将污水净化为饮用水,主要处理步骤与自来水的净化过程相似,如图所示:(③中离子交换树脂的主要作用是去除重金属离子、软化水质)
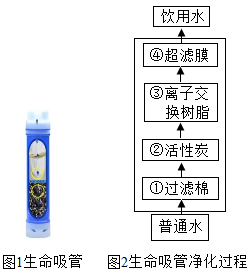
②中活性炭的作用是(填字母。下同),④中超滤膜的作用是。
A 去除有害菌和部分病毒 B 吸附杂质 C 除去较大的不溶性杂质
-
(3) 若无生命吸管,取用河水时,要降低水的硬度和杀灭病原微生物,生活中常采取方法。通过生命吸管净化后的水属于(填“纯净物”“混合物”)。


-
(1) 图1为自然界水循环示意图。下列关于水的天然循环的说法中正确的是____(填选项序号)。
①太阳为水的天然循环提供了能量
②水的天然循环是通过水的三态变化实现的
③水在天然循环过程中实现了水的自身净化
④水的天然循环完成了水资源的重新分配
A . 只有①② B . 只有①③ C . 只有②③④ D . ①②③④ -
(2) 图2是电解水的示意图,实验中玻璃管a、b中产生气体的体积比约为,能使带火星木条复燃的气体是玻璃管(填a或b)中的气体此玻璃管连接电源的极,能燃烧的气体是玻璃管(填a或b)中的气体,燃烧时产生火焰,电解水的文字表达式为,反应涉及到的能量转化是电能转化为能。
-
(3) 天然水净化的方法有:①沉降②过滤③消毒杀菌④蒸馏等,其中净化程度最高的是(选填序号)。杀菌消毒时加入的液氯与水反应生成盐酸和次氯酸,这个变化属于(“化学变化”或“物理变化”)。
-
(4) 实验室对一杯浑浊的天然水进行过滤操作(如图),请指出图中的一处不正确。用滴管取两滴过滤后的滤液,滴在洁净的玻璃片,置于酒精灯上慢慢加热,至水分消失。观察到玻璃片上有少许残留物,该现象说明过滤后的水中含有。

-
(5) 生活中我们可以用区分硬水和软水,可以用的方法降低水的硬度。
-
(6) 水的用途很广,铁丝在氧气中燃烧时,在集气瓶底放少量的水,目的是。

-
(1) 自来水厂常用采用静置沉淀、、活性炭吸附、消毒等净水操作,已达到净化水质的目的。
-
(2) 净化后的自来水是硬水还是软水,可用来进行鉴别。
-
(3) 硬水不利于人体的健康,所以日常生活中常采用操作降低水的硬度。
-
(1) 下列有关水的说法正确的是______。A . 地下水是纯净物,可以直接饮用 B . 淡水资源是取之不尽的 C . 利用活性炭可以软化硬水 D . 使用无磷洗涤剂可以减少水体污染
-
(2) 冬天用氯化钠做融雪剂,渗入地下增加地下水的含盐量,会造成地下水污染。氯化钠在不同温度时的溶解度如下表所示:
温度/℃
20
40
60
80
100
溶解度/g
36.0
36.6
37.3
38.4
39.8
①80℃时,将38 g氯化钠放入到100 g水中,搅拌至固体全部消失,此时为溶液(填“饱和”或“不饱和");冷却到室温(20℃),有g晶体析出。
②如图是NaCl和KNO3的溶解度曲线图。

30℃时,NaCl的溶解度KNO3的溶解度(填写“>”“=”或“<”)。
-
(3) 天然水转化为自来水,消毒常用液氯消毒剂,发生的反应为:Cl2+H2O=HCl+HClO。小明用自来水直接配制硝酸银溶液发现产生了白色沉淀,请写出化学方程式。
-
(4) 生活中含氮有机物分解等会造成废水中氨氮(以NH3形式存在)含量过高,直接排放会导致水体富营养化。次氯酸(HClO)可以除去废水中的NH3 , 若废水碱性过强(pH>10),NH3的去除率会显著降低,原因是。

-
(1) ①中过滤棉的作用是(填字母,下同),④中超滤膜的作用是。
A.去除有害菌和部分病毒 B.除去颗粒较大的不溶性杂质 C.吸附杂质
-
(2) 若无“生命吸管”,要杀灭天然水中的病原微生物,生活中常采取方法,通过生命吸管净化后的水属于(填“纯净物或“混合物”)。
-
(3)

☆如上中图为A、B两种固体物质的溶解度曲线。
在t1℃时,A、B两种物质的溶解度。 -
(4) t1℃时,要使接近饱和的B物质溶液变为饱和溶液,可采取的一种措施是。
-
(5) t2℃时,A物质饱和溶液中溶质的质量分数为。若要把100克该饱和溶液稀释成质量分数为5%的溶液,应加水克。



