溶液的酸碱性与pH值的关系 知识点题库
下列表示错误的是( )
A . 银铜铁的金属活动性强弱 B . 物质形成溶液的pH
B . 物质形成溶液的pH C . 据含碳量分为生铁和钢
C . 据含碳量分为生铁和钢 D . 硫及其化合物与化合价的关系
D . 硫及其化合物与化合价的关系
 B . 物质形成溶液的pH
B . 物质形成溶液的pH C . 据含碳量分为生铁和钢
C . 据含碳量分为生铁和钢 D . 硫及其化合物与化合价的关系
D . 硫及其化合物与化合价的关系
质量为50g溶质质量分数为20%的氢氧化钾溶液和质量为50g溶质质量分数为20%的稀硫酸混合,所得溶液的pH( )
A . 小于7
B . 等于7
C . 大于7
D . 不确定
pH如下表所示,其中显酸性的是( )
番茄汁 | 糖水 | 牙膏 | 肥皂水 | |
pH | 4 | 7 | 9 | 10 |
A . 番茄汁
B . 糖水
C . 牙膏
D . 肥皂水
下列四个图象能正确反映其对应实验操作的是( )
A .  高温煅烧一定质量的石灰石
B .
高温煅烧一定质量的石灰石
B .  用等质量、等浓度的双氧水分别制取氧气
C .
用等质量、等浓度的双氧水分别制取氧气
C .  向一定体积的稀盐酸中逐滴加入氢氧化钠溶液
D .
向一定体积的稀盐酸中逐滴加入氢氧化钠溶液
D .  某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
 高温煅烧一定质量的石灰石
B .
高温煅烧一定质量的石灰石
B .  用等质量、等浓度的双氧水分别制取氧气
C .
用等质量、等浓度的双氧水分别制取氧气
C .  向一定体积的稀盐酸中逐滴加入氢氧化钠溶液
D .
向一定体积的稀盐酸中逐滴加入氢氧化钠溶液
D .  某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
如图所示是化学试剂瓶上的标签,取10mL该硫酸可配制成9.8%的稀硫酸质量为 g,配制9.8%的稀硫酸的操作是;完全中和稀硫酸需要氢氧化钠的质量为mg,若用mg氢氧化钾与上述稀硫酸充分反应,所得溶液的pH7(填“大于”、“小于”或“等于”).

节假日或双休日,去郊游野炊实为一大快事.然而,在野炊的情趣之中,如果遇到下面一些问题,你是如何处理的?
-
(1) 对野炊有经验的人会告诉你,餐具最好是导热性好、不易破碎的材料制的,你准备带的餐具是用 (填字母)制的.A . 金属 B . 陶瓷 C . 无所谓
-
(2) 在“灶”上悬挂野炊锅时,应调节野炊锅到合适的高度.你觉得原因可能是.
-
(3) 在引燃细枯枝后,如果迅速往“灶”里塞满枯枝,结果反而燃烧不旺,并产生很多浓烟,说明物质充分燃烧需要的条件是.
-
(4) 若不小心被蚊虫叮咬(蚊虫能分泌出蚁酸),下列物质可用于涂抹以减轻疼痛的是 . (填字母)A . 食醋(pH<7) B . 食盐水(pH=7) C . 肥皂水(pH>7)
-
(5) 郊外通常比较泥泞,如果你的交通工具是自行车,铁质部件容易生锈.铁锈蚀的条件是铁与氧气和共同接触.铁锈的主要成分是(填化学式).你回来进行清洗后是如何防锈的:(填字母).
A.立即晾晒干 B.链条传动部件涂上油 C.涂油漆.
目前,人们使用的燃料大多来自于化石燃料,它们是(填“可”或“不可”)再生资源.二氧化硫直接排放到空气中会造成空气污染,若遇降雨会形成,取这种刚降到地面的雨水水样,在一段时间内每隔几分钟测一次pH值,其pH值会逐渐减小,这说明在测定期间酸性会.
据2017年5月21日长沙晚报报道:中央第六环保督察组向长沙市转办的群众信访举报件中.其中有一封有关某洗涤厂违规排放废水污染河流的举报信,当地环保部门高度重视,立即派工作人员实地检测,测得污水的pH>7,请你分析并回答:
-
(1) 工厂排出的废水显性(填“酸”、“碱”、“中”);
-
(2) 为了长沙的青山绿水,请你提一条合理的建议.
向一定质量的Ba(OH)2溶液中先后滴加CuSO4、H2SO4溶液,过程中加入溶液的质量与产生沉淀的质量关系如图所示.下列说法正确的是( )

A . a点对应溶液pH>7
B . b点对应溶液中溶质有2种
C . m=3.31
D . 取c点对应溶液,滴加NaOH溶液,立刻产生沉淀
氯化钙应用广泛,以石灰石(杂质主要是Fe2O3、MgSO4)为原料生产氯化钙的流程如下。

已知:BaCl2 + MgSO4 = BaSO4↓+ MgCl2
Ca(OH)2 + MgCl2 = Mg(OH)2↓+ CaCl2
Ca(OH)2 + FeCl3 = Fe(OH)3↓+ CaCl2
-
(1) 氧化铁与盐酸反应的化学方程式为。
-
(2) 滤液1中的溶质有HCl、FeCl3、MgSO4和。
-
(3) 滤液2中加入Ca(OH)2是为了除去 (填序号,下同)。A . MgCl2 B . FeCl3 C . HCl
-
(4) 滤液3呈碱性,为使溶液pH降低,可加入适量的 。A . NaCl B . NaOH C . 盐酸
某工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸(该产品中其它物质不与NaOH反应),消耗氢氧化钠溶液的质量与反应过程中溶液的pH值关系如图所示。

-
(1) 图中A点表示的意义是。
-
(2) A点消耗氢氧化钠溶液的溶质的质量为g。
-
(3) 求石油产品中残余硫酸的质量g(写出计算过程)。
pH是水质监测的重要指标之一,下列水样酸性最强的是( )
A . pH=1.3的工业废水
B . pH=4.5的雨水
C . pH=7.0的蒸馏水
D . pH=7.3的矿泉水
下列人体体液中,酸性最强的是( )
A . 唾液(pH约6.6~7.1)
B . 胃液(pH约0.8~1.5)
C . 胆汁(pH约6.8~7.4)
D . 血液(pH约7.35~7.45)
如图是常温下一些常见物质的pH,其中酸性最强的是( )
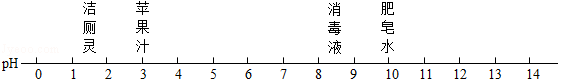
A . 洁厕灵
B . 苹果汁
C . 消毒液
D . 肥皂水
已知某NH4NO3溶液的pH=4.下列说法错误的是( )
A . 盐溶液不一定都显中性
B . NH4NO3是一种复合肥料
C . NH4NO3不能与熟石灰混合使用
D . 久施NH4NO3的土壤可能被酸化
Na2CO3溶液具有碱性,可清洗油污,碱性越强,去油污的效果越好,小菁决定对影响Na2CO3溶液碱性的因素展开探究。
[进行实验]
实验一: 用不同温度的水,配制溶质质量分数分别为2%、6%和10%的Na2CO3溶液,依次测量溶液pH,记录数据如下表:
|
实验编号 |
a1 |
a2 |
a3 |
b1 |
b2 |
b3 |
c1 |
c2 |
c3 |
|
溶质质量分数 |
2% |
2% |
2% |
6% |
6% |
6% |
10% |
10% |
10% |
|
水的温度(℃) |
20 |
40 |
60 |
20 |
50 |
60 |
20 |
40 |
70 |
|
溶液pH |
10.90 |
11.18 |
11.26 |
11.08 |
11.27 |
11.30 |
11.22 |
11.46 |
11.50 |
实验二: 将10%的Na2CO3溶液从20℃持续升温到70℃,所测得的pH如下表:
|
温度(℃) |
20 |
30 |
40 |
50 |
60 |
70 |
|
溶液pH |
11.22 |
11.35 |
11.46 |
11.48 |
11.50 |
11.50 |
[解释与结论]
-
(1) 碳酸钠俗称是。
-
(2) 要证明Na2CO3溶液的溶质质量分数变化与pH变化关系,可选择最佳的一组实验是(填实验编号),其结论是。
-
(3) 实验二的目的是。
-
(4) [反思与评价]
小菁将Na2CO3粉末洒在有油污的餐具上,再加适量热水,进行擦洗,达到较好的洗涤效果,这是因为。
-
(5) 解释Na2CO3溶液显碱性的反应如下,请补全该反应的化学方程式:Na2CO3+H2O=NaHCO3+
“关爱生命,注意安全,拥抱健康”是永恒的主题。下列有关叙述错误的是( )
A . 煤矿的矿井里不但要严禁烟火而且要经常通风
B . 健康人体内血浆的pH范围是7.35~7.45
C . 吸烟有害健康,青少年一定不要吸烟
D . 人体中的硒元素、铁元素、氯元素等微量元素摄入量过低会影响身体健康
科学就是发现问题和解决问题,化学兴趣小组发现向碳酸钠溶液中滴加相同浓度的盐酸溶液并不是立即有气体生成,据此小组首先查阅资料:原来向碳酸钠溶液中加入盐酸时反应分两步完成。第一步,Na2CO3+HCl=NaHCO3+NaCl;第二步,NaHCO3+HCl=NaCl+CO2↑+H2O。然后在老师指导下使用数字化传感器测定反应过程中pH及CO2浓度的变化值如图所示,请同学们根据所学化学知识和资料及实验数据判断下列有关实验分析正确的是( )

A . A~B段,溶液中溶质为碳酸氢钠
B . A~B,溶液中的pH值逐渐变小,碱性变大
C . 上图曲线,②表示盐酸滴加到碳酸钠溶液中生成二氧化碳气体体积数
D . 滴加0﹣40mL盐酸溶液时CO2浓度几乎不变,说明此时盐酸与碳酸钠未发生反应。
取NaOH和NaCl的混合物3.63克放入烧杯中,加水溶解配制成70克溶液。向该溶液滴加溶质质量分数为7.3%的稀盐酸,测得溶液pH与滴入稀盐酸的质量关系如图所示。

-
(1) 当滴入稀盐酸的质量为11.2克时,溶液的pH7(填“>”、“<”或“=”);此时溶液中的溶质是(填化学式)。
-
(2) 当pH=7时,计算该溶液中溶质的质量分数。(写出计算过程)
化学与农业密切相关,请回答下列问题:
-
(1) 海水稻在我国首种成功。海水呈弱碱性,其pH7(填“>”、“=”或“<”)。
-
(2) 农作物生长必需的营养元素中,元素需求量较大。
-
(3) 海稻米也称为海红米,营养丰富,大米中的淀粉在人体内经过一系列变化转变成和水。
-
(4) 把稻草放在密闭的沼气池中发酵,可产生沼气,沼气的主要成分为,用沼气作燃料,与用煤相比能减少的空气污染物有。
最近更新



