有关元素化合价的计算 知识点题库
吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体内的活性氧。亚硒酸钠中硒元素的化合价是( )
A . +2
B . +3
C . +4
D . +6
普通玻璃的成分之一是硅酸钠(化学式为Na2SiO3),硅酸中钠的化合价是( )
A . +1
B . +2
C . +4
D . +6
“LED”节能光源材料是砷化镓(GaAs),其中Ga的化合价为+3价,则As的化合价为( )
A . +3
B . +1
C . ﹣3
D . -1
钾长石是一种金属矿物,其主要成分的化学式为KAlSi3O8 , 其中硅元素的化合价为( )
A . ﹣4
B . +2
C . +4
D . +6
下列有关硝酸钾(KNO3)的说法中,错误的是( )
A . 由三种元素组成
B . 氮元素的化合价为+3价
C . 可用作复合肥料
D . 氮、氧两种元素的质量比为7:24
生活中有化学,化学在我们身边.下列叙述正确的是( )
A . 灯泡发光、木材燃烧是化学变化
B . 用苏打粉可以除去发酵后面团中的酸味
C . 面包、饼干的主要物质为我们提供了丰富的蛋白质
D . 含磷洗衣粉的主要成分为Na3PO4 , Na3PO4中P的化合价为﹣5价
备受市民关注的梅州市第一条高铁项目﹣﹣梅汕高铁先行段2015年4月27日在丰顺县开工建设.这意味着在不久的将来,我市将迈入“高铁时代”,融入全国高铁大家庭.
-
(1) 高铁列车的车体建设需要消耗大量的铝合金.铝具有很强的抗腐蚀性,其原因是(用化学方程式表示).
-
(2) 高铁列车上提供的矿泉水中富含钾、钙、钠等,这里的钾、钙、钠指的是(填“原子”、“分子”、“元素”或“单质”).
-
(3) 高铁的建成,缩短出行时间,有利于减少化石燃料的使用,含硫化石燃料燃烧时排放出,其在空气中发生反应后生成物溶于雨水,会形成酸雨.
-
(4) 高铁酸钠(Na2FeO4)是高铁上常用的一种“绿色环保”的消毒剂,高铁酸钠中铁元素的化合价为.
现代生活节奏加快,汽车也日趋增多,其尾气造成的空气污染也日趋严重,图1为汽车尾气净化过程发生反应的微观示意图,请回答下列问题:
图1 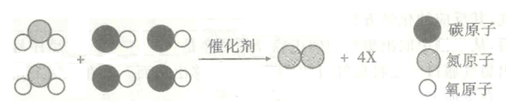
-
(1) 图2中X所表示物质的分子示意图为A .
 B .
B .  C .
C .  D .
D . 
-
(2) 请写出表示图1中反应的化学方程式,
某同学根据生成物是一种单质和一种化合物判定该反应为置换反应,你认为(填“正确”或“不正确”);
-
(3) 尾气中的二氧化氮可以转化为氨气(NH3)制氮肥,NH。中氮元素的化合价为;又知镁原子的结构示意图为
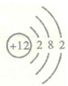 ,则镁元素与氮元素(化合价与氨气中相同)形成化合物的化学式为
,则镁元素与氮元素(化合价与氨气中相同)形成化合物的化学式为
-
(4) 将尾气中的一氧化碳收集起来作为燃料,为防止泄漏事先在收集装置中加入一种有恶臭味的乙硫醇,这样做的目的是。
钛酸钡粉体是电子陶瓷元器件的重要基础原料。工业以草酸盐共沉淀法获得草酸氧钛钡晶体[BaTiO(C2O4)2.4H2O],煅烧可获得钛酸钡粉体。

-
(1) BaTiO3中Ti元素的化合价是
-
(2) “酸浸”过程中发生反应的化学方程式为.
-
(3) “操作A”的名称是
-
(4) “绿色化学”理念提倡循环利用,流程中能循环使用的物质是.
-
(5) 现有394kg BaCO3,理论上可以制备BaTiO3的质量为kg.(BaTiO3的相对分子质量为233,BaCO3的相对分子质量为197)
分类、类比、迁移是学习化学的方法,“宏观辨识与微观探析”是化学学科核心素养之一”,学科思想方法与核心素养的形成与发展帮助我们更好地分析与解决问题。
-
(1) 化学发展史上许多实验之间存在一定的关联:有些实验是“一种物质的认识是研究其他物质的基础”,有些实验是“药品与研究方法相同而研究目的不同”。据此可将下列实验中的①(填字母)归为一类,依据是②
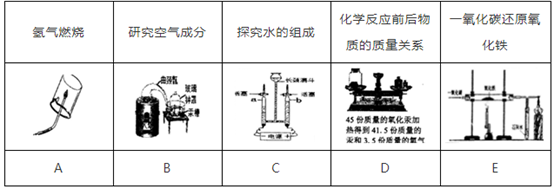
-
(2) 利用实验E中一氧化碳的性质、仿照E中的实验原理,写出“使用催化净化装置将燃油汽车尾气中的一氧化碳和二氧化氮转化为两种无害气体”的反应的化学方程式①,反应前、后碳元素化合价的变化为②,其原因是有③(填“电子”或“质子”)偏离(或转移)
新版人民币的防伪油墨中含MgF2 , MgF2中F元素的化合价是()
A . +1
B . -1
C . +2
D . -2
下列各组物质中,划线元素的化合价相同的一组是( )
A . KMnO4、K2MnO4
B . P2O5、Ca3(PO4)2
C . NH4Cl、HNO3
D . Cl2、CaCl2
钨(W)及其化合物具有优良的机械加工性能,在航空航天、军事装备、电子等领域应用广泛。工业上用黑钨矿(主要成分为钨酸亚铁,化学式FeWO4)制得金属钨的工艺流程如图所示:

回答问题:
-
(1) 金属钨可用作电灯的灯丝,是因为钨具有的性质。
-
(2) H2WO4的名称为,其中钨元素的化合价为。
-
(3) 反应①为4FeWO4+4Na2CO3+O2
 4Na2WO4+2Fe2O3+4X,X的化式为。反应③属于反应(填基本反应类型)。
4Na2WO4+2Fe2O3+4X,X的化式为。反应③属于反应(填基本反应类型)。
-
(4) 反应④的化学方程式为。
-
(5) 将含76%钨酸亚铁的钨黑矿m吨,通过上述流程,理论上能制得金属钨的质量吨(填含有m的式子)。
“垃圾是放错的资源”。碘循环工艺不仅能吸收SO2 , 减少环境污染,而且还可以得到重要化工产品H2SO4 , 和H2 , 流程如下:

-
(1) SO2是大气污染的主要污染物之一,它主要来源于含硫化石燃料的燃烧。化石燃料包括、和天然气。
-
(2) 副产品H2SO4 , 中S的化合价为。
-
(3) 反应器中发生反应的化学方程式是。
-
(4) 膜反应器中发生的化学方程式是,该反应属于反应(填基本反应类型)。
-
(5) 流程中可循环利用的物质是。
化学与我们的生活息息相关,请用所学的化学知识回答有关问题:
-
(1) 生活中使用铜丝来做导线,利用了金属良好的。
-
(2) 体温计中填充的银白色物质是(填化学符号)。
-
(3) 84消毒液主要成分为次氯酸钠(NaClO),写出次氯酸钠中阴离子的离子符号。
-
(4) 抗击“新型冠状病毒肺炎”疫情的战斗中,我们需要用75%的医用酒精进行室内消毒,酒精的化学式是。
-
(5) 加碘盐是在食盐中加入碘酸钾(KIO3),KIO3中碘元素的化合价为。
误食工业用盐亚硝钠(NaNO2)会引起中毒。亚硝钠中氮元素的化合价为( )
A . -2
B . +1
C . +3
D . +5
炎热的夏日即将到来,如图是一款变色眼镜,它的镜片内含有溴化银和氧化铜。在强光照射下,溴化银分解成单质溴和银,镜片颜色变深;当光线变暗时,溴和银在氧化铜催化作用下,又立即化合成溴化银,镜片颜色变浅。有关该眼镜的说法不正确的是( )

A . 塑料是有机合成材料
B . 钛合金属于化合物
C . 溴化银分解后,银元素的化合价降低
D . 溴和银化合成溴化银前后,氧化铜化学性质不变
2022年冬季奥运会在北京市和张家口市联合举行,这是中国历史上第一次举办冬季奥运会。
-
(1) 为了解决两地交通问题,增开多列高铁,制造高铁车身会用到镁铝合金,镁铝合金属于(填“金属”或“复合”)材料。
-
(2) 二氧化氯(ClO2)是冬奥场馆用水的一种消毒剂,ClO2中氯元素的化合价为。
-
(3) 冬奥会在场馆建设中用到一种耐磨、耐高温的表面涂料,该涂料以双环烯酯(C14H20O2)为原料制得,双环烯酯属于(填“无机化合物”或“有机化合物”),其中碳、氢元素的质量比为。
-
(4) 冬奥火炬“飞扬”采用氢气作为燃料。氢气燃烧的化学方程式为。
资料显示:新冠病毒在高温、碱性环境、高锰酸钾和次氯酸钠等消毒剂中生存能力较差,其中次氯酸钠(NaClO)中氯元素的化合价为( )
A . -1
B . +1
C . 0
D . +3
水是人类生活中不可缺少的物质。
-
(1) 下列净水方法中,通常用于除去水中难溶性杂质的是,净水程度最高的是。
A.过滤 B.煮沸 C.蒸馏 D.吸附
-
(2) 自来水厂常用二氧化氯(ClO2)消毒,其中氯元素的化合价为。
-
(3) 自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一。请写出Ca(HCO3)2受热分解的化学方程式:。
-
(4) 如图是电解水的实验装置图,请根据你所了解的知识填空:
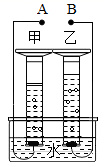
①A为极。甲量筒内产生的气体是;
②甲管与乙管中产生的气体体积比是,
③该实验中往往要在水中滴入氢氧化钠溶液或稀硫酸,其目的是。
④通过该实验可得出水是由组成的。
⑤该反应的化学方程式。
最近更新



