制取气体的反应原理的探究 知识点题库
 2KCl+3O2↑
B . 2H2O
2KCl+3O2↑
B . 2H2O 2H2↑+O2↑
C . 2Na2O2+2CO2═2Na2CO3+O2
D . 2HgO
2H2↑+O2↑
C . 2Na2O2+2CO2═2Na2CO3+O2
D . 2HgO 2Hg+O2↑
2Hg+O2↑
 锰酸钾+二氧化锰+氧气
B . 分离液态空气
C . 过氧化钠(固体)+二氧化碳→碳酸钠(固体)+氧气
D . 过氧化氢
锰酸钾+二氧化锰+氧气
B . 分离液态空气
C . 过氧化钠(固体)+二氧化碳→碳酸钠(固体)+氧气
D . 过氧化氢  水+氧气
水+氧气

-
(1) 实验室用高锰酸钾制取氧气的化学方程式为,选用的发生装置是(填字母序号,下同)。
-
(2) 实验室制取二氧化碳时,选用的收集装置是。将燃着的木条放在瓶口,若观察到,说明瓶中已充满二氧化碳。

-
(1) 仪器①的名称为.
-
(2) 实验室用高锰酸钾制取氧气,反应的化学方程式为,若选用装置AE制取氧气时,发现水槽中的水变红的原因是.
-
(3) 实验室制取二氧化碳时,选用的发生装置是,能用装置C收集该气体的原因是.向该集气瓶中加入紫色石蕊溶液,震荡后,观察到溶液变红,发生反应的化学方程式为.
-
(4) 一种洗气装置如图乙所示,为了检验一氧化碳中混有二氧化碳,气体应从(填“a”或“b”)端导管口通入.

-
(1) 写出标字母仪器的名称:ab;
-
(2) 实验室用氯酸钾和二氧化锰制取氧气,发生装置选;请写出此反应的方程式;如改用高锰酸钾制取氧气,发生装置选用甲,则甲还需作的改动是;
-
(3) 实验室制取并收集二氧化碳的装置组合是;请写出反应的化学反应方程式;
-
(4) 请写出实验室检验二氧化碳的化学方程式;
-
(5) 通常状况下,氨气是一种易溶于水密度比空气小的气体,实验室常用熟石灰和氯化铵固体加热来制取它。则制取和收集氨气的装置组合是。

-
(1) 写出图中②的仪器名称:;
-
(2) 实验室制取二氧化碳时只能选用C装置收集的原因是,收集该气体的验满方法是。
-
(3) 加热高锰酸钾制取氧气发生反应的化学方程式,该反应属于基本反应类型中的反应。
-
(4) 已知氨气的密度比空气小,极易溶于水。可用加热氢氧化钙和氯化铵固体混合物的方法制得。制取并收集氨气的装置组合应选择(填字母序号)。

-
(1) 写出图中标号的仪器名称:a; b。
-
(2) 若用高锰酸钾制取氧气,应选用的发生装置是(填字母编号),管口放棉花的作用是,反应的化学方程式是;如果用F装置收集CO2 , 则CO2应从端进入(填c或d)。
-
(3) 通过查阅资料得知:①氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水;②实验室通过加热氯化铵(NH4Cl)和氢氧化钙的固体混合物制取氨气。则实验室制取氨气应选择的发生和收集装置是。(填字母编号)
①过氧化钠属于氧化物 ②该反应属于置换反应 ③反应前后部分氧元素化合价发生了变化 ④实验室可利用这一原理制取纯净的氧气。

 B . 收集氧气
B . 收集氧气  C . 铁丝在氧气中燃烧
C . 铁丝在氧气中燃烧 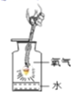 D . 测定空气中氧气的含量
D . 测定空气中氧气的含量 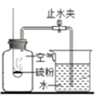
资料:①氯酸钾的熔点约为356℃,二氧化锰的分解温度约为535℃。用酒精灯给物质加热,受热物质的温度一般约为400℃左右;②氯酸钾分解时(图1),传感器得到氧气浓度随温度的变化示意图(图2)及使用不同催化剂时的固体残留率示意图(图3)如下:

-
(1) 实验室利用氯酸钾制取氧气,该化学反应的符号表达式:;分析图2,氯酸钾分解温度(填“高于”、“等于”或“低于”)其熔点。
-
(2) 分析图3,对氯酸钾分解催化效果更好的催化剂是:。
-
(3) 为探究催化剂种类对氯酸钾分解速率的影响,甲同学设计如表对比实验:
氯酸钾的质量
催化剂的种类
MnO2的质量
反应条件
收集45mLO2所需的时间(S)
Ⅰ
3.0g
MnO2
1.0g
混合加热
21
Ⅱ
xg
CuO
1.0g
混合加热
48
表Ⅱ中x的值应为;通过分析上表数据,可以得出的实验结论是:在相同的条件下,氯酸钾在二氧化锰作催化剂比氧化铜作催化剂的分解速率(选填“快”或“慢”)。
-
(4) 小组同学还想继续探究,影响氯酸钾分解速率的因素可能还有:。(填一种因素即可)
(资料)氨气是一种有刺激性气味的气体,密度小于空气,极易溶于水,难溶于CCl4。
-
(1) 探究一氨气制备

写出仪器的名称:a;b
-
(2) 实验室常用浓氨水和氢氧化钠固体在常温下制取氨气,发生装置可以选择图1中,收集装置可选择图1中。某同学用图2中G装置收集氨气,应该从(填“a”或“b”)通入,实验时还需在装置G后接装置H,装置H的作用是。
-
(3) 探究二二氧化碳制备
实验室制取二氧化碳常选择装置C,相对装置B,优点是。
高锰酸钾与草酸反应可以生成二氧化碳气体。某化学小组为了研究外界条件对化学反应速率的影响,进行了酸性高锰酸钾与草酸的反应,记录以下实验数据:
实验编号
实验温度
试管中所加试剂及用量/mL
溶液褪色所需时间/min
H2C2O4溶液
H2O
H2SO4稀溶液
KMnO4溶液
①
25
3.0
2.0
2.0
3.0
1.5
②
25
2.0
3.0
2.0
3.0
2.7
③
50
2.0
V
2.0
3.0
1.0
-
(4) V=。
-
(5) 由实验①②可知,___________(填选项)。A . 其他条件相同时,反应物浓度越大,反应速率越快 B . 其他条件相同时,反应物浓度越小,反应速率越快
-
(6) 为探究温度对反应速率的影响,应选择(填实验编号)。
-
(7) 探究三合成氨气
工业上氨气与二氧化碳在一定条件下合成尿素,该反应符号表达式为:。

-
(8) 如图为某特定条件下,不同水碳比n(H2O)/n(CO2)和温度影响CO2转化率变化的趋势曲线。为了提高产率,提高二氧化碳的转化率,最优的反应条件应该是___________。A . 190℃n(H2O)/n(CO2)=0.3 B . 200℃n(H2O)/n(CO2)=0.5 C . 200℃n(H2O)/n(CO2)=0.3
-
(1) 实验室制取气体时需要的部分装置如图所示,请回答下列问题。

①实验室中可用过氧化氢溶液与二氧化锰制取氧气,反应的化学方程式为,应选用的发生装置是(选填装置字母序号)。
②实验室中用石灰石和稀盐酸制取一瓶干燥、纯净的二氧化碳气体,所选装置的连接顺序为:气体发生装置→→→D(选填装置字母序号)。
-
(2) (信息)二氧化碳不易溶于饱和碳酸氢钠溶液。
③确定实验室制取气体的反应原理时,下列因素中不需要考虑的是(选填字母序号)
A.药品容易获得,能生成所要制取的气体
B.反应条件易于控制,反应速率适中
C.操作简便易行,安全可靠,节能环保
D.所要制取气体的颜色和气味
④制取气体的过程包括;a.选择制取装置;b.验证所得气体;c.明确反应原理。据此总结出实验室里制取气体的一般思路为(填字母)。
-
(3) 某化学兴趣小组为验证酸的通性,做了以下5组实验,请分析并回答问题:
(演示实验)

(提出质疑)实验③没有明显现象,甲同学对该实验是否发生化学反应提出质疑,并设计了以下实验进行验证。
(实验探究)
实验方案
实验操作
实验现象
实验结论
一
测定氧氧化钠溶液的pH=a,滴加稀盐酸后测得溶液pH=b(忽略体积的变化)
a(填“>”“<”或“=”》
发生了反应
二
向实验③所得混合溶液中加入硝酸银溶液
有白色沉淀产生
发生了反应
-
(4) (评价交流)①乙同学认为甲同学的验证实验中方案二不可行,理由是,
②请再设计一个实验证明氢氧化钠溶液与稀盐酸发生了反应。
-
(5) (拓展延伸)演示实验中有一组没有验证酸的通性,该组是(填序号)。请你补充一个演示实验(不改变反应物的类别)完整验证酸的通性,该实验的化学方程式为。

-
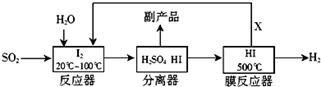
(1) 图中标有序号X的仪器名称是。
-
(2) 确定实验室制取气体的化学反应原理时,下列因素中,不需要考虑的是____(填字母序号)。A . 所要制取气体的颜色和气味 B . 药品容易获得,能生成所要制取的气体 C . 反应条件易于控制,反应速率适中 D . 操作简便易行,安全可靠,节能环保
-
(3) 选用B作为发生装置,用过氧化氢和二氧化锰制取氧气。该反应的化学方程式是。
-
(4) 实验室利用大理石和稀盐酸反应制取二氧化碳,可选用的发生装置和收集装置的组合是(填字母序号):反应后的废液中如果含有稀盐酸不能直接排放,以免污染环境。请你选择下列试剂设计一种实验方案,检验废液中是否含有稀盐酸。
可供选择的试剂:石灰石、硝酸银溶液、紫色石蕊试液、氢氧化钠溶液
实验操作
现象与结论

-
(1) 装置A中发生反应的化学方程式为。
-
(2) ①装置B中饱和NaHCO3溶液的作用是。
②装置C中试剂X应该选用(填字母)。
a.稀H2SO4 b.浓H2SO4 c.KOH溶液
-
(3) 收集CO2并验满。将集满CO2的锥形瓶与盛有足量NaOH溶液的注射器和传感器密封连接,缓慢的将NaOH溶液注入到锥形瓶中,采集信息形成图像。见图。


①检验装置D中CO2已经集满的方法是。
②随着反应的进行,锥形瓶中压强降低的原因是。
③反应结束后锥形瓶中的压强保持在40kPa说明。
-
(4) 取2mL饱和澄清石灰水于试管中,用4mL蒸馏水稀释,向其中缓慢通入足量CO2。测定反应体系的电导率变化如图所示。(忽略反应前后溶液体积的变化)

【查阅资料】
材料一:溶液的导电力越强,溶液的电导率越大。
材料二:单位体积溶液中某离子的个数越多,则该离子的浓度越大,溶液的导电能力越强。相同浓度的不同离子导电能力不同。
材料三:Ca(OH)2溶于水能完全解离出Ca2+和OH-。
CaCO3遇到溶有CO2的水时,能反应生成易溶于水的Ca(HCO3)2 , Ca(HCO3)2在水中能完全解离出Ca2+和
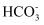 ;。
;。①石灰水中通入CO2气体,溶液的电导率先逐渐降低的主要原因是。
②反应最终电导率的稳定值低于初始值的可能原因是、。
-
(1) 实验室制取某种气体X,X可能为氢气、氧气或二氧化碳。回答下列问题:

①图中用于加热试管的仪器名称是。
②诺将装置A和E连接制取气体X,A中反应的化学方程式为。
③诺用装置B和F制取气体X,装置中a和c相连,则气体X是。
-
(2) 长途运输活鱼常向水中加入过氧化钙(CaO2)固体。某探究小组对过氧化钙进行了如下探究活动。
【操究活动1】①将一定量的过氧化钙加入水中,缓慢产生气泡(经检验该气体能使带火星的木条复燃);
②取少量反应后的液体于试管中,滴加酚酞试液,溶液变红。据此得出反应的化学方程式为
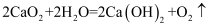 。
。【探究活动2】另取①中上层清液,加入Na2CO3溶液,充分反应后有沉淀生成,生成沉淀的化学方程式为。过滤,得到滤渣和滤液。
-
(3) 【提出问题】滤液中溶质的成分是什么?
【作出猜想】猜想一:NaOH 猜想二: 猜想三:NaOH、Na2CO3
-
(4) 【实验探究】取少量滤液,向其中加入足量稀盐酸,(填写实验现象),猜想三成立。
-
(5) 【反思交流】根据以上探究事实,你认为过氧化钙的用途有(写一条即可)。
编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
仪器及导管 |
|
|
|
|
|
|
-
(1) 已知实验室制备Cl2的反应为
 。组装氯气发生器时,应选用的仪器及导管(填写图中编号)是。
。组装氯气发生器时,应选用的仪器及导管(填写图中编号)是。
-
(2) 实验进行中,按气流方向从左到右的顺序,气体流经的各仪器及导管的编号依次是。
-
(3) 仪器①的橡皮塞上应有个孔,原因是。
-
(4) 实验时,仪器①中除观察到红光外还有现象。
-
(5) 实验需用约10%H2O2溶液100mL,现用市售30%(密度近似为lg/cm3)H2O2来配制,其具体配制方法是。
-
(6) 常温时,Cl2能与NaOH溶液反应生成次氯酸钠、氯化钠和水。该反应的化学方程式为。

-
(1) 写出图中仪器①的名称。
-
(2) 实验室用高锰酸钾制取并收集氧气,应选用的装置为(填序号,在A~E中选取),反应的化学方程式为。
-
(3) 实验室用石灰石和稀盐酸制取二氧化碳,该反应的化学方程式为;若用装置F收集二氧化碳,验满时,燃着木条应放在(填“a”或“b”)端。







