固体溶解度曲线及其作用 知识点题库
如图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述正确的是( )

A . t1℃时,等质量的甲、乙溶液中所含溶质的质量为乙>甲
B . t2℃时,20g丙能溶解于50g水中形成70g溶液
C . 若要将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法
D . t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液溶质质量分数的大小关系为乙>甲>丙
氯化钠、硝酸钾、硒酸镉的溶解度曲线如图所示,据图回答:

-
(1) 溶解度受温度变化影响最大的是
-
(2) t℃时,将25g硒酸镉加入 g水中,完全溶解后,恰好得到饱和溶液,要进一步提高该溶液的溶质质量分数,可进行的操作是;
-
(3) 硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是.
如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )

A . 30℃时,甲的饱和溶液溶质质量分数为40%
B . 20℃时,甲、乙的饱和溶液中所含溶质的质量一定相等
C . 将等质量的甲、乙固体,分别配成30℃的饱和溶液,所需水的质量:甲>乙
D . 将20℃时甲、乙的饱和溶液升温到30℃,所得甲、乙溶液的溶质质量分数相等
如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是 )

A . P点表示甲、丙两种物质的饱和溶液质量相等
B . t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液
C . t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1:4
D . 将三种物质的溶液从t2℃降至t1℃,析出晶体最多的是甲物质
如图是硫酸钠和氯化按的溶解度曲线,请回答:

-
(1) 70℃,硫酸钠的溶解度为 g.
-
(2) 曲线中P点表示.
-
(3) 50℃时,将30g氯化按溶于50g水中,所形成的溶液属于溶液(填“饱和”或“不饱和”).
-
(4) 60℃时,将氯化钱和硫酸钠各30g分别溶于100g水中形成溶液,冷却到20℃时,有晶体析出的是.
右图是甲、乙、丙三种物质的溶解度曲线,下列说法不正确的是( )

A . 甲的溶解度受温度影响最大
B . 10℃时,三种物质的溶解度大小顺序为丙>乙>甲
C . 30℃时,乙、丙两种物质的饱和溶液溶质质量分数相等
D . 50℃时,分别将40g甲、乙两种物质放入100g水中均得到饱和溶液
如图是甲、乙两种固体物质在水中的溶解度曲线。下列说法正确的是( )

A . 20℃时,甲、乙两种物质的溶解度相同
B . 甲物质溶解度大于乙物质溶解度
C . 30℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为90g
D . 将20℃时两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大
如下图是 A、B、C 三种固体物质的溶解度曲线,请回答:

-
(1) 40℃时,A、B、C三种物质饱和溶液溶质的质量分数由大到小顺序是,
-
(2) 20℃时,溶解度大小相等的物质是;
-
(3) 三种物质中,的溶解度受温度影响最大,的溶解度随温度的升高而减小;
-
(4) 将 A 的不饱和溶液变为饱和溶液,可以采取的方法是(任填一种)
如图是A、B两种固体物质的溶解度曲线。

-
(1) 当温度为 ℃时,A、B两种物质的溶解度相等。
-
(2) 欲使饱和状态的B溶液变成不饱和溶液,可采用的一种方法是。
-
(3) t2℃时,将30gA物质加入50g水中,充分溶解后,所得溶液中溶质与溶液的质量比是。
如图是A,B两种物质的溶解度曲线.在t1℃时往两个盛有100克水的烧杯中分别加入a克A物质和b克B物质,充分搅拌后都加热到t2℃.下列说法正确的是( )

A . t1℃时,AB两物质的溶解度相等.两杯溶液均是不饱和溶液
B . t1℃时,AB两物质的溶解度相等,A溶液为饱和溶液,B溶液为不饱和溶液
C . t2℃时,A的溶解度比B的溶解度大,两杯溶液均是不饱和溶液
D . t2℃时,A的溶解度比B的溶解度大,A溶液为不饱和溶液,B溶液为饱和溶液
如图为A,B,C三种固体物质的溶解度曲线,下列说法中正确的是( )

A . 将t2℃的A,B,C的饱和溶液降温到t1℃,溶液中溶质质量分数的关系是B>A=C
B . t1℃时,将20gC物质加入到50g水中充分溶解,得到70gC的饱和溶液
C . 将等质量的A,B,C三种饱和溶液从t2℃降温至t1℃时,所得三种溶液中所含溶剂的质量关系是C>B>A
D . 当A中混有少量B时,可用蒸发结晶的方法提纯A
如图所示,小试管中盛放着固体乙,滴管中有液体甲,广口瓶中有少量饱和的澄清石灰水(试管底部浸没在澄清石灰水中)。当把甲滴加到乙中,过一会儿可看到石灰水变浑浊,右侧气球胀大。根据以上现象请你分析下列说法正确的是( )
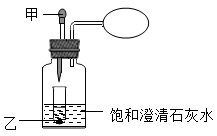
A . 甲、乙一定分别是稀盐酸和碳酸钙
B . 甲、乙有可能分别是水和氢氧化钠
C . 石灰水变浑浊,一定是发生了化学变化
D . 当把甲滴加到乙中广口瓶内的气压降低
甲、乙的溶解度曲线如图所示。下列有关说法正确的是( )
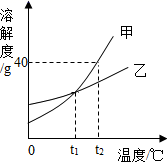
A . 甲的溶解度大于乙
B . t1℃时,甲、乙溶液浓度相同
C . t2℃时,甲溶液中的溶质质量一定大于乙溶液中溶质质量
D . 甲、乙两种饱和溶液分别从t2℃降温到t1℃,两溶液中溶质质量分数相等
如图是甲、乙的溶解度曲线。

-
(1) t1℃时、甲、乙的饱和溶液中溶质的质量分数是。
-
(2) t2℃时,等质量的甲、乙配成饱和溶液,需要水较多的是。
-
(3) t2℃时,90g甲的饱和溶液中加入g水,可以得到质量分数为20%的溶液。
如图是X、Y、Z三种物质的溶解度曲线图,认真阅读完成下列各小题

-
(1) 在℃时,Y、Z两物质溶解度相等。
-
(2) t2℃时,将20gZ放入装有50g水的烧杯中,充分搅拌可能得到gZ的饱和溶液。
-
(3) 在t1℃时把质量均为mg的X、Y、Z三种固体溶于水中形成饱和溶液,需水质量最多的是。
-
(4) 下列说法正确的有(只需填正确的选项序号)。
①Z物质有可能是气体
②若X中含有少量的Y,可用蒸发结晶提纯X
③将t3℃时等质量的X、Y饱和溶液同时降温到t1℃,析出晶体的质量是X>Y
④要将t1℃时接近饱和的X溶液变成饱和溶液,如不改变该溶液的组成,可选择降低温度的方法
⑤将t3℃时Z的饱和溶液降温至t2℃后,溶液的溶质质量分数会变大
-
(5) t2℃时,将X、Y、Z三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数由大到小的顺序是 。
甲、乙、丙三种固体物质在水中的溶解度曲线如图所示,据图回答:

-
(1) 50℃时,物质甲的溶解度是g。
-
(2) 将10℃时的甲、乙、丙三种物质的饱和溶液(溶液底部没有未溶解的固体)升温到50℃,则其溶质质量分数由小到大排列的是(用“>”、“<”、“=”连接)。
-
(3) 50℃时向60g水中加入40g固体甲,得到物质甲溶液质量g,此时溶液中溶质质量分数是(结果精确到0.1%)。
-
(4) 若甲中混有少量的乙,最好采用的方法提纯甲。
KNO3和KCl的溶解度曲线如图所示。下列说法正确的是( )

A . KCl的溶解度小于KNO3的溶解度
B . 10℃时,KNO3饱和溶液的质量分数为20.9%
C . T1℃时,KNO3、KCl两溶液中溶质的质量分数一定相等
D . 将60℃时的KNO3饱和溶液210g冷却至10℃,析出硝酸钾品体89.1g
甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法中正确的是( )

A . 乙的溶解度大于甲的溶解度
B . t2℃时,乙的饱和溶液升温或降温均会析出晶体
C . t3℃时,甲、乙溶液的溶质质量分数会相等
D . t1℃或 t3℃时,100g 乙的饱和溶液中均含有 40g 甲物质
甲、乙两种固体物质的溶解度曲线如图所示。回答下列问题

-
(1) P点表示的意义;
-
(2) 将接近饱和的乙溶液变为饱和溶液,可以采用方法(任选一种);
-
(3) 40℃时,将30克甲固体加入到50克水中,充分溶解,所得溶液的溶质质量分数为;(保留到0.1%)
-
(4) 40℃时,将等质量的甲、乙饱和溶液降温到20℃时,析出的晶体的质量甲乙(填“>”、“=”或“<”);
-
(5) 若甲固体中含有少量乙固体,则采用方法提纯甲。(填“降温结晶”或“蒸发结晶”)
如图3是a、b、c三种物质的溶解度曲线,回答下列问题:

-
(1) P点的含义是。
-
(2) t2℃时,将50ga物质加入100g水中,充分溶解后,所得溶液的质量是g。
-
(3) 若a中含有少量b,可用(蒸发结晶/降温结晶)的方法提纯a。
-
(4) t2℃时,等质量a、b、c三种物质的饱和溶液中溶剂质量由大到小的顺序为。
-
(5) 欲配制6%的氯化钠溶液,如下图:

①用上述图示的序号表示配制溶液的操作顺序(填字母序号)。
②经检测,所配制的溶液质量分数偏小,其原因可能是(填字母序号)。
a.称量前天平未调平,指针偏右
b.氯化钠固体不纯
c.量取水时,仰视读数
d.装瓶时,有少量溶液洒出
最近更新



