分散系、胶体与溶液的概念及关系 知识点题库
氯化铁溶液和氢氧化铁胶体具有的共同性质是:( )
A . 分散质颗粒直径都在1 nm~100 nm之间
B . 能通过半透膜
C . 加热蒸干、灼烧后都有氧化铁生成
D . 呈红褐色
下列分散系中,分散质微粒直径介于10﹣9﹣10﹣7m (l﹣100nm)之间的是( )
A . 溶液
B . 胶体
C . 悬浊液
D . 乳浊液
芳条结寒翠,请君添暖衣.深秋及寒冬的清晨,我们芜湖市经常出现大雾天气,雾中小液滴直径范围是( )
A . 小于1nm
B . 在1~100nm间
C . 大于100nm
D . 无法确定
下列关于胶体的说法不正确的是( )
A . 胶体和溶液一样都不带电,但是胶体中的胶体粒子可能带电
B . 胶体、溶液和浊液这三种分散系的根本区别是分散质粒子直径的大小不同
C . 胶体中的微粒不能透过滤纸
D . 用激光笔的光束照射Fe(OH)3胶体会产生丁达尔效应
淀粉溶液是一种胶体,并且淀粉遇到碘单质,可以出现明显的蓝色特征.现将淀粉和稀Na2SO4溶液混合,装在半透膜中,浸泡在盛蒸馏水的烧杯内,过一段时间后,取烧杯中的液体进行下列实验,能证明半透膜完好无损的是( )
A . 加入BaCl2溶液产生白色沉淀
B . 加入碘水不变蓝
C . 加入BaCl2溶液没有白色沉淀产生
D . 加入碘水变蓝
2013年冬天,多个地区发生持续大雾天气,“PM2.5”数据监测进入公众视野.“PM2.5”是指大气中直径小于或等于2.5微米的细小颗粒物,也称为可入肺颗粒物.下列有关说法中错误的是( )
A . PM2.5表面积大能吸附大量的有毒、有害物质
B . PM2.5在空气中形成的分散系为胶体
C . 实施绿化工程,可以有效地防治PM2.5污染
D . 烟、雾属于胶体,能产生丁达尔效应
下列说法错误的是( )
A . FeO是碱性氧化物
B . 用加热法分离泥沙中的碘单质是化学变化
C . 丁达尔效应可用于区分胶体和溶液
D . Fe2O3+3CO  2Fe+3CO2 是复分解反应
2Fe+3CO2 是复分解反应
阅读下面短文。
光的散射与丁达尔效应
光通过光学性质不均匀的介质时出现偏离原来传播方向,而沿侧向传播的现象,称为光的散射。在暗室里,将一束经聚集后的光线投射到胶体系统上,在与入射光垂直的方向上,可观察到一条明亮的光路,这就是丁达尔效应。产生丁达尔效应的实质是光的散射。
表1 分散系对可见光的不同作用
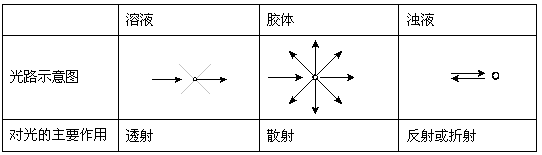
当入射光的波长略大于分散相粒子的直径时就发生光的散射。可见光的波长在400~760 nm的范围,略大于一般胶体粒子的直径(1~100 nm),因此当可见光束投射于胶体时,就发生光的散射,产生丁达尔效应。
对于溶液,分散质分子或离子更小,对可见光的散射作用很微弱;而当可见光束通过浊液时,由于分散质的粒子直径大于入射光的波长,主要发生反射或折射现象。
回答下列问题:
-
(1) 产生丁达尔效应的实质是。
-
(2) 制备Fe(OH)3胶体,在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入5~6滴饱和的溶液,继续煮沸至液体呈红褐色即可。
-
(3) 胶体区别于其他分散系的本质特征是(填序号)。
a.胶体有丁达尔效应 b.胶体粒子可以透过滤纸
c.胶体的胶粒带有电荷 d.胶体粒子的直径在1~100 nm之间
-
(4) CuSO4溶液无明显丁达尔效应的原因是。
研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列有关叙述错误的是( )
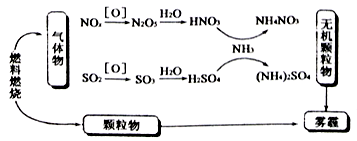
A . 雾和霾的分散质不同分散剂相同
B . 雾霾中含有硝酸铵和硫酸铵
C . NH3是形成无机颗粒物的催化剂
D . 雾霾的形成与过度施用氮肥有关
关于胶体和溶液的本质区别,下列叙述中正确的( )
A . 溶液呈电中性,胶体带电荷
B . 溶液中通过一束光线出现明显光路,胶体中通过一束光线没有特殊现象
C . 溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸
D . 溶液与胶体的本质区别在于分散质微粒直径大小
下列关于胶体的认识及应用正确的是( )
A . 胶体具有电泳现象,是因为胶体带有正电荷或负电荷
B . 纳米材料的粒子直径一般为几纳米或几十纳米(1 nm=10-9m),因此纳米材料属于胶体
C . 向Fe(OH)3胶体中逐滴加入稀硫酸,先产生沉淀然后沉淀逐渐溶解
D . 水泥厂、冶金厂常用高压电除去烟尘,原因是烟尘粒子的直径比较小
朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影……”月光穿过薄雾形成的种种美景本质原因是( )
A . 发生丁达尔效应
B . 空气中的小水滴颗粒的布朗运动
C . 雾是一种胶体,胶粒带有电荷
D . 空气中的小水滴颗粒直径大小约为1~100 nm
活性氧化锌(ZnO)广泛用于橡胶、涂料、陶瓷、电子等行业,以粗氧化锌(主要成分为ZnO,还含有少量MnO、CuO、FeO、Fe2O3等)为原料经深度净化可制备高纯活性氧化锌,其流程如图所示:
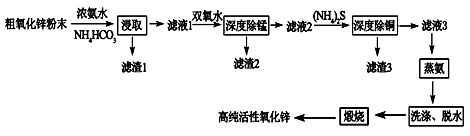
几种难溶物的Ksp:
| 物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | ZnS | CuS |
| Ksp | 1.9×10-13 | 8.0×10-16 | 4.0×10-38 | 2.5×10-22 | 6.4×10-36 |
-
(1) 将大小为66nm的高纯活性氧化锌粉末分散到水中,所得分散系为。
-
(2) “浸取”过程中ZnO与NH3·H2O、NH4HCO3反应生成可溶性的Zn[(NH3)n]CO3和H2O。若有1mol ZnO溶解,则在该转化反应中参加反应的NH3·H2O和NH4HCO3物质的量之比的最大值为(已知:1≤n≤4)。
-
(3) “深度除锰”过程中双氧水可将“滤液1”中的Mn(OH)2转化为更难溶的MnO2·H2O,写出反应的化学方程式,“滤渣2”中存在的物质除了MnO2·H2O还可能含有(用化学式表示)。
-
(4) “深度除铜”过程中当溶液中
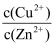 ≤2.0×10-6时,才能满足“深度除铜”的要求,若溶液中Zn2+浓度为1mol/L时,则最终溶液中S2-的浓度理论上的最小值为mol/L。
≤2.0×10-6时,才能满足“深度除铜”的要求,若溶液中Zn2+浓度为1mol/L时,则最终溶液中S2-的浓度理论上的最小值为mol/L。
-
(5) “蒸氨”过程中Zn[(NH3)n]CO3分解为ZnCO3·2Zn(OH)2·H2O、NH3和CO2。为了提高经济效益,请设计循环利用NH3和CO2方案。
-
(6) “煅烧”时ZnCO3·2Zn(OH)2转变为高纯活性氧化锌,写出反应的化学方程式
医学上对血液中毒最常用的净化手段是血液透析。透析时,病人的血液通过浸在透析液中的透析膜进行循环和透析。血液中的蛋白质和血细胞不能透过透析膜,血液内的毒性物质则可以透过,由此可以判断( )
A . 蛋白质、血细胞不溶于水,毒性物质可溶于水
B . 蛋白质以分子形式存在,毒性物质以离子形式存在
C . 蛋白质、血细胞的粒子直径大于毒性物质的粒子直径
D . 蛋白质、血细胞不能透过滤纸,毒性物质能透过滤纸
分类是化学学习与研究的常用方法,下列分类正确的是( )
A . Na2O2、MgO、Al2O3均属于碱性氧化物
B . 纯碱、烧碱、熟石灰均属于碱
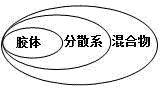
C . 空气、液氯、冰水混合物均属于混合物
D . 混合物、分散系、胶体从属关系如图所示
下列说法正确的是( )
A . K2FeO4溶于水后既能净水又能杀菌消毒
B . 胶体区别于溶液和浊液的本质是丁达尔效应
C . 明矾溶液能净水,主要是明矾中Al3+的毒性
D . 将氯化铁饱和溶液慢慢滴加到沸水中,用玻璃棒搅拌,所得的分散系是胶体
用TiOSO4溶液生产纳米TiO2的工艺流程如下:
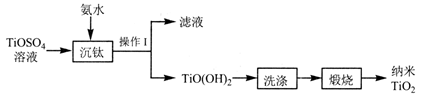
下列说法错误的是( )
A . 在实验室中进行“操作I”,需要的玻璃仪器有烧杯、玻璃棒、漏斗
B . “沉钛”时反应的离子方程式为:‘TiO2++2NH3·H2O=TiO(OH)2↓+2NH  C . 回收“滤液”中的(NH4)2SO4 , 应采用蒸发结晶法
D . 纳米TiO2形成分散系时,具有较好的散射能力
C . 回收“滤液”中的(NH4)2SO4 , 应采用蒸发结晶法
D . 纳米TiO2形成分散系时,具有较好的散射能力
 C . 回收“滤液”中的(NH4)2SO4 , 应采用蒸发结晶法
D . 纳米TiO2形成分散系时,具有较好的散射能力
C . 回收“滤液”中的(NH4)2SO4 , 应采用蒸发结晶法
D . 纳米TiO2形成分散系时,具有较好的散射能力
下列说法正确的是( )
A . 咳嗽形成的飞沫气溶胶属于胶体分散系
B . “城市空气质量日报”报道的内容包括CO2、NO、SO2、可吸入颗粒物等
C . 口罩熔喷布的原料聚丙烯属于天然有机高分子
D . 蚕丝、羊毛和棉花的主要成分都是蛋白质
下列不能产生“丁达尔效应”的分散系是( )
A . 硫酸钾溶液
B . 氢氧化铁胶体
C . 雾
D . 水
下列说法正确的是( )
A . 混合物均由两种或两种以上的元素组成
B . 液态 不导电,所以
不导电,所以 不是电解质
C . 胶体区别于溶液和浊液的本质特征是分散质微粒直径介于
不是电解质
C . 胶体区别于溶液和浊液的本质特征是分散质微粒直径介于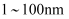 D . 盐类物质一定含有金属阳离子
D . 盐类物质一定含有金属阳离子
 不导电,所以
不导电,所以 不是电解质
C . 胶体区别于溶液和浊液的本质特征是分散质微粒直径介于
不是电解质
C . 胶体区别于溶液和浊液的本质特征是分散质微粒直径介于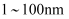 D . 盐类物质一定含有金属阳离子
D . 盐类物质一定含有金属阳离子
最近更新



