电解质与非电解质 知识点题库
下列状态的物质,既能导电又属于电解质的是( )
A . MgCl2晶体
B . NaCl溶液
C . 液态氯化氢
D . 熔融的KOH
现有下列物质:
①Na2CO3 ②铜 ③氯化氢 ④CO2 ⑤NaHSO4 ⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水 ⑨稀硝酸 ⑩KI
-
(1) 按物质的分类方法填写表格的空白处(填物质编号)
分类标准
电解质
盐
非电解质
混合物
属于该类
的物质
-
(2) 上述某两种物质在溶液中可发生离子反应:H++OH﹣═H2O,写出其中一个该离子反应对应的化学方程式.
-
(3) 物质⑩的稀溶液在空气中被氧化,加入淀粉溶液显蓝色,则反应的离子方程式为:.
下列物质属于电解质的是属于非电解质的是
①NaNO3溶液②H2SO4 ③蔗糖 ④Ba(OH)2⑤SO3⑥Fe ⑦MgO ⑧NH3 .
下列化合物中,只有在水溶液中才能导电的电解质是( )
A . NaCl
B . CH3CH2OH(酒精)
C . H2SO4
D . CO2
下列属于电解质并能导电的物质是( )
A . 乙醇
B . KNO3溶液
C . Fe
D . 熔融的Na2O
现有常温下体积均为10 mL、 pH=3的两种溶液:① HCl溶液,② CH3COOH溶液。下列说法中,正确的是( )
A . 溶液中溶质的物质的量浓度:① > ②
B . 溶液中酸根的物质的量浓度:① = ②
C . 加水稀释至1 L,溶液的pH:① < ②
D . 分别加入等浓度NaOH溶液至中性,消耗NaOH的量:① = ②
下列有关电解质的叙述正确的是( )
A . 液态HCl不导电,所以HCl是非电解质
B . NH3的水溶液能够导电,所以NH3是电解质
C . 液态Cl2不导电,所以Cl2是非电解质
D . 熔融NaCl可以导电,所以NaCl是电解质
下列物质:
①Cu ②石墨 ③Na2O ④CO2 ⑤NH3 ⑥H2SO4 ⑦Ba(OH)2 ⑧蔗糖
⑨NaCl溶液。(填序号)
-
(1) 能导电的是 ,
-
(2) 属于电解质的是,
-
(3) 属于非电解质的是。
下列说法正确的是( )
A . 化学变化中往往伴随着化学键的破坏与形成,物理变化中一定没有化学键的破坏或形成
B . 硫酸钾和硫酸溶于水都电离出硫酸根离子,所以它们在熔融状态下都能导电
C . 在N2、CO2和SiO2物质中,都存在共价键,它们都是由分子构成
D . H2和Cl2在光照条件反应生成HCl,一定有共价键的断裂和形成
下列物质的水溶液均能导电,其中属于电解质的是( )
A . SO2
B . Cl2
C . NH4HCO3
D . NH3
-
(1) 按要求写出方程式:
①HNO3(电离方程式) 。
②Fe2(SO4)3(电离方程式) 。
③硫酸钠和氯化钡溶液反应(离子方程式) 。
④二氧化碳通入足量氢氧化钠溶液(离子方程式)。
-
(2) 以下为中学化学中常见的几种物质:①二氧化碳 ②熔融KCl ③NaHSO4固体 ④铜 ⑤稀硫酸 ⑥澄清石灰水,其中属于电解质的有,属于非电解质的有(填序号)。
-
(1) I.如图是按一定的方法给物质进行的分类。

该物质分类方法名称是,类别1是,类别2是。
-
(2) 上述物质中属于电解质的是。
-
(3) II.同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰(CaO)。
生石灰属于(填“酸性氧化物”或“碱性氧化物”)。
-
(4) 生石灰可作干燥剂的理由是(用化学方程式表示)。
-
(5) 生石灰与稀盐酸反应的离子方程式。
下列属于非电解质的是( )
A . 氨气
B . 碳酸钾
C . HCl
D . 氢气
下列物质属于电解质的是( )
A . 酒精
B . 石墨
C . 盐酸
D . 水
下列物质组合正确的是( )
| 序号 | 纯净物 | 混合物 | 非电解质 | 弱电解质 | 强电解质 |
| A | 盐酸 | 水煤气 | HD | 醋酸 | 硫酸 |
| B | 胆矾 | 漂白粉 | NH3 | HNO2 | 硫酸钡 |
| C | 火碱 | 蔗糖溶液 | 三氧化硫 | 氨水 | 碳酸氢钠 |
| D | 冰醋酸 | 福尔马林 | 乙醇 | 碘化氢 | 苛性钾 |
A . A
B . B
C . C
D . D
下列物质属于电解质,且能导电的是( )
A . 金属铜
B . 熔融氯化钠
C . H2SO4
D . NH3
阅读下列材料,回答问题:
含硫矿物如黄铁矿(FeS2)、黄铜矿、芒硝在工业上有着重要的用途。收集黄铜矿炼铜过程中产生的SO2制备SO3 , 其反应为2SO2(g)+O2(g)  2SO3(g)
2SO3(g) 
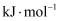
-
(1) 指定条件下,下列物质转化不能实现的是( )A .
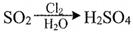 B .
B .  C .
C .  D .
D . 
-
(2) 下列关于2SO2(g)+O2(g)
 2SO3(g)说法正确的是( )
A . 该反应的
2SO3(g)说法正确的是( )
A . 该反应的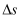 >0
B . 该反应中,反应物的总能量小于生成物的总能量
C . 生产过程中将SO3分离出去,逆反应速率减慢
D . 其他条件不变,增大压强,平衡右移,平衡常数增
>0
B . 该反应中,反应物的总能量小于生成物的总能量
C . 生产过程中将SO3分离出去,逆反应速率减慢
D . 其他条件不变,增大压强,平衡右移,平衡常数增
-
(3) 下列有关说法正确是( )
 A . SO2溶于水所得溶液能导电,所以SO2是电解质 B .
A . SO2溶于水所得溶液能导电,所以SO2是电解质 B . 的空间构型为平面三角形
C . 电负性:O<S
D . 黄铜矿的晶胞如图所示,则其化学式为:CuFeS2
的空间构型为平面三角形
C . 电负性:O<S
D . 黄铜矿的晶胞如图所示,则其化学式为:CuFeS2
-
(4) 工业上通过惰性电极电解Na2SO4浓溶液来制备氢氧化钠和硫酸,a、b为离子交换膜,装置如下图所示,下列说法正确的是( )
 A . c电极与外接电源负极相连 B . a为阴离子交换膜 C . 从d端注入的是稀NaOH溶液 D . 生成标状况下22.4L的02,将有2molNa+穿过阳离子
A . c电极与外接电源负极相连 B . a为阴离子交换膜 C . 从d端注入的是稀NaOH溶液 D . 生成标状况下22.4L的02,将有2molNa+穿过阳离子交换膜
按要求填空:
-
(1) Ⅰ.现有7种物质:①Na、②FeCl3溶液、③稀盐酸、④熔融的KNO3、⑤CO2、⑥Fe(OH)3胶体、⑦NH4Cl晶体。
属于非电解质的是;上述状态下的物质能导电的电解质有 (填序号)。
-
(2) 制备⑥的方法是:在小烧杯中加入40mL蒸馏水,加热至沸腾后,向烧杯中加入5至6滴FeCl3饱和溶液,继续煮沸至液体呈色,即可制得
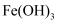 胶体。区分Fe(OH)3胶体和FeCl3溶液的常用物理方法是。
胶体。区分Fe(OH)3胶体和FeCl3溶液的常用物理方法是。
-
(3) FeCl3在水溶液中的电离方程式是。
-
(4) Ⅱ.完成下列问题
在标准状况下,33.6LCH4的质量是。
-
(5) 相同质量的SO2和SO3 , 氧原子数之比为。
下列物质能导电,但不属于电解质的是( )
A . 浓硝酸
B . 熔融的NaCl
C . 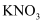 晶体
D . 液氨
晶体
D . 液氨
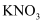 晶体
D . 液氨
晶体
D . 液氨
下列物质属于电解质的是( )
A . 硫酸
B . 铜
C . 氯化钠溶液
D . 酒精
最近更新



