钠的化学性质 知识点题库
下列灭火剂能用于扑灭金属钠着火的是( )
A . 煤油
B . 砂土
C . 干粉(含NaHCO3)灭火剂
D . 水
下列有关钠的叙述正确的是①钠在空气中燃烧生成氧化钠②金属钠可以保存在煤油中③钠与硫酸铜溶液反应,可以置换出铜④金属钠有强还原性⑤钠原子的最外层上只有一个电子,所以在化合物中钠的化合价显+1价
A . ①②④
B . ②③⑤
C . ①④⑤
D . ②④⑤
少量金属钠分别与下列溶液反应时,既有气体又有沉淀产生的是( )
A . HCl
B . NaCl
C . AlCl3
D . Na2SO4
当一小块金属钠久置在潮湿的空气中,可能有如下现象产生:①生成白色粉未;②表面变暗;③生成白色块状固体;④发生潮解,表面产生液体.这些现象的先后顺序为( )
A . ①②③④
B . ②③④①
C . ②①③④
D . ④②③①
下列物质发生化学反应时,在不同条件下,可得到不同产物的是( )
①P+Cl2②P2O5+H2O③H2S+O2④Na+O2 .
A . 只有①②
B . 只有③④
C . 只有②③④
D . 全部
下列叙述正确的是( )
A . Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
B . Na2CO3溶液和NaHCO3溶液都能跟CaCl2溶液反应得到白色沉淀
C . 钠在常温下不容易被氧化
D . 石蕊试液中加入Na2O2粉末,先变蓝后褪色,并有气泡生成
下列说法错误的是( )
A . 钠在空气中燃烧最后所得产物为Na2O2
B . 镁因在空气中形成了一层致密的氧化膜,保护了里面的镁,故镁不需要进行特殊保护
C . 铝制品在生活中非常普遍,这是因为铝不活泼
D . 铁在潮湿的空气中因为生成的氧化膜很疏松不能保护内层金属,故铁制品往往需涂保护层
做化学实验必须注意实验安全。下列做法正确的是( )
A . 金属钠保存在四氯化碳中
B . 制氯气在通风橱中进行
C . 金属钠着火用小苏打干粉灭火
D . 发生火灾拨打110报警电话
将一块金属钠投入到滴有紫色石蕊溶液的盛冷水的烧杯中,甲同学认为可观察到下列现象,其中正确的有( )
①钠投入水中,先沉入水底,后浮出水面 ②钠立即与水反应,并有气体产生 ③反应后溶液变红 ④钠熔成闪亮的小球 ⑤小球在水面上四处游动 ⑥有“嘶嘶”的响声发出
A . ①②③④
B . ②③④⑤
C . ②④⑤⑥
D . ②③④⑤⑥
下列说法正确的是( )
A . 钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+
B . Na2O2与水反应时,生成0.1molO2 , 转移的电子数为0.2NA
C . Na2O2遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
D . 在酒精灯加热条件下,Na2CO3和 NaHCO3固体都能发生分解
把2.3 g钠投入38.8 g水中,发生化学反应。假设水蒸发损失1 g,所得溶液中溶质的质量分数为( )
A . 4.6%
B . 7.7%
C . 10.0%
D . 8.0%
图中,A为一种中学化学中常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色实验均为黄色。
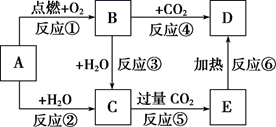
-
(1) 写出A的原子结构示意图,B的化学式。
-
(2) 以上6个反应中属于氧化还原反应的有(填写编号)。
-
(3) 写出B→D反应的化学方程式,C溶液→E反应的离子方程式。
-
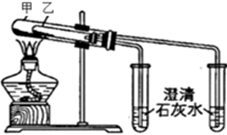
(4) 若用所示装置验证D和E的稳定性,则试管乙中装入的固体最好是(填化学式)。
-
(5) 将一定量的B投入到含有下列离子的溶液中:
 、
、  、
、  、Na+ , 反应完毕后,溶液中上述离子数目几乎不变的有(不考虑溶液体积的变化)填离子符号)。
、Na+ , 反应完毕后,溶液中上述离子数目几乎不变的有(不考虑溶液体积的变化)填离子符号)。
下列实验操作正确的是( )
| 选项 | 实验 | 操作 |
| A | 观察钠与水反应的现象 | 用镊子从煤油中取出金属钠,切下黄豆大小的钠,小心放入装满水的烧杯中 |
| B | 检验NaHCO3溶液与Na2CO3溶液 | 用小试管分别取少量溶液,然后滴加澄清石灰水 |
| C | 证明Na2O2与CO2是放热反应 | Na2O2用棉花包裹,放入充满CO2的集气瓶中,棉花燃烧,说明该反应是放热反应 |
| D | 检验Na2CO3溶液与K2CO3溶液 | 用铂丝分别蘸取溶液,在酒精灯外焰上灼烧,直接观察火焰的颜色 |
A . A
B . B
C . C
D . D
下列说法错误的是( )
A . 二氧化硅导电能力强,可用于制造光导纤维
B . 石灰石在高温下可用于消除燃煤烟气中的  C . 钠着火不能用泡沫灭火器灭火
D . 利用催化剂可减少汽车尾气中有害气体的排放
C . 钠着火不能用泡沫灭火器灭火
D . 利用催化剂可减少汽车尾气中有害气体的排放
 C . 钠着火不能用泡沫灭火器灭火
D . 利用催化剂可减少汽车尾气中有害气体的排放
C . 钠着火不能用泡沫灭火器灭火
D . 利用催化剂可减少汽车尾气中有害气体的排放
某实验小组对中学课本中可生成氢气的反应进行了研究,总结出两个可以生成H2的反应:①Zn+盐酸,②Na+水。为点燃上述两个反应生成的H2 , 他们设计了图示装置。请回答下列问题:

-
(1) 写出Na与H2O反应的化学方程式:。
-
(2) 实验小组在点燃用上述装置制得的H2时,①实验获得成功,②却失败了。他们分析认为失败的原因是Na的用量太少,Na与H2O的反应速率太快。于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因是。
-
(3) 实验小组查阅钠、煤油、水的密度分别为0.97 g·cm-3、0.80 g·cm-3、1.00 g·cm-3 , 并据此对实验进行改进。在改进后的实验中H2的生成速率减慢,原因是。
下列说法不正确的是( )
A . 硅酸钠是一种难溶于水的硅酸盐
B . 镁在空气中燃烧可生成氧化镁和氮化镁
C . 钠与水反应生成氢氧化钠和氢气
D . 常温下,铝遇浓硝酸或浓硫酸时会发生钝化
根据你对金属钠性质的了解,下列叙述中,正确的是( )
①钠是银白色金属,硬度很大
②金属钠的熔点很高
③金属钠在空气中燃烧,生成氧化钠
④加热时,金属钠剧烈燃烧,产生黄色火焰,生成过氧化钠
⑤金属钠在氯气中燃烧,产生白色烟雾
⑥金属钠放置在空气中,最终变成碳酸氢钠
⑦当金属钠与硫酸铜溶液反应时,有大量蓝色沉淀出现
A . ①②③④
B . ⑤⑥⑦
C . ④⑤⑦
D . ④⑦
化合物A由两种元素组成,是一种重要的还原剂,在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3)。将4.80g化合物A隔绝空气加热至完全分解,得到金属单质X和2.24L的气体Y;所得单质X与水反应又得到2.24L气体Y和强碱溶液Z(题中气体体积均已折算为标准状况)。
回答下列问题:
-
(1) 气体Y的分子式为;
-
(2) 单质X与水反应的化学方程式;
-
(3) 化合物A在钢铁制品脱锈过程发生反应的化学方程式;
-
(4) 化合物A化学活性很高,在潮湿空气中能自燃。若着火,(填“能”或“不能”)用二氧化碳灭火;若不能,写出原因(用化学方程式表示)。
列关于实验的叙述中,正确的是( )
| 选项 | 实验操作 | 实验现象或结论 |
| A | 把一小块钠迅速投入到热坩埚中,继续加热坩埚片刻 | 钠受热后熔成小球,剧烈燃烧,火焰呈黄色,产物为淡黄色固体 |
| B | 把小块钠投入到滴有紫色石蕊试液的盛冷水中 | 钠熔化成闪亮的小球,在水面上四处游动,有“嘶嘶”的响声发出,反应后溶液变红 |
| C | 将有色鲜花放入盛有干燥氯气的集气瓶中,盖上玻璃片 | 鲜花褪色,证明氯气具有漂白性 |
| D | 用洁净铂丝蘸取溶液,在酒精喷灯外焰上灼烧,观察到火焰呈黄色 | 溶液中一定存在 Na+ ,不存在 K+ |
A . A
B . B
C . C
D . D
下列各组中的物质,不能发生化合反应的是( )
A . Na与Cl2
B . Na2O与H2O
C . Al2O3与HCl
D . FeO与O2
最近更新



